 和CO可在催化剂(
和CO可在催化剂( )表面转化为无害气体,其反应原理为
)表面转化为无害气体,其反应原理为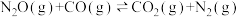 ,下列有关该反应说法正确的是
,下列有关该反应说法正确的是A.催化剂能改变反应的 |
B.通入过量CO,可使 转化率达100% 转化率达100% |
| C.保持反应容器体积不变,通入He增大压强,反应速率不变 |
D.单位时间内消耗n mol  同时生成n mol 同时生成n mol  ,则反应一定达到平衡状态 ,则反应一定达到平衡状态 |
更新时间:2022-01-23 22:01:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
| A.NaOH固体 | B.NH4Cl固体 |
| C.CH3COONa固体 | D.NaNO3固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于化学反应说法正确的是
| A.活化分子之间的碰撞一定是有效碰撞 |
| B.增大反应物的浓度,可使单位体积内活化分子百分数增多,反应速率加快 |
| C.增大体系压强,可使单位体积内活化分子百分数增多,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内活化分子百分数增加,反应速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,有反应: CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol测得n(N2)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol测得n(N2)随时间变化数据如下表:
下列说法不正确的是
 N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol测得n(N2)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol测得n(N2)随时间变化数据如下表:| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(N2) | 0 | 0.20 | 0.25 | 0.40 | 0.40 |
| T2 | n(N2) | 0 | 0.25 | …… | 0.30 | 0.30 |
下列说法不正确的是
| A.0~10 min内,T1时V(N2)的平均反应速率比T2时的平均反应速率小 |
| B.T1<T2 |
| C.a < 0 |
| D.在温度为T2时,向平衡后的容器中再充入1.2mol CH4,重新达平衡时n(N2)=0.40mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在恒温恒压的密闭体系中,可逆反应:A(s)+2B(g)⇌2C(g)ΔH<0,能作为该反应达到化学平衡的标志的是
①v正(B)=v逆(C)
②n(B)∶n(C)=1∶1
③容器内压强不再改变
④容器内气体的密度不再改变
⑤容器内混合气体的平均相对分子质量不再改变
①v正(B)=v逆(C)
②n(B)∶n(C)=1∶1
③容器内压强不再改变
④容器内气体的密度不再改变
⑤容器内混合气体的平均相对分子质量不再改变
| A.②③④ | B.①③④ | C.②③⑤ | D.①④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关接触氧化反应2SO2+O2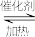 2SO3的说法中正确的是
2SO3的说法中正确的是
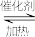 2SO3的说法中正确的是
2SO3的说法中正确的是| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.该反应达到平衡后,反应就完全停止了,即正、逆反应速率均为零 |
| C.在达到平衡的体系中,充入由18O原子组成的O2后,SO2中18O含量减少,SO3中18O含量增多 |
| D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
您最近一年使用:0次



