某工厂的废水中含有较多的 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
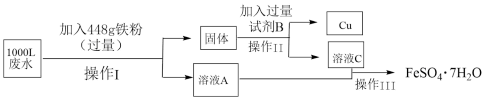
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为___________ 。
(2)操作Ⅰ和操作Ⅱ的名称是___________ ,所用到的玻璃仪器有___________ 。
(3)流程中“固体”的主要成分是___________ (填化学式);加入试剂B所发生反应的化学方程式为___________ 。
(4)操作Ⅲ包括蒸发浓缩、___________ 、过滤、___________ 、干燥。
(5)设计实验方案检验废水中是否含有 :
:___________ 。
(6)若废水中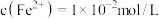 ,
,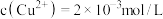 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是___________ g。
 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为
(2)操作Ⅰ和操作Ⅱ的名称是
(3)流程中“固体”的主要成分是
(4)操作Ⅲ包括蒸发浓缩、
(5)设计实验方案检验废水中是否含有
 :
:(6)若废水中
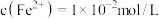 ,
,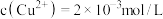 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是
更新时间:2022-01-24 17:38:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】正盐A、B均含有三种元素。且所含元素种类相同。24.5g的A在加热条件下发生如图变化。已知:生成的标况下2.24L的气体D,能使得火星的水条复燃。透过蓝色钴玻璃,A、B、C的焰色实验均为紫色,往C的溶液中加入AgNO3溶液,出现白色沉淀。再加入稀硝酸,沉淀不溶解,且质量称得为14.35g。请回答:

(1)D的物质的量为____________ mol,C的化学式为____________ 。
(2)写出A分解的化学方程式______________ 。

(1)D的物质的量为
(2)写出A分解的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】新冠肺炎期间,化学消毒剂大显身手.高铁酸钾 是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
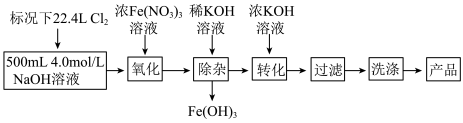
已知:转化过程发生复分解反应.
回答下列问题:
(1)配制上述 溶液,需要
溶液,需要 的质量为
的质量为_______________ 。
(2)下列操作可能导致溶液浓度偏大的有_______________ (填序号)。
A.将 放在滤纸上称量
放在滤纸上称量
B. 溶液转移到容量瓶后,未洗涤玻璃棒就定容
溶液转移到容量瓶后,未洗涤玻璃棒就定容
C.容量瓶洗净之后未干燥
D.定容时俯视刻度线
E.摇匀后发现液面低于刻度线,再加水至刻度线
(3) 溶液应置于冰水浴中,否则温度升高将发生如下副反应:
溶液应置于冰水浴中,否则温度升高将发生如下副反应:
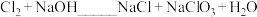 (未配平)
(未配平)
①若有 发生该副反应,该过程中转移电子数目为
发生该副反应,该过程中转移电子数目为_______________ ;
②若反应后溶液中 和
和 的物质的量之比为
的物质的量之比为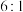 ,则生成
,则生成 和
和 的物质的量之比为
的物质的量之比为__________ 。
(4)氧化过程中溶液保持碱性.写出反应的离子方程式:______________ 。
(5) ,试解释该反应能发生的原因
,试解释该反应能发生的原因__________ 。
(6)产品经干燥后得到纯品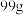 ,则
,则 的产率为
的产率为____________ (用百分数表示)。
 是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
已知:转化过程发生复分解反应.
回答下列问题:
(1)配制上述
 溶液,需要
溶液,需要 的质量为
的质量为(2)下列操作可能导致溶液浓度偏大的有
A.将
 放在滤纸上称量
放在滤纸上称量B.
 溶液转移到容量瓶后,未洗涤玻璃棒就定容
溶液转移到容量瓶后,未洗涤玻璃棒就定容C.容量瓶洗净之后未干燥
D.定容时俯视刻度线
E.摇匀后发现液面低于刻度线,再加水至刻度线
(3)
 溶液应置于冰水浴中,否则温度升高将发生如下副反应:
溶液应置于冰水浴中,否则温度升高将发生如下副反应: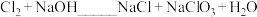 (未配平)
(未配平)①若有
 发生该副反应,该过程中转移电子数目为
发生该副反应,该过程中转移电子数目为②若反应后溶液中
 和
和 的物质的量之比为
的物质的量之比为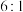 ,则生成
,则生成 和
和 的物质的量之比为
的物质的量之比为(4)氧化过程中溶液保持碱性.写出反应的离子方程式:
(5)
 ,试解释该反应能发生的原因
,试解释该反应能发生的原因(6)产品经干燥后得到纯品
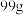 ,则
,则 的产率为
的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】明矾 可做中药,性味酸涩、寒、有毒。利用废铝制备明矾,并测定其组成,实验过程如下。
可做中药,性味酸涩、寒、有毒。利用废铝制备明矾,并测定其组成,实验过程如下。
Ⅰ.制备明矾
实验步骤如图:
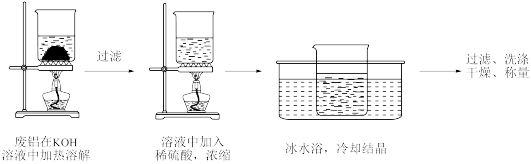
(1)溶解步骤中主要发生的离子反应方程式为_______ 。
(2)用蒸馏水洗涤晶体的操作过程是_______ 。
(3)生活中明矾可用作净水剂,结合离子方程式说明净水原理:_______ 。
Ⅱ.样品中硫酸根的测定
(一)绘制标准硫酸钡悬浊液吸光光谱图
①分别量取0、1.0、2.0、3.0、4.0mL浓度为500μg/mL的标准硫酸钾溶液移入10mL的比色管中,然后分别加入5mL浓度为1g/mL的 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
②用分光光度计测量标准系列(波长采用420nm),数据如下(忽略混合过程中的体积变化)。
③绘制硫酸钡悬浊液的吸光光谱图,绘制如下。
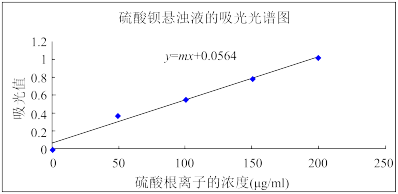
(4)上述实验数据中b=_______ ,m=_______ (保留1位有效数字)。
(二)测定样品中硫酸根浓度
①称取1.018g样品晶体配制成250mL的样品溶液。
②量取1.0mL样品溶液移入10mL的比色管中,然后加入5mL浓度为1g/mL的 溶液,用蒸馏水定容,测得样品的吸光值为0.858。
溶液,用蒸馏水定容,测得样品的吸光值为0.858。
(5)测得样品中硫酸根的质量分数为_______ %(保留2位有效数字)。
(6)实验测得硫酸根的含量小于理论值,可能的原因有_______(填标号)。
 可做中药,性味酸涩、寒、有毒。利用废铝制备明矾,并测定其组成,实验过程如下。
可做中药,性味酸涩、寒、有毒。利用废铝制备明矾,并测定其组成,实验过程如下。Ⅰ.制备明矾
实验步骤如图:

(1)溶解步骤中主要发生的离子反应方程式为
(2)用蒸馏水洗涤晶体的操作过程是
(3)生活中明矾可用作净水剂,结合离子方程式说明净水原理:
Ⅱ.样品中硫酸根的测定
(一)绘制标准硫酸钡悬浊液吸光光谱图
①分别量取0、1.0、2.0、3.0、4.0mL浓度为500μg/mL的标准硫酸钾溶液移入10mL的比色管中,然后分别加入5mL浓度为1g/mL的
 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。②用分光光度计测量标准系列(波长采用420nm),数据如下(忽略混合过程中的体积变化)。
 (mL) (mL) | 1.0 | 2.0 | 3.0 | 4.0 | |
| 蒸馏水体积(mL) | 5 | a | b | c | 1 |
 浓度(μg/mL) 浓度(μg/mL) | 0 | 50 | 100 | 150 | 200 |
| 吸光值A | 0 | 0.371 | 0.553 | 0.778 | 1.013 |

(4)上述实验数据中b=
(二)测定样品中硫酸根浓度
①称取1.018g样品晶体配制成250mL的样品溶液。
②量取1.0mL样品溶液移入10mL的比色管中,然后加入5mL浓度为1g/mL的
 溶液,用蒸馏水定容,测得样品的吸光值为0.858。
溶液,用蒸馏水定容,测得样品的吸光值为0.858。(5)测得样品中硫酸根的质量分数为
(6)实验测得硫酸根的含量小于理论值,可能的原因有_______(填标号)。
A.实验Ⅰ制得样品中有 杂质 杂质 | B.实验中所用标准硫酸钾溶液浓度偏大 |
| C.样品溶液配制过程中,定容仰视读数 | D.样品溶液配制过程中,容量瓶未润洗 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学在实验室进行铁盐与亚铁盐相互转化实验。
实验I:将Fe3+转化为Fe2+

(1) Fe3+与Cu粉发生反应的离子方程式为___________ 。
(2)探究白色沉淀产生的原因,请填写实验方案:
CuSO4溶液与KSCN溶液反应产生了白色沉淀查阅资料:
已知:①SCN-的化学性质与I-相似;②2Cu2++4I-=2CuI↓+I2。
Cu2+与SCN-反应的离子方程式为___________ 。
实验II:将Fe2+转化为Fe3+
探究上述现象出现的原因:
查阅资料:Fe2++NO=Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因___________ 。
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应I:Fe2+与HNO3反应;反应II:Fe2+与NO反应
①据实验现象,可推知反应I的速率比反应II的___________ (填“快”或“慢”)。
②反应I是一个不可逆反应,设计实验方案加以证明:___________ 。
实验I:将Fe3+转化为Fe2+

(1) Fe3+与Cu粉发生反应的离子方程式为
(2)探究白色沉淀产生的原因,请填写实验方案:
| 实验方案 | 现象 | 结论 |
| 步骤1:取4mL | 产生白色沉淀 | |
| 步骤2:取 | 无明显现象 |
已知:①SCN-的化学性质与I-相似;②2Cu2++4I-=2CuI↓+I2。
Cu2+与SCN-反应的离子方程式为
实验II:将Fe2+转化为Fe3+
| 实验方案 | 现象 |
| 向3mL0.1 mol∙L-1FeSO4溶液中加入1mL稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
查阅资料:Fe2++NO=Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应I:Fe2+与HNO3反应;反应II:Fe2+与NO反应
①据实验现象,可推知反应I的速率比反应II的
②反应I是一个不可逆反应,设计实验方案加以证明:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
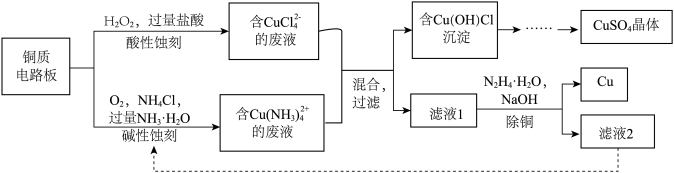
【推荐2】铜质电路板可采用酸性蚀刻与减性蚀刻两种方法,将二者的废液混合可实现回收再利用,其主要流程如下: 具有强还原性,易被氧化为
具有强还原性,易被氧化为 。
。
ii. 形成配合物后,氧化性降低。
形成配合物后,氧化性降低。
(1)蚀刻
①酸性蚀刻过程中盐酸的作用是______________ 。
②将碱性蚀刻铜的离子方程式补充完整:__________ 。
☐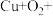 ☐_______+☐_______=☐
☐_______+☐_______=☐ +☐_______
+☐_______
③关于蚀刻的下列说法正确的是_________ (填字母)。
A.用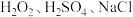 也可以使
也可以使 溶解
溶解
B.碱性蚀刻和酸性蚀刻分别利用了 的氧化性和
的氧化性和 的还原性
的还原性
C.在碱性蚀刻和酸性蚀刻中,溶解相同质量的 转移的电子数之比为
转移的电子数之比为
(2)滤液1的 约为5,其中除少量
约为5,其中除少量 外,还大量存在的离子是
外,还大量存在的离子是_______________ 。
(3)除铜
①利用水合肼 还原
还原 的离子方程式是
的离子方程式是_________________ 。
②已知滤渣中除金属铜外不含其他形式的含 沉淀。测得铜去除率、水合肼还原能力随溶液
沉淀。测得铜去除率、水合肼还原能力随溶液 的变化情况如图所示。
的变化情况如图所示。 时,铜去除率随
时,铜去除率随 增大而减小,结合图给信,息和已知信息分析其原因:
增大而减小,结合图给信,息和已知信息分析其原因:________________ 。
 具有强还原性,易被氧化为
具有强还原性,易被氧化为 。
。ii.
 形成配合物后,氧化性降低。
形成配合物后,氧化性降低。(1)蚀刻
①酸性蚀刻过程中盐酸的作用是
②将碱性蚀刻铜的离子方程式补充完整:
☐
 ☐_______+☐_______=☐
☐_______+☐_______=☐ +☐_______
+☐_______③关于蚀刻的下列说法正确的是
A.用
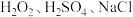 也可以使
也可以使 溶解
溶解B.碱性蚀刻和酸性蚀刻分别利用了
 的氧化性和
的氧化性和 的还原性
的还原性C.在碱性蚀刻和酸性蚀刻中,溶解相同质量的
 转移的电子数之比为
转移的电子数之比为
(2)滤液1的
 约为5,其中除少量
约为5,其中除少量 外,还大量存在的离子是
外,还大量存在的离子是(3)除铜
①利用水合肼
 还原
还原 的离子方程式是
的离子方程式是②已知滤渣中除金属铜外不含其他形式的含
 沉淀。测得铜去除率、水合肼还原能力随溶液
沉淀。测得铜去除率、水合肼还原能力随溶液 的变化情况如图所示。
的变化情况如图所示。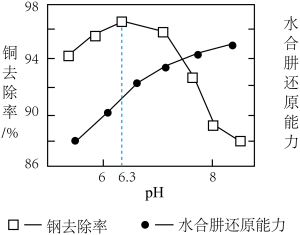
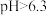 时,铜去除率随
时,铜去除率随 增大而减小,结合图给信,息和已知信息分析其原因:
增大而减小,结合图给信,息和已知信息分析其原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
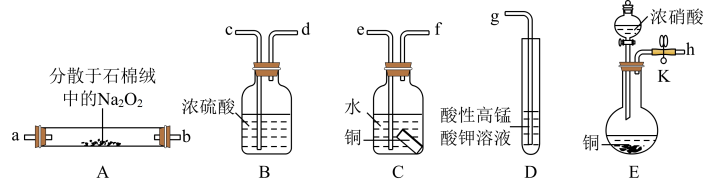
【推荐3】亚硝酸钠(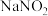 )外观酷似食盐且有咸味,是一种常用的防腐剂。某化学兴趣小组设计如图所示装置(省略夹持装置)制备
)外观酷似食盐且有咸味,是一种常用的防腐剂。某化学兴趣小组设计如图所示装置(省略夹持装置)制备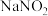 并探究其性质。
并探究其性质。
已知: ① ;
;
②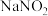 易被空气氧化,
易被空气氧化, 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为 ;
;
③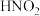 为弱酸, 室温下存在反应
为弱酸, 室温下存在反应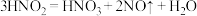 。
。
回答下列问题:
(1)装置。E中盛放铜片的仪器名称是___________ , 其中发生反应的化学方程式为___________ ,检查E装置气密性的方法是___________ 。
(2)上述实验装置中, 依次连接的合理顺序为
___________ 。
(3)装置D中酸性 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
(4)反应结束后,取适量产品溶于稀硫酸中,观察到的实验现象为___________ 。
(5)测定深水井中亚硝酸钠含量:取 水样于锥形瓶中,立即加入
水样于锥形瓶中,立即加入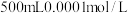 酸性高锰酸钾溶液,充分反应后用
酸性高锰酸钾溶液,充分反应后用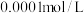 草酸溶液滴定高锰酸钾,终点时消耗草酸溶液
草酸溶液滴定高锰酸钾,终点时消耗草酸溶液 。到达滴定终点的现象
。到达滴定终点的现象___________ 。若所取样品在空气中放置时间过长,则测定结果___________ (填“偏高”“偏低”或“无影响”)。
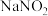 )外观酷似食盐且有咸味,是一种常用的防腐剂。某化学兴趣小组设计如图所示装置(省略夹持装置)制备
)外观酷似食盐且有咸味,是一种常用的防腐剂。某化学兴趣小组设计如图所示装置(省略夹持装置)制备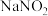 并探究其性质。
并探究其性质。
已知: ①
 ;
;②
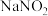 易被空气氧化,
易被空气氧化, 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为 ;
;③
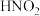 为弱酸, 室温下存在反应
为弱酸, 室温下存在反应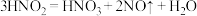 。
。回答下列问题:
(1)装置。E中盛放铜片的仪器名称是
(2)上述实验装置中, 依次连接的合理顺序为

(3)装置D中酸性
 溶液的作用是
溶液的作用是(4)反应结束后,取适量产品溶于稀硫酸中,观察到的实验现象为
(5)测定深水井中亚硝酸钠含量:取
 水样于锥形瓶中,立即加入
水样于锥形瓶中,立即加入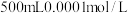 酸性高锰酸钾溶液,充分反应后用
酸性高锰酸钾溶液,充分反应后用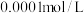 草酸溶液滴定高锰酸钾,终点时消耗草酸溶液
草酸溶液滴定高锰酸钾,终点时消耗草酸溶液 。到达滴定终点的现象
。到达滴定终点的现象
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】用 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含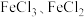 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:

回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为_______ ,过氧化氢和盐酸的混合溶液也可以刻蚀铜电路板,反应的化学方程式为_______ 。
(2)检验刻蚀后液体中 通常选用的试剂为
通常选用的试剂为_______ ,滤渣B的主要成分为_______ 。
(3)检验滤渣B中提取出的 已经洗净的操作为
已经洗净的操作为_______ 。
(4)从滤液A中提取 的操作:加入
的操作:加入 粉后,先浓缩滤液至出现
粉后,先浓缩滤液至出现_______ ,趁热过滤,取溶液_______ 、过滤、洗涤、干燥。
 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含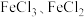 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为
(2)检验刻蚀后液体中
 通常选用的试剂为
通常选用的试剂为(3)检验滤渣B中提取出的
 已经洗净的操作为
已经洗净的操作为(4)从滤液A中提取
 的操作:加入
的操作:加入 粉后,先浓缩滤液至出现
粉后,先浓缩滤液至出现
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组以废铁屑(含有碳、Fe2O3杂质)为原料制备 晶体。具体的流程如下:
晶体。具体的流程如下:
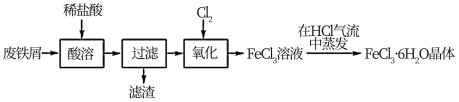
试回答下列问题:
(1)请写出“酸溶”时发生反应的离子方程式: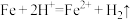 、
、 _______ 。
(2)过滤时,需要用到的玻璃仪器有_______ 。
(3)“氧化”过程中发生反应的化学方程式为_______ ,该反应中氧化剂是_______ 。
(4)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是_______ 。
(5)“氧化”过程结束后,如何证明溶液中有Fe3+存在?请写出实验方案:________ 。
 晶体。具体的流程如下:
晶体。具体的流程如下:
试回答下列问题:
(1)请写出“酸溶”时发生反应的离子方程式:
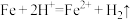 、
、 (2)过滤时,需要用到的玻璃仪器有
(3)“氧化”过程中发生反应的化学方程式为
(4)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是
(5)“氧化”过程结束后,如何证明溶液中有Fe3+存在?请写出实验方案:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A一J是中学化学中常见的物质,其相互转化关系如下图所示,反应条件均已略去。A、B常温下均为无色液体,且均由两种相同的元素组成;C、F、G均为非金属单质,常温下C、F为无色气体,G可用于制取“84”消毒液;D是应用最广泛的金属;J溶液中滴入KSCN 溶液显红色。

回答下列问题:
(1)A的化学式是_________ 。
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是______ 。
(3)B和G能发生反应,写出反应的离子方程式______ 。
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:______ 。

回答下列问题:
(1)A的化学式是
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是
(3)B和G能发生反应,写出反应的离子方程式
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.某同学设计如下实验方案,以分离NaCl和BaCl2两种固体混合物,回答下列问题:
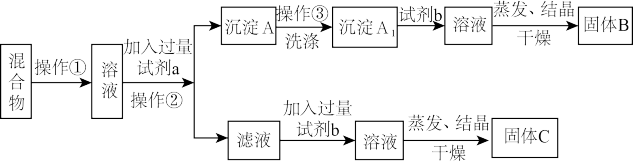
(1)操作①的名称是_____________ ;
(2)试剂a是______ (填化学式,下同),试剂b是______ ,固体B是______ 。
Ⅱ.工业上用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
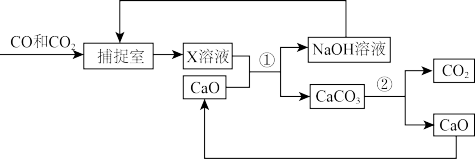
(3)反应②分离出的CO2可制成干冰,干冰常用于____________ ;
(4)“捕捉室"中发生反应的化学方程式为_____________ ;
(5)反应①在“反应分离室"内进行,将NaOH溶液和CaCO3分离的操作是__________ ;
(6)下列有关该捕捉过程的叙述正确的有___________ 。
A.捕捉到的CO2可用于制备其他化工产品,减少了温室气体的排放
B.“反应分离室”中的反应要吸收大量热
C.整个过程中只有一种物质可循环利用
D.能耗大是该捕捉技术的一大缺点

(1)操作①的名称是
(2)试剂a是
Ⅱ.工业上用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):

(3)反应②分离出的CO2可制成干冰,干冰常用于
(4)“捕捉室"中发生反应的化学方程式为
(5)反应①在“反应分离室"内进行,将NaOH溶液和CaCO3分离的操作是
(6)下列有关该捕捉过程的叙述正确的有
A.捕捉到的CO2可用于制备其他化工产品,减少了温室气体的排放
B.“反应分离室”中的反应要吸收大量热
C.整个过程中只有一种物质可循环利用
D.能耗大是该捕捉技术的一大缺点
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】从海带中提取碘,有以下甲、乙两种实验方案如下:
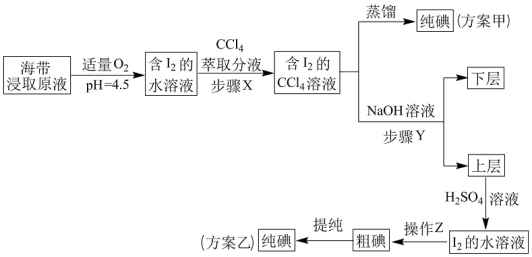
已知:3I2 + 6NaOH = 5NaI + NaIO3 + 3H2O。请回答:
(1)步骤X为萃取分液,分液时需要用到分液漏斗,分液漏斗在使用前需要___________ 。
(2)方案甲进行蒸馏操作时,通常需要水浴加热,其优点是___________ 。
(3)方案乙在上层溶液中加入硫酸得到I2的水溶液,发生反应的离子方程式___________ 。
(4)操作Z的名称是___________ 。

已知:3I2 + 6NaOH = 5NaI + NaIO3 + 3H2O。请回答:
(1)步骤X为萃取分液,分液时需要用到分液漏斗,分液漏斗在使用前需要
(2)方案甲进行蒸馏操作时,通常需要水浴加热,其优点是
(3)方案乙在上层溶液中加入硫酸得到I2的水溶液,发生反应的离子方程式
(4)操作Z的名称是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】过氧化钙是具有较强的漂白、杀菌、消毒作用,难溶于水的固体。对环境无危害而具有很高的应用价值。一种生产过氧化钙的工艺流程如图所示:
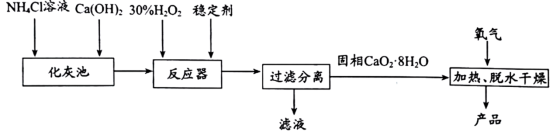
已知:CaO2在274℃开始分解,350℃迅速分解生成CaO和O2;H2O2具有弱酸性。回答下列问题:
(1)在化灰池中应控制Ca(OH)2的加入速度防止气体生成,化灰池中发生反应的化学方程式为_______ 。
(2)反应器中发生反应的化学方程式为____________ 。
(3)实验室中进行过滤操作时用到的玻璃仪器有___________ 。
(4)该生产工艺中可循环使用的物质是_______ (填化学式)。
(5)常采用Ca(OH)2过量而不是H2O2过量的方式来生产的原因是________ 。
(6)加热、脱水干燥过程中要控制加热温度并通入氧气,通入氧气的目的是______ 。(从化学平衡移动角度回答)

已知:CaO2在274℃开始分解,350℃迅速分解生成CaO和O2;H2O2具有弱酸性。回答下列问题:
(1)在化灰池中应控制Ca(OH)2的加入速度防止气体生成,化灰池中发生反应的化学方程式为
(2)反应器中发生反应的化学方程式为
(3)实验室中进行过滤操作时用到的玻璃仪器有
(4)该生产工艺中可循环使用的物质是
(5)常采用Ca(OH)2过量而不是H2O2过量的方式来生产的原因是
(6)加热、脱水干燥过程中要控制加热温度并通入氧气,通入氧气的目的是
您最近一年使用:0次



