W、X、Y、Z、R是原子序数依次递增的五种短周期元素,Y原子核外电子数与W、X的最外层电子数之和相等,Y原子半径是短周期元素原子半径中最大的,R最高正价与最低负价代数和为4,W的一种氢化物常作制冷剂,Z原子的电子层数与最外层电子数相等。回答下列问题:
(1)W元素的名称为___________ ,R元素在周期表中位于第三周期___________ 族。
(2)X、Z、R所形成的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)R的简单氢化物的电子式为___________ ;W、X的最简单氢化物稳定性关系:___________ (填氢化物化学式)。
(4)Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(5) 与
与 气体发生氧化还原反应,生成X的常见单质和一种盐,写出该反应的化学方程式:
气体发生氧化还原反应,生成X的常见单质和一种盐,写出该反应的化学方程式:___________ 。
(1)W元素的名称为
(2)X、Z、R所形成的简单离子半径由大到小的顺序为
(3)R的简单氢化物的电子式为
(4)Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式为
(5)
 与
与 气体发生氧化还原反应,生成X的常见单质和一种盐,写出该反应的化学方程式:
气体发生氧化还原反应,生成X的常见单质和一种盐,写出该反应的化学方程式:
更新时间:2022-01-23 18:39:08
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钴酸锂一般用作锂离子电池的正极材料,需求量大,而我国极度缺乏钴资源,主要依赖进口,因而从废旧电池中进行回收具有重要意义。以废旧钴酸锂电池材料(主要成分为LiCoO2,含单质Cu及为改善电池性能添加的单质Al等)回收钴酸锂的--种工艺流程如下:

回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理,粉碎的目的是_____ 。
(2)“碱浸”所得滤液中主要溶质的化学式为__________ 、NaOH。
(3)H2O2的电子式为________ 。“酸浸”时H2O2作还原剂,还原产物为Co2+,反应的离子方程式为_________ ;上述反应的氧化产物又将铜氧化而溶解浸出,该反应的化学方程式为____________ 。
(4)“萃取铜”中的有机萃取剂用HR表示,发生萃取的反应可表示为Cu2+ +2HR CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为
CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为___________ (溶液体积变化忽略,保留小数点后两位);为回收铜,可用一定浓度的H2SO4将有机相中的铜反萃取到水相,其原理是______________________
(5)“碱浸”时少量未浸出的残余铝可在“酸浸”时浸出,萃取铜后的溶液需调pH至5.0以上将铝离子沉淀除去。若c(Co2+ ) =0.16mol·L-1,为避免析出Co(OH)2沉淀,则调pH不能超过___________ 。(已知K[Co(OH)2]=1.6×10-15)
(6)“钴、锂共沉淀”时析出CoCO3和li2CO3,经过滤、无水乙醇洗涤、80°C干燥后在750°C煅烧,反应的化学方程式为_________________ 。

回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理,粉碎的目的是
(2)“碱浸”所得滤液中主要溶质的化学式为
(3)H2O2的电子式为
(4)“萃取铜”中的有机萃取剂用HR表示,发生萃取的反应可表示为Cu2+ +2HR
 CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为
CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为(5)“碱浸”时少量未浸出的残余铝可在“酸浸”时浸出,萃取铜后的溶液需调pH至5.0以上将铝离子沉淀除去。若c(Co2+ ) =0.16mol·L-1,为避免析出Co(OH)2沉淀,则调pH不能超过
(6)“钴、锂共沉淀”时析出CoCO3和li2CO3,经过滤、无水乙醇洗涤、80°C干燥后在750°C煅烧,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA的单质跟足量盐酸反应,可置换出标准状况下22.4L的H2,这时A转变为与氖原子具有相同电子层结构的离子。请回答:
(1)用电子式表示A和C组成的化合物的形成过程为__________________ ;
(2)B离子的电子式是___________ ,与B的离子具有相同电子数的分子中,有一种分子可与盐酸化合生成盐,该分子的电子式是_________ ;
(3)周期表中与C上下相邻的同族元素形成的气态氢化物中,沸点最高的是_______ ,(填氢化物化学式),原因是______________________ ;
(4)写出B最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式(本题涉及的含C元素的物质均易溶于水):_________________________ 。
(1)用电子式表示A和C组成的化合物的形成过程为
(2)B离子的电子式是
(3)周期表中与C上下相邻的同族元素形成的气态氢化物中,沸点最高的是
(4)写出B最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式(本题涉及的含C元素的物质均易溶于水):
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】汽车是现代社会重要的交通工具之一,化学物质在汽车的动力、安全等方面有着极为重要的作用。
Ⅰ.氨气是制备NaN3(叠氮化钠)的原料之一,汽车安全气囊中的填充物有NaN3、SiO2、KNO3等物质,NaN3遇撞击时能生成金属钠和N2。
(1)上述列举的三种汽车安全气囊填充物中属于共价化合物的是___________ (填化学式),所涉及的5种元素中,非金属元素的原子半径由大到小的顺序为___________ 。
(2)请列举一个事实说明N元素与O元素的非金属性强弱___________ 。
(3)下列有关化学用语表示正确的是___________。
(4) 的空间构型为___________。
的空间构型为___________。
Ⅱ.NaN3是由一种单原子离子和多原子离子以1:1的比例构成的化合物。
(5)叠氮化钠固体中所含化学键的类型为___________ ,叠氮化钠的晶体类型为___________ 。
(6)写出叠氮化钠分解的化学方程式___________ 。
(7)工业通过反应一:
反应二:
制备NaN3,下列有关说法中正确的是___________(双选)。
Ⅰ.氨气是制备NaN3(叠氮化钠)的原料之一,汽车安全气囊中的填充物有NaN3、SiO2、KNO3等物质,NaN3遇撞击时能生成金属钠和N2。
(1)上述列举的三种汽车安全气囊填充物中属于共价化合物的是
(2)请列举一个事实说明N元素与O元素的非金属性强弱
(3)下列有关化学用语表示正确的是___________。
A.Ne和N3-的结构示意图均为 | B.二氧化硅的分子式:SiO2 |
C.氨气的空间填充模型: | D.NH4Br的电子式: |
 的空间构型为___________。
的空间构型为___________。| A.平面三角形 | B.三角锥形 | C.四面体形 | D.直线形 |
Ⅱ.NaN3是由一种单原子离子和多原子离子以1:1的比例构成的化合物。
(5)叠氮化钠固体中所含化学键的类型为
(6)写出叠氮化钠分解的化学方程式
(7)工业通过反应一:

反应二:

制备NaN3,下列有关说法中正确的是___________(双选)。
| A.反应一每生成5.6L氢气(已换算至标准状况下的体积),转移电子数目为NA |
| B.反应一中NaNH2为强电解质,NH3为弱电解质 |
| C.反应二中生成的氨气可以循环利用 |
| D.与NaN3同为碱金属叠氮化物的LiN3受撞击分解产生Li3N和氮气,反应过程中发生了离子键和共价键的破坏与形成 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有部分元素的原子结构特点如下表所示:
(1)画出G原子结构示意图:____________________ 。
(2)元素X与元素Z相比,非金属性较强的是_________________ (填元素名称),写出一个能表示X、Z非金属性强弱关系的化学方程式:_________ 。
(3)X、Y、Z、G四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为___ 。
(4)元素X和元素Y以原子个数比为1∶1形成的化合物Q,元素G和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式:________ 。
X | L层电子数是K层电子数的3倍 |
Y | 核外电子层数等于原子序数 |
Z | L层电子数是K层和M层电子数之和 |
G | 最外层电子数是次外层电子数的2.5倍 |
(2)元素X与元素Z相比,非金属性较强的是
(3)X、Y、Z、G四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)元素X和元素Y以原子个数比为1∶1形成的化合物Q,元素G和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合物的代数和为6;R和Q可形原子数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应.请回答下列问题:
(1)T元素在周期表中的位置是________ ;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为________ (写出其中一种物质的名称).
(2)X、Z、Q三种元素的原子半径由小到大顺序为________ (填元素符号).
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为________ .
(4)下列可以判断R和T金属性强弱的是________ (填序号).
a.单质的熔点R比T低 b.单质与酸反应时,失电子数R比T少
c.单质与水反应R比T剧烈 d.最高价氧化物的水化物的碱性R比T强
(5)某同学用Q、R两元素的单质反应生成固体物质R2Q2,R2Q2属于离子化合物,且能与化合物X2Q反应生成Q的单质.R2Q2的电子式为________ ;R2Q2与X2Q反应的化学方程式为________ 。
(1)T元素在周期表中的位置是
(2)X、Z、Q三种元素的原子半径由小到大顺序为
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为
(4)下列可以判断R和T金属性强弱的是
a.单质的熔点R比T低 b.单质与酸反应时,失电子数R比T少
c.单质与水反应R比T剧烈 d.最高价氧化物的水化物的碱性R比T强
(5)某同学用Q、R两元素的单质反应生成固体物质R2Q2,R2Q2属于离子化合物,且能与化合物X2Q反应生成Q的单质.R2Q2的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为八种短周期主族元素的部分性质(已知铍的原子半径为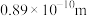 ):
):
(1)元素Z在元素周期表中的位置为_______ 。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:_______ 。
(3)R与T相比,非金属性较强的是_______ (填元素符号),下列事实能证明这一结论的是_______ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: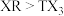
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是_______ (填元素符号),能证明这一结论的依据是_______ 。
(5)根据表中数据推测,M的原子半径的最小范围是_______ 。
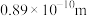 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 |  | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
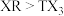
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表是指导我们系统学习化学的重要工具。下表是元素周期表的一部分:
(1)元素周期表中每种元素的具体信息如图例示。从中可以获得氟元素的有关信息有(任意写出1点)_________________________________________ 。
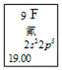
(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的______ 相同。N和P处于同一列,因为它们的________ 相同,它们都位于元素周期表的第______ 族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为___________ ,其气态氢化物的电子式为_________________ 。
②原子半径:r(P)_________ r(S)(填“>”、“<”或“=”)。
③在上表所列元素的最高价氧化物对应水化物中酸性最强的是_________ (写化学式).
| C | N | O | F |
| Si | P | S | Cl |
| Br | |||
| I |
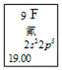
(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为
②原子半径:r(P)
③在上表所列元素的最高价氧化物对应水化物中酸性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,其中A、B、D、E、G、J为短周期元素,G元素的核电荷数为B元素的2倍。请回答下列问题:
(1)J的最高价氧化物对应水化物的化学式是___________________ 。
(2)G2J2常用作橡胶的低温硫化剂和黏结剂,其电子式为_______________________ 。写出一个能表示元素G、J非金属性强弱关系的化学方程式____________________________ 。
(3)G单质在空气中燃烧生成一种无色有刺激性气味的气体,该无色有刺激性气味的气体与含1molJ的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在—定条件下反应,可生成一种强酸和一种氧化物,且该反应中有NA个电子转移,则该反应的化学方程式是________________________ 。
(4)A的最简单氢化物是___________ (填“极性”或“非极性”)分子,实验室制备该物质的化学方程式为__________________________________________ 。
(5)根据元素周期律,可以推测上表中长周期元素的单质具有半导体特性的是__________ (填元素符号)。
| A | B | ||
| D | E | G | J |
| L | M | Q |
(2)G2J2常用作橡胶的低温硫化剂和黏结剂,其电子式为
(3)G单质在空气中燃烧生成一种无色有刺激性气味的气体,该无色有刺激性气味的气体与含1molJ的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在—定条件下反应,可生成一种强酸和一种氧化物,且该反应中有NA个电子转移,则该反应的化学方程式是
(4)A的最简单氢化物是
(5)根据元素周期律,可以推测上表中长周期元素的单质具有半导体特性的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,请回答有关问题:

(1)⑤的元素符号是______ ;
(2)②的离子结构示意图__________________ ;
(3)表中最活泼的金属是______ (填写元素符号);
(4)表中元素②③④的原子半径由大到小排列____________ (用元素符号表示);
(5)表中能形成两性氢氧化物的元素是______ ,分别写出该元素的氢氧化物与⑨最高价氧化物对应水化物反应的离子方程式: __________________________________ ;
(6)比较⑦、⑩单质氧化性的强弱:___________ (用化学式表示),请设计一个实验证明你的结论__________________________________ 。

(1)⑤的元素符号是
(2)②的离子结构示意图
(3)表中最活泼的金属是
(4)表中元素②③④的原子半径由大到小排列
(5)表中能形成两性氢氧化物的元素是
(6)比较⑦、⑩单质氧化性的强弱:
您最近一年使用:0次



