下列说法正确的是
| A.测定中和反应反应热的实验中,可用铜丝代替玻璃搅拌器 |
| B.需要加热才能发生的反应是吸热反应 |
| C.升高温度,反应速率加快,主要原因是活化分子的百分数增加 |
| D.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
更新时间:2022-01-23 21:22:37
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】从图所示的某气体反应的能量变化分析,以下判断错误的是


| A.这是一个放热反应 |
| B.该反应可能需要加热 |
| C.生成物从气态变成液态时会放出热量 |
| D.生成物具有的总能量高于反应物具有的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】反应 的能量变化与反应进程关系如图所示,下列说法正确的是
的能量变化与反应进程关系如图所示,下列说法正确的是

 的能量变化与反应进程关系如图所示,下列说法正确的是
的能量变化与反应进程关系如图所示,下列说法正确的是
| A.图中实线表示加入了催化剂 |
B.该反应的焓变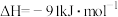 |
| C.图中虚线表示的反应I、反应II均为吸热反应 |
| D.加入催化剂,速率加快是因为改变了反应的焓变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在中和热的测定实验中,下列操作正确的是( )
| A.量取0.50mol/L的盐酸0.50mol/L的NaOH溶液各50mL |
| B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中 |
| C.环形搅拌棒上下移动,使酸碱溶液混合 |
| D.用温度计测定NaOH溶液起始温度后直接测定H 2SO 4 溶液的温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】甲~丁图为中学化学常用仪器的全部或局部,下列说法正确的是
 |  |  |  |
| 甲 | 乙 | 丙 | 丁 |
| A.甲图所示仪器使用前需检查是否漏水 |
| B.乙图所示仪器用于蒸馏时,冷却水应从下口通入 |
| C.丙图所示仪器用于观察氯化钠的焰色试验 |
| D.丁图所示仪器可用于中和热测定实验 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列热化学方程式中,正确的是
A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) H= -890.3 kJ·mol-1 H= -890.3 kJ·mol-1 |
B.500℃、30MPa下,将0.5 mo lN2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g)放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) 2NH3(g)  H= -38.6 kJ·mol-1 H= -38.6 kJ·mol-1 |
C.HCl和NaOH反应的中和热 H= -57.3 kJ·mol-1,则H2SO4(aq)+Ba(OH)2(aq)=BaSO4(S)+2H2O(g) H= -57.3 kJ·mol-1,则H2SO4(aq)+Ba(OH)2(aq)=BaSO4(S)+2H2O(g) H>2×(-57.3) kJ·mol-1 H>2×(-57.3) kJ·mol-1 |
D.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)的 H= +566.0 kJ/mol H= +566.0 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】天然气属于洁净能源,主要成分是甲烷,下列能正确表示甲烷燃烧热的热化学方程式是
A.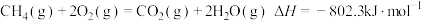 |
B.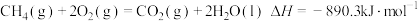 |
C.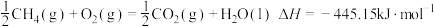 |
D.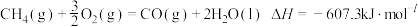 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】有关热化学方程式书写与对应表述均正确的是
| A.已知2C(s)+O2(g)=2CO(g) △H=-221 kJ·mol-1, 则可知C的燃烧热为110.5 kJ·mol-1 |
| B.在101KPa下氢气的燃烧热△H =-285.5 kJ·mol-1, 则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) △H = +285.5 kJ·mol-1 |
| C.已知C(石墨, s)=C(金刚石, s); ΔH>0 则石墨比金刚石稳定 |
| D.1mol氢气完全燃烧生成液态水放热为285.8kJ,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(g) △ H=-285.8 kJ· mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对下列图示描述错误的是:
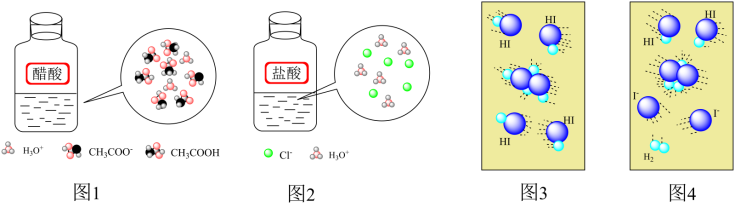

A.图1为 在水中电离示意图 在水中电离示意图 |
| B.图2为HCl在水中电离示意图 |
| C.图3为HI分解反应中分子碰撞时能量不足示意图 |
| D.图4为HI分解反应中分子发生有效碰撞时示意图 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】“活化分子”是衡量化学反应速率快慢的重要依据,下列说法中不正确的是( )
| A.活化分子之间的碰撞一定是有效碰撞 |
| B.增大反应物的浓度,可使单位体积内的活化分子增多,反应速率加快 |
| C.对于有气体参加的反应,通过压缩容器增大压强,可使单位体积内的活化分子增多,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内的活化分子百分数增加 |
您最近一年使用:0次

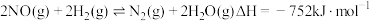 的反应机理如下:
的反应机理如下: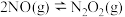 (快)
(快) (慢)
(慢) 快)
快)

