相关规律
(1)ΔH____ 0,ΔS____ 0的反应,任何温度下都能自发进行。
(2)ΔH____ 0,ΔS____ 0的反应任何温度下都不能自发进行。
(3)ΔH和ΔS的作用相反,且相差不大时,____ 对反应的方向起决定性作用。
①当ΔH<0,ΔS<0时,____ 下反应能自发进行。
②当ΔH>0,ΔS>0时,____ 下反应能自发进行。
(4)当反应的焓变和熵变的影响相反时,且大小相差悬殊时,某一因素可能占主导地位。
①常温下的放热反应,____ 对反应方向起决定性作用。
②常温下的吸热反应,____ 对反应方向起决定性作用。
(1)ΔH
(2)ΔH
(3)ΔH和ΔS的作用相反,且相差不大时,
①当ΔH<0,ΔS<0时,
②当ΔH>0,ΔS>0时,
(4)当反应的焓变和熵变的影响相反时,且大小相差悬殊时,某一因素可能占主导地位。
①常温下的放热反应,
②常温下的吸热反应,
21-22高二·全国·课前预习 查看更多[2]
更新时间:2022-02-12 08:57:22
|
【知识点】 化学反应进行方向的判据
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】CH4和H2O(g)在催化剂表面发生反应CH4(g)+H2O(g)  CO(g)+3H2(g),该反应仅在高温下能自发进行。
CO(g)+3H2(g),该反应仅在高温下能自发进行。
(1)该反应的 ΔH____ 0(填“<” “>” 或 “=”)。
(2)T ℃时,向2L密闭容器中投入2mol CH4和1.5mol H2O(g),发生上述反应,平衡时CH4的转化率为50%,该温度下反应的平衡常数K=_____ 。
(3) T ℃时,向1 L密闭容器中投入2 mol CH4、1 mol H2O(g)、3 mol CO、2 mol H2,则反应的v(正)___ v(逆) (选填“<” “>”或“=”)
(4)现向三个体积均为2L的恒容密闭容器I、Ⅱ、Ⅲ中,均分别充入1molCO 和2molH2发生反应:CO(g)+2H2(g) CH3OH(g) ΔH1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
CH3OH(g) ΔH1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
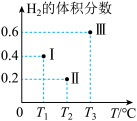
①5min时三个容器中的反应达到化学平衡状态的是容器_______ (填序号)。
②0-5 min内容器I中用CH3OH表示的化学反应速率v(CH3OH)=_______ 。(保留两位有效数字)
③当三个容器中的反应均达到平衡状态时,CO转化率最高的是容器______ 。
 CO(g)+3H2(g),该反应仅在高温下能自发进行。
CO(g)+3H2(g),该反应仅在高温下能自发进行。(1)该反应的 ΔH
(2)T ℃时,向2L密闭容器中投入2mol CH4和1.5mol H2O(g),发生上述反应,平衡时CH4的转化率为50%,该温度下反应的平衡常数K=
(3) T ℃时,向1 L密闭容器中投入2 mol CH4、1 mol H2O(g)、3 mol CO、2 mol H2,则反应的v(正)
(4)现向三个体积均为2L的恒容密闭容器I、Ⅱ、Ⅲ中,均分别充入1molCO 和2molH2发生反应:CO(g)+2H2(g)
 CH3OH(g) ΔH1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
CH3OH(g) ΔH1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
①5min时三个容器中的反应达到化学平衡状态的是容器
②0-5 min内容器I中用CH3OH表示的化学反应速率v(CH3OH)=
③当三个容器中的反应均达到平衡状态时,CO转化率最高的是容器
您最近一年使用:0次
填空题
|
适中
(0.65)
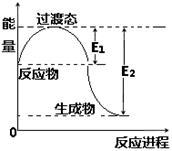
【推荐2】Ⅰ.(1)下图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134KJ/mol,E2=368KJ/mol( E1、 E2为反应的活化能)。若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是 、 (填“增大”、“减小”或“不变”)。写出该 反应的热化学方程式 。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可
Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
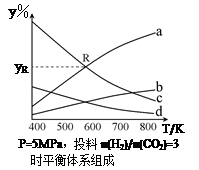
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大 B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变 D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可


Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大 B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变 D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)化学反应 2NO(g)+2CO(g)=N2(g)+2CO2(g)在 298 K、100 kPa 下:ΔH=-113.0 kJ/mol,ΔS=-0.1kJ/(mol·K),反应在常温下________ (填“能”或“不能”)自发进行。
(2)在密闭容器中,控制不同温度进行 2SO3(g) 2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
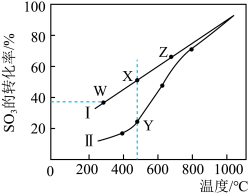
①比较图中X 点与 Y 点、X 点与 Z 点的平衡常数大小:K(X)______ K(Y),K(X)_______ K(Z)(填“>”“<”或“=”)。
②Y 点的反应速率:υ正____ υ逆(填“>”“<”或“=”)。
③随温度升高,曲线Ⅱ逼近曲线Ⅰ的原因是_______ 。
④下列措施在其他条件不变时,能提高 SO3转化率的是____ 。
A.使用合适的催化剂 B.升高温度 C.增大压强 D.降低温度 E.减小压强 F.SO3的起始浓度增加至 2c mol/L
(2)在密闭容器中,控制不同温度进行 2SO3(g)
 2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
①比较图中X 点与 Y 点、X 点与 Z 点的平衡常数大小:K(X)
②Y 点的反应速率:υ正
③随温度升高,曲线Ⅱ逼近曲线Ⅰ的原因是
④下列措施在其他条件不变时,能提高 SO3转化率的是
A.使用合适的催化剂 B.升高温度 C.增大压强 D.降低温度 E.减小压强 F.SO3的起始浓度增加至 2c mol/L
您最近一年使用:0次



