表中列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素⑧在周期表中所处位置____ ,元素④的名称是____ ,从元素原子得失电子的角度看,元素④的单质应具有____ 性(填“氧化’或“还原”)。
(2)⑥、④、⑦的氢化物稳定性由强到弱的顺序是____ (用化学式表示)。
(3)元素⑦的原子结构示意图是____ 。元素①与元素④以相等的原子个数形成化合物的电子式是____ 。
(4)写出元素⑤的单质在氧气中燃烧的化学方程式____ ,这一反应的现象是____ 。
IA | ||||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ④ | ⑧ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑨ |
(1)元素⑧在周期表中所处位置
(2)⑥、④、⑦的氢化物稳定性由强到弱的顺序是
(3)元素⑦的原子结构示意图是
(4)写出元素⑤的单质在氧气中燃烧的化学方程式
更新时间:2022-02-25 17:34:39
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A,B,C,D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型:C,D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号)
(2)单质A有两种同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为_______ ,中心原子的杂化轨道类型为_______ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_______ ;晶胞中A原子的配位数为_______ ;列式计算晶体F的密度(g·cm-3)_______ 。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分,填写下列空格:
(1)比较④⑤⑧的原子半径由大到小依次___________ 。(填元素符号,下同)
(2)元素②与④形成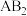 型化合物的电子式为
型化合物的电子式为___________ ,属于___________ 晶体。
(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:___________ ,所得产物中含有的化学键类型有___________ 。
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是___________ 。(填化学式)
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
(2)元素②与④形成
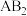 型化合物的电子式为
型化合物的电子式为(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期律和周期表有力地论证了事物变化中量变引起质变的规律性,以及结构决定性质的化学观念.随着原子序数的递增,七种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示,请回答下列问题:________ 周期第_______ 族.
(2)D、E、F三种元素对应的简单离子半径由大到小的顺序为________ (用元素的离子符号表示).
(3)用电子式表示G的氢化物的形成过程_______________________ .
(4)元素A与C形成的电子总数为22的分子的结构式为_____________ .
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为___________ .
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为___________ .
(7)下列有关物质性质的推断,正确的是__________ (填标号).
a.单质的氧化性: b.金属性:
b.金属性:
c.气态氢化物的稳定性: d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:

(2)D、E、F三种元素对应的简单离子半径由大到小的顺序为
(3)用电子式表示G的氢化物的形成过程
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为
(7)下列有关物质性质的推断,正确的是
a.单质的氧化性:
 b.金属性:
b.金属性:
c.气态氢化物的稳定性:
 d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分。

(1)请用实线在图中画出金属与非金属的分界线
(2)阴影部分中P 元素在元素周期表中的位置为________ ;H2SO4、H3AsO4、H3PO4酸性由强到弱的顺序是____________ ;
(3)卤族元素对应的氢化物沸点递变规律正确的是_______ ;
A.HF<HCl<HBr<HI B.HCl<HBr<HI<HF
(4)氢化物的稳定性H2Se_____ H2S (填“<”、“>”或“=”)。
(5)稼(Ga)和同族的铝具有相似的化学性质,请写出稼与沸水反应的化学方程式____________ 。

(1)请用实线在图中画出金属与非金属的分界线
(2)阴影部分中P 元素在元素周期表中的位置为
(3)卤族元素对应的氢化物沸点递变规律正确的是
A.HF<HCl<HBr<HI B.HCl<HBr<HI<HF
(4)氢化物的稳定性H2Se
(5)稼(Ga)和同族的铝具有相似的化学性质,请写出稼与沸水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】甲图是部分短周期元素的常见化合价与原子序数的关系图:

请回答下列问题:
(1)D元素在周期表中的位置为___________ ,D和G的简单氢化物中沸点高的是___________ (写化学式),A和E形成的化合物的电子式为_____________ 。
(2)D、E、G、H的简单离子半径由大到小的顺序为__________________________ 。(用化学式表示)
(3)二元化合物X是含有C元素的18电子分子,1molX(l)在25℃ 101kPa下完全燃烧放出622kJ的热量,写出表示X燃烧热的热化学方程式________________________________ 。
(4)H的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式___________________________________ 。
(5)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。
①溶液a和b分别为________ ,________ (填化学式)。
②溶液c中的离子方程式为__________________________________________ 。
③请从原子结构的角度解释非金属性C>B的原因____________________________________________________ 。

请回答下列问题:
(1)D元素在周期表中的位置为
(2)D、E、G、H的简单离子半径由大到小的顺序为
(3)二元化合物X是含有C元素的18电子分子,1molX(l)在25℃ 101kPa下完全燃烧放出622kJ的热量,写出表示X燃烧热的热化学方程式
(4)H的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式
(5)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。
①溶液a和b分别为
②溶液c中的离子方程式为
③请从原子结构的角度解释非金属性C>B的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】根据要求完成下列各小题实验目的。a、b为弹簧夹,(加热及固定装置已略去)
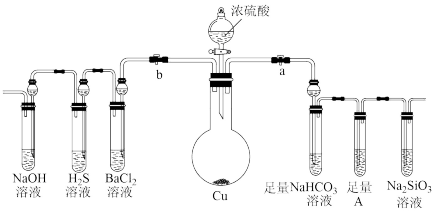
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、_______ 、加药品后,打开a关闭b,打开分液漏斗旋转活塞,然后滴入浓硫酸,发现硫酸滴入几滴,就不再滴下,原因是_______ ,当顺利滴入时加热。
②铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂可以是_______ 。(用a,b,c填空)
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
③能说明碳的非金属性比硅强的实验现象是_______ 。
(2)验证 的氧化性、还原性和酸性氧化物的通性。
的氧化性、还原性和酸性氧化物的通性。
①在(1)操作后打开b,关闭a。
②一段时间后, 溶液中的现象是
溶液中的现象是_______ ,化学方程式是_______ 。
(3) 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、
②铜与浓硫酸反应的化学方程式是
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
③能说明碳的非金属性比硅强的实验现象是
(2)验证
 的氧化性、还原性和酸性氧化物的通性。
的氧化性、还原性和酸性氧化物的通性。①在(1)操作后打开b,关闭a。
②一段时间后,
 溶液中的现象是
溶液中的现象是(3)
 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有X、Y、 Z、M、R、Q六种短周期主族元素,部分信息如下表所示:
请回答下列问题:
(1)R在元素周期表中的位置是________ 。
(2)根据表中数据推测,Y的原子半径的最小范围是________ 。
(3) Z、M、Q的简单离子的离子半径由大到小的顺序为_______ (用元素符号表示)。
(4)Y与R相比,非金属性较强的是______ (用元素符号表示),下列事实能证明这一结论的是_____ (选填字母序号)
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:XR>YX4
c.Y与R形成的化合物中Y呈正价
(5)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式:__________ 。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | |||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
请回答下列问题:
(1)R在元素周期表中的位置是
(2)根据表中数据推测,Y的原子半径的最小范围是
(3) Z、M、Q的简单离子的离子半径由大到小的顺序为
(4)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:XR>YX4
c.Y与R形成的化合物中Y呈正价
(5)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
(1)元素①在周期表中的位置为__ 。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为__ (填化学式)。
(3)元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是__ (填化学式)。
(4)元素②、⑤形成化合物的电子式为__ 。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的化学反应方程式为__ 。
(6)原子序数比④小1的元素X是___ ,X的晶体类型是___ ,举例说明它的一个用途___ 。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为
(3)元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是
(4)元素②、⑤形成化合物的电子式为
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的化学反应方程式为
(6)原子序数比④小1的元素X是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】随原子序数递增,八种短周期元素(分别用字母x、y、z、d、e、f、g、h表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
回答下列问题:
(1)元素z在周期表中的位置是_______ 。h的离子结构示意图_______ 。元素d、e、f、g原子的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)下列各项比较,正确的是(填序号)_______ 。
①氢化物的沸点:g<d ②最高价氧化物对应的水化物碱性:e<f
③气态氢化物稳定性:g比h稳定 ④阳离子的氧化性:e<f
(3)用电子式表示e的单质与g的单质形成化合物的过程_______
(4)元素h单质的氧化性强于元素g单质的氧化性的事实是_______ (用离子方程式表示)。
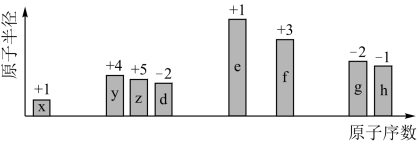
回答下列问题:
(1)元素z在周期表中的位置是
(2)下列各项比较,正确的是(填序号)
①氢化物的沸点:g<d ②最高价氧化物对应的水化物碱性:e<f
③气态氢化物稳定性:g比h稳定 ④阳离子的氧化性:e<f
(3)用电子式表示e的单质与g的单质形成化合物的过程
(4)元素h单质的氧化性强于元素g单质的氧化性的事实是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F六种元素,原子序数依次增大,A是周期表中原子半径最小的元素,B原子的最外层上有4个电子;D的阴离子和E的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体,F的L层电子数等于K、M两个电子层上的电子数之和。(用元素符号或化学式 填空回答以下问题)
(1)B为________ ,D为________ ,E为________ 。
(2)C元素在周期表中的位置________ 。
(3)B、D两元素形成化合物属(“离子”或“共价”)化合物________ 。
(4)F原子结构示意图为________ 。
(5)写出BD2和E2D2的电子式:_______ ;_______ 。
(6)B、C、D的最简单氢化物稳定性由强到弱依次为:______ 。(填化学式)
(7)写出F元素的最高价氧化物的水化物和B反应的化学方程式:________ 。
(8)E与F两元素可形成化合物,用电子式表示其化合物的形成过程:_________ 。
(1)B为
(2)C元素在周期表中的位置
(3)B、D两元素形成化合物属(“离子”或“共价”)化合物
(4)F原子结构示意图为
(5)写出BD2和E2D2的电子式:
(6)B、C、D的最简单氢化物稳定性由强到弱依次为:
(7)写出F元素的最高价氧化物的水化物和B反应的化学方程式:
(8)E与F两元素可形成化合物,用电子式表示其化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W、R五种元素的性质或结构信息如表,根据表中的信息回答下列问题:
(1)写出元素R在元素周期表中的位置:_______ 。
(2)由X、Z、R三种元素形成的化合物XRZ的结构式为_______ ;化合物WR的电子式为_______ 。
(3)Y、Z的最简单氢化物中较稳定的是_______ (填化学式),判断依据是_______ 。由Y和Z组成且Y和Z的质量之比为7:4的化合物的分子式是_______ 。
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:_______ ,燃烧片刻后取出燃烧管,迅速将集气瓶倒扣在过量的烧碱溶液中,可能产生的现象是_______ ,所得溶液中存在的溶质除了过量的NaOH外,还含有的是_______ (填化学式)。
| 元素 | X | Y | Z | W | R |
| 性质或结构信息 | 是原子半径最小的元素 | 常见单质为空气中的主要成分之一 | 是海水中质量分数最大的元素 | 原子核内有11个质子 | 原子核外有3个电子层,常见单质为气体 |
(2)由X、Z、R三种元素形成的化合物XRZ的结构式为
(3)Y、Z的最简单氢化物中较稳定的是
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D为短周期元素,请根据下表信息回答问题。
(1)B在元素周期表的位置:_________________ 。
(2)工业上电解法冶炼单质C的化学方程式为_______________ 。
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质;D的单质与A的另一种氢化物反应生成A的单质。有关反应的化学方程式为:________ ;______ 。
(4)D的最高价氧化物为无色液体,该物质与水混合得到一种强酸溶液,该反应的化学方程式为_________________________________________ 。
| 元素 | A | B | C | D |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
(2)工业上电解法冶炼单质C的化学方程式为
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质;D的单质与A的另一种氢化物反应生成A的单质。有关反应的化学方程式为:
(4)D的最高价氧化物为无色液体,该物质与水混合得到一种强酸溶液,该反应的化学方程式为
您最近一年使用:0次



