碱式氯化镁[ ]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
(1)装 溶液的仪器名称是
溶液的仪器名称是_______ 。装置B的作用是_______ 。
(2)上述实验装置中存在的一处明显错误是_______ 。
(3)写出装置A中发生反应的离子方程式:_______ 。
(4)装置C中发生反应的化学方程式为_______ 。
(5)装置F中倒置漏斗的作用是_______ 。
(6)在空气中加热 也可制备
也可制备 ,若将
,若将 和
和 混合共热可制备无水
混合共热可制备无水 ,
, 的作用是
的作用是_______ 。
 ]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
(1)装
 溶液的仪器名称是
溶液的仪器名称是(2)上述实验装置中存在的一处明显错误是
(3)写出装置A中发生反应的离子方程式:
(4)装置C中发生反应的化学方程式为
(5)装置F中倒置漏斗的作用是
(6)在空气中加热
 也可制备
也可制备 ,若将
,若将 和
和 混合共热可制备无水
混合共热可制备无水 ,
, 的作用是
的作用是
2022·河北·模拟预测 查看更多[4]
河北省部分名校2021-2022学年高三下学期3月份联考考试化学试题 (已下线)三轮冲刺卷02-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)河南省名校联盟2021-2022学年高三下学期3月大联考理科综合化学试题2023届河南省驻马店树人高级中学高三下学期一模理科综合试卷-高中化学
更新时间:2022-03-08 20:38:41
|
相似题推荐
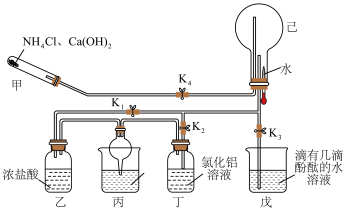
【推荐1】某化学兴趣小组在教师的指导下,利用如图所示装置(夹持和加热装置已省略)和试剂进行NH3的制备及性质探究的一体化实验。请回答下列问题:___________ ;乙处瓶内观察到的现象为___________ ;丙处烧杯中的试剂为稀硫酸,丙处球形干燥管的作用是___________ 。
(2)一段时间后关闭K1,打开K2,丁处瓶内发生反应的离子方程式为___________ ;继续反应一段时间后,关闭K2、K4,打开K3,挤压胶头滴管,己处圆底烧瓶内能观察到的现象为___________ 。
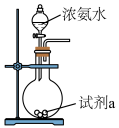
(3)甲装置可以用如图所示装置代替,试剂a可选择___________ (填试剂名称)。氨的催化氧化是工业制硝酸的基础,氨与氧气在催化剂作用下发生反应生成氮的氧化物时,氧化剂和还原剂的物质的量之比为___________ 。
(2)一段时间后关闭K1,打开K2,丁处瓶内发生反应的离子方程式为
(3)甲装置可以用如图所示装置代替,试剂a可选择
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】依据下图氮元素及其化合物的转化关系,回答问题:

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。
(2)下列试剂不能用于干燥NH3的是_______ 。
A.浓硫酸 B.碱石灰 C.NaOH固体
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①加热时NH3可催化氧化为NO,化学方程式为_______ 。
②NO→NO2反应的实验现象是_______ 。
③NO2+H2O→HNO3中氧化剂与还原剂物质的量之比为_______ 。
(4)若要将NH3→N2,从原理上看,下列试剂可行的是_______。

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
(2)下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①加热时NH3可催化氧化为NO,化学方程式为
②NO→NO2反应的实验现象是
③NO2+H2O→HNO3中氧化剂与还原剂物质的量之比为
(4)若要将NH3→N2,从原理上看,下列试剂可行的是_______。
| A.O2 | B.Na | C.NH4Cl | D.NO2 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D四种物质之间有下图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。

请回答下列问题:
(1)写出B的化学式:_______ 。
(2)在D→C的过程中,D表现出强_______ (填“氧化性”或“还原性”)。
(3)写出C→D的化学方程式:_______ ,此反应中,每生成1mol NO,转移的电子数目为_______ 。
(4)写出D和Cu反应生成C的离子方程式_______ 。
(5)写出实验室用氯化铵和熟石灰共热制备 的化学方程式
的化学方程式_______ 。

请回答下列问题:
(1)写出B的化学式:
(2)在D→C的过程中,D表现出强
(3)写出C→D的化学方程式:
(4)写出D和Cu反应生成C的离子方程式
(5)写出实验室用氯化铵和熟石灰共热制备
 的化学方程式
的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】焦亚硫酸钠(Na2S2O5)是生产、生活中重要的物质,受热易分解,实验室制备Na2S2O5的实验流程如下:
H2SO4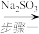 SO2
SO2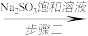 Na2S2O5溶液
Na2S2O5溶液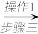 Na2S2O5晶体
Na2S2O5晶体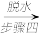 Na2S2O5
Na2S2O5
(1)步骤一中一般用70%的H2SO4,H2SO4浓度过小或过大均不利于SO2的逸出,原因是_______ 。
(2)步骤二的实验装置如图:

①三颈烧瓶中发生反应的化学方程式为_________ 。
②处理尾气,选用的最合理的装置(夹持装置已略去)为_______ (填标号)。

(3)“操作1”包括的操作有低温蒸发、结晶、____ 、洗涤。洗涤时先用饱和SO2水溶液,再用无水乙醇,用饱和SO2水溶液、无水乙醇洗涤产品的共同优点是____ ,用无水乙醇洗涤的另外一个优点是_____ 。
(4)“步骤四”脱水需在N2的气氛中低温烘干,原因是______ 。
(5)用酸性KMnO4溶液______ (填“能”或“不能”)鉴别出产品Na2S2O5中含有Na2SO4。
(6)产品纯度检验:取1.0 g Na2S2O5产品溶于水配成100 mL溶液,取上述配好的溶液25.00 mL,用0.1 mol·L-1的碘标准液滴定至终点,消耗24.00 mL碘标准液,该样品中Na2S2O5的纯度为_____ 。(其他杂质不参与反应)
H2SO4
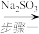 SO2
SO2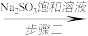 Na2S2O5溶液
Na2S2O5溶液 Na2S2O5晶体
Na2S2O5晶体 Na2S2O5
Na2S2O5(1)步骤一中一般用70%的H2SO4,H2SO4浓度过小或过大均不利于SO2的逸出,原因是
(2)步骤二的实验装置如图:

①三颈烧瓶中发生反应的化学方程式为
②处理尾气,选用的最合理的装置(夹持装置已略去)为

(3)“操作1”包括的操作有低温蒸发、结晶、
(4)“步骤四”脱水需在N2的气氛中低温烘干,原因是
(5)用酸性KMnO4溶液
(6)产品纯度检验:取1.0 g Na2S2O5产品溶于水配成100 mL溶液,取上述配好的溶液25.00 mL,用0.1 mol·L-1的碘标准液滴定至终点,消耗24.00 mL碘标准液,该样品中Na2S2O5的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】从铬锰矿渣(主要成分为Cr2O3、MnO,含少量Fe2O3、SiO2、Al2O3)中分离铬、锰的一种工艺流程如图所示。

已知:焙烧时MnO不发生反应。
回答下列问题:
(1)焙烧中,SiO2转化为Na2SiO3,Cr2O3转化为 Na2CrO4,写出Cr2O3转化为Na2CrO4的化学方程式为_______ 。
(2)加快酸浸速率的措施有_______ (任写一条)。
(3)滤渣1的成分是_______ (写化学式)。
(4)加入Na2S2O3的作用为_______
(5)Mn2+发生“转化”的离子方程式为_______ 。
(6)某温度下,Cr3+、Mn2+的沉淀率与pH关系如图所示,则“沉铬”过程最佳的pH为_______ 。 计算“沉铬”后滤液中c(Cr3+ )为_______ mol/L。[已知在该温度下,Kw=1×10-13,Ksp(Cr(OH)3)=1×10-30]


已知:焙烧时MnO不发生反应。
回答下列问题:
(1)焙烧中,SiO2转化为Na2SiO3,Cr2O3转化为 Na2CrO4,写出Cr2O3转化为Na2CrO4的化学方程式为
(2)加快酸浸速率的措施有
(3)滤渣1的成分是
(4)加入Na2S2O3的作用为
(5)Mn2+发生“转化”的离子方程式为
(6)某温度下,Cr3+、Mn2+的沉淀率与pH关系如图所示,则“沉铬”过程最佳的pH为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】化工产品中,含氯物质众多,其用途广泛。回答下列化合价问题:
(1)如图为氯及其化合物的“价-类”二维图。缺失的类别A为___________ 、物质B为___________ (填化学式)。

(2)“84”消毒液和洁厕灵不能混合使用,请用离子方程式解释:___________ 。
(3)电石渣[主要成分为 ]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取
]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取 的工艺流程如图所示:
的工艺流程如图所示:

已知: 易溶于水。
易溶于水。
①工业生产电石(CaC2)的反应为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为___________ 。
②“转化”发生反应的离子方程式为___________ 。
③上述流程中所用 是用
是用 与浓盐酸反应制得,该反应的离子方程式是
与浓盐酸反应制得,该反应的离子方程式是___________ ,其中盐酸体现的性质为___________ 。
(1)如图为氯及其化合物的“价-类”二维图。缺失的类别A为

(2)“84”消毒液和洁厕灵不能混合使用,请用离子方程式解释:
(3)电石渣[主要成分为
 ]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取
]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取 的工艺流程如图所示:
的工艺流程如图所示:
已知:
 易溶于水。
易溶于水。①工业生产电石(CaC2)的反应为
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为②“转化”发生反应的离子方程式为
③上述流程中所用
 是用
是用 与浓盐酸反应制得,该反应的离子方程式是
与浓盐酸反应制得,该反应的离子方程式是
您最近一年使用:0次



