我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生 的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
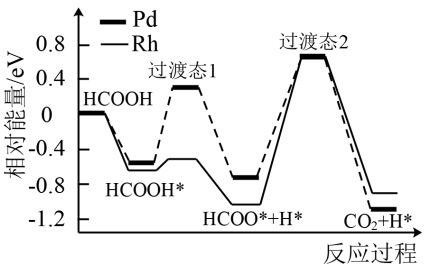
 的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
的部分反应过程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法正确的是
A.Pd、Rh作催化剂时HCOOH分解产生 的 的 相同 相同 |
B.反应 在Pd和Rh表面进行时均为放热过程 在Pd和Rh表面进行时均为放热过程 |
C.HCOOH吸附在催化剂表面的过程 |
D.反应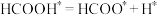 对总反应的速率影响相对较大 对总反应的速率影响相对较大 |
更新时间:2022-03-10 17:52:39
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.反应物分子之间的碰撞一定是有效碰撞 |
| B.催化剂降低反应的活化能,增大反应速率 |
| C.吸热反应一定不能自发,熵减反应一定不能自发 |
D.恒温恒容下反应 ,充入 ,充入 化学反应速率增加 化学反应速率增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】硼氢化钠(NaBH4)中的氢元素为-1价,具有很强的还原性,被称为“万能还原剂”,NaBH4在催化剂钌(Ru)表面与水反应的历程如图所示:
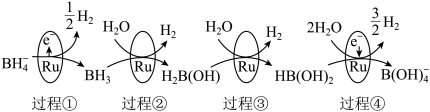
下列说法中错误的是

下列说法中错误的是
| A.过程②反应为BH3+H2O=H2↑+H2B(OH) |
| B.反应过程中硼元素的化合价发生了变化 |
| C.若过程③和过程④均产生lmol H2,则转移电子数目不相等 |
| D.Ru可使上述反应活化分子的百分数提高,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成气(CO和H2)是目前化工常用的原料,下面是用甲烷制备合成气的两种方法:①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
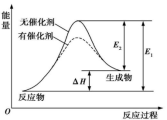
 CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
| A.E1表示2CH4(g)+O2(g)=2CO(g)+4H2(g)的活化能 |
B.E2表示CH4(g)+H2O(g) CO(g)+3H2(g)的活化能 CO(g)+3H2(g)的活化能 |
| C.该图示为反应②的反应过程与能量变化示意图 |
| D.一般情况下,加入催化剂,既能降低E1,也能降低E2,但不能改变E1与E2的差值 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】由于水氧化反应包含多个电子/质子转移,而且其动力学过程缓慢,因此,目前其仍是太阳能驱动人工光合系统的瓶颈,水氧化催化机理如图所示。下列叙述错误的是


| A.钴元素位于元素周期表的d区 |
B.该机理总反应式为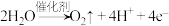 |
C.氧化性: |
| D.催化剂能降低反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列生产或实验事实引出的相应结论错误的是( )
选项 | 事实 | 结论 |
| A | 其他条件相同,Na2S、Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间短 | 当其他条件不变时,升高温度,化学反应速率加快 |
| B | H+浓度相同的盐酸和醋酸分别与相同形状等质量的锌粒反应 | 反应开始时,速率相同 |
| C | 在容积可变的密闭容器中发生反应2NH3(g) N2H4(l)+H2(g),把容器的积体缩小一半 N2H4(l)+H2(g),把容器的积体缩小一半 | 正反应速率加快,逆反应速率减慢 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2--3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知 Na2SO3和 KIO3 反应过程和机理较复杂,一般认为分以下①~④步反应。
①IO3-+SO32-=IO2-+SO42-(反应速率慢)
②IO2-+2SO32-=I-+2SO42-(反应速率快)
③5I-+IO3-+6H+=3I2+3H2O(反应速率快)
④I2+SO32-+H2O=2I-+SO42-+2H+(反应速率快)
下列说法不正确的是:
①IO3-+SO32-=IO2-+SO42-(反应速率慢)
②IO2-+2SO32-=I-+2SO42-(反应速率快)
③5I-+IO3-+6H+=3I2+3H2O(反应速率快)
④I2+SO32-+H2O=2I-+SO42-+2H+(反应速率快)
下列说法不正确的是:
| A.IO2-和 I-是该反应的催化剂 |
| B.此反应总反应速率由反应①决定 |
| C.此反应①中氧化剂是IO3-,反应③中还原剂是 I- |
| D.若生成 0.5mol 碘单质,则总反应中有 5mol 电子转移 |
您最近一年使用:0次

 )。下列说法正确的是
)。下列说法正确的是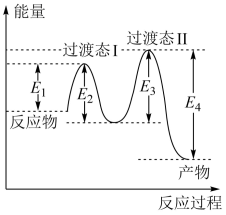
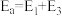
 的反应,必须加热才能进行
的反应,必须加热才能进行
 捕获和转化可减少
捕获和转化可减少 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到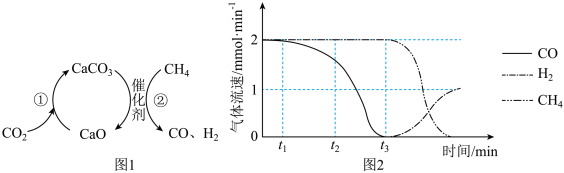
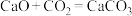 ;反应②为
;反应②为
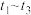 ,
, 比
比 多,且生成
多,且生成
 时刻,副反应生成
时刻,副反应生成 之后,反应②的速率逐渐减小
之后,反应②的速率逐渐减小

