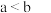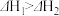下列关于反应热和热化学反应的描述中正确的是
| A.中和热为57.3 kJ∙mol−1,则浓H2SO4和NaOH反应的反应热为ΔH=−114.6 kJ∙mol−1 |
| B.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l) △H2,则△H1>△H2 |
| C.2CO(g)+O2(g)=2CO2(g) ΔH=−283.0 kJ∙mol−1,则CO(g)的燃烧热是283.0 kJ∙mol−1 |
D.CH3Cl(g)+Cl2(g)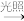 CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的ΔH>0 CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的ΔH>0 |
更新时间:2022-03-30 21:38:19
|
相似题推荐
【推荐1】下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ/mol | H2的燃烧热为483.6 kJ/mol |
| B | OH-(aq)+H+(aq)= H2O(g) △H=-57.3 kJ/mol | 含1mol NaOH的稀溶液与浓H2SO4完全中和,放出热量小于57.3 kJ |
| C | 2C(s)+2O2(g)=2CO2(g) △H=-a kJ/mol 2C(s)+O2(g)=2CO(g) △H=-b kJ/mol | b<a |
| D | C(石墨,s)=C(金刚石,s) △H=+1.5 kJ/mol | 金刚石比石墨稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关中和反应及其反应热测定实验的说法错误的是
| A.强酸与强碱的稀溶液发生中和反应生成lmol水时,放出的热量约为57.3kJ |
| B.为了使反应更充分,往往将碱溶液分多次倒入酸溶液中,并不断搅拌 |
| C.大烧杯上用硬纸板作盖板,可以减少热量的散失 |
| D.测定中和热时,酸和碱溶液一般采用稀溶液,避免浓溶液稀释额外放热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】已知:(1)HCl(aq)和NaOH(aq)反应的中和热△H=-57.3 kJ • mol−1;
(2)CO(g)的燃烧热是283.0 kJ·mol−1。则下列描述正确的是
(2)CO(g)的燃烧热是283.0 kJ·mol−1。则下列描述正确的是
| A.H2SO4(aq)和NaOH(aq)反应的中和热△H=2×(-57.3) kJ·mol−1 |
| B.2CO2(g)=2CO(g)+O2(g) △H=2×(+283.0) kJ·mol−1 |
| C.1/2H2SO4(aq,浓)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l) △H=-57.3 kJ·mol−1 |
| D.1 mol甲烷燃烧所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法错误的是
| A.所有燃烧反应都是放热反应 |
| B.由H原子形成1molH-H键要放出热量 |
| C.凡经加热而发生的化学反应都是吸热反应 |
| D.在稀溶液中,强酸与强碱发生中和反应生成1mol液态水时释放的热量称为中和热 |
您最近一年使用:0次
【推荐2】C和 在生产、生活、科技中是重要的燃料。
在生产、生活、科技中是重要的燃料。
①
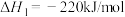
②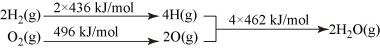
下列推断正确的是
 在生产、生活、科技中是重要的燃料。
在生产、生活、科技中是重要的燃料。①

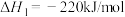
②
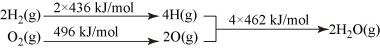
下列推断正确的是
A. 的燃烧热为 的燃烧热为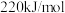 |
B.  |
C.  |
D.欲分解2mol ,至少需要提供 ,至少需要提供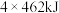 的热量 的热量 |
您最近一年使用:0次
【推荐2】已知:
①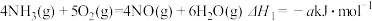
②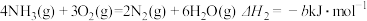
③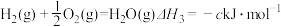
④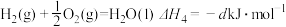
下列叙述正确的是
①
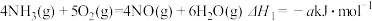
②
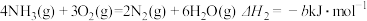
③
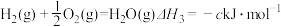
④
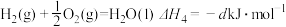
下列叙述正确的是
A.由上述热化学方程式可知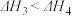 |
B. 的摩尔燃烧焓为 的摩尔燃烧焓为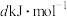 |
C.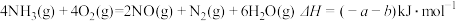 |
D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法中正确的是
| A.熵增加且放热的反应一定是自发反应 |
| B.非自发反应在任何条件下都不能实现 |
| C.凡是放热反应都是自发的,吸热反应都是非自发的 |
| D.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.非自发反应一定不能实现 |
| B.同种物质气态时熵值最小,固态时熵值最大 |
| C.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H <0 |
| D.恒温恒压下,△H <0且△S>0的反应一定不能自发进行 |
您最近一年使用:0次

 O2(g)=2CO2(g)+H2O(g)
O2(g)=2CO2(g)+H2O(g) 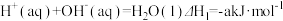
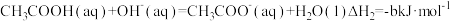 下列关系正确的是
下列关系正确的是