如图所示,将锌、铜通过导线相连,置于稀硫酸中。
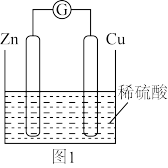
(1)锌片为____ 极,电极反应为:____ 。
(2)铜片为____ 极,电极反应为:____ 。
(3)若反应中有0.2mol电子转移,则生成的氢气在标准状况下的体积为____ 。

(1)锌片为
(2)铜片为
(3)若反应中有0.2mol电子转移,则生成的氢气在标准状况下的体积为
更新时间:2022-04-12 08:20:49
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】工作原理: (以Zn-H2SO4-Cu原电池为例)
| 电极材料 | 锌 | 铜 |
| 电极名称 | ||
| 电极反应 | Zn-2e-=Zn2+ | 2H++2e-=H2↑ |
| 反应类型 | ||
| 外电路电子流向 | 由 | |
| 内电路离子移向 | 溶液中 | |
| 原电池总反应 | Zn+2H+=Zn2++H2↑ | |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】依据氧化还原反应:2Ag +(aq)+Cu(s)=Cu 2+(aq)+2Ag(s)设计的原电池如图所示。
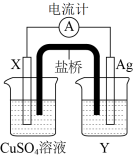
请回答下列问题:
(1)电极X的材料是_______ ;电解质溶液Y是 _______ ;
(2)银电极为电池的_______ 极,发生的电极反应为 _______ ;
(3)外电路中的电子是从_______ 电极流向 _______ 电极。外电路中每通过0.1 mol电子,银电极的质量理论上增加 _______ g。
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl -移向_______ 电极。

请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl -移向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】原电池原理
(1)根据原电池的工作原理分析判断(填写“正极”或“负极”)。
①由组成原电池的电极材料判断。一般是活动性较强的金属为___________ 极,活动性较弱的金属或能导电的非金属为___________ 极。
②根据电流方向或电子流动方向判断。电流由___________ 极流向___________ 极;电子由___________ 极流向___________ 极。
③根据原电池中电解质溶液内离子的移动方向判断。在原电池的电解质溶液内,阳离子移向___________ 极,阴离子移向___________ 极。
④根据原电池两极发生的变化来判断。原电池的___________ 极失电子发生氧化反应,其___________ 极得电子发生还原反应。
⑤根据现象判断。一般情况下,溶解的一极为___________ 极,增重或有气体逸出的一极为___________ 极。
(2)如图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下。
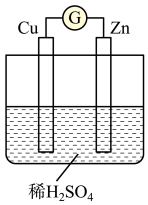
①实验报告中记录合理的是___________ (填字母)。
②请写出该电池的负极反应式:___________ 。
③将稀硫酸换成硫酸铜溶液,电极质量增加的是___________ (填“锌极”或“铜极”,下同),溶液中 移向
移向___________ 。
(1)根据原电池的工作原理分析判断(填写“正极”或“负极”)。
①由组成原电池的电极材料判断。一般是活动性较强的金属为
②根据电流方向或电子流动方向判断。电流由
③根据原电池中电解质溶液内离子的移动方向判断。在原电池的电解质溶液内,阳离子移向
④根据原电池两极发生的变化来判断。原电池的
⑤根据现象判断。一般情况下,溶解的一极为
(2)如图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下。

| a.电流计指针偏转 |
| b.Cu极有H2产生 |
| c.H+向负极移动 |
| d.电流由Zn经导线流向Cu |
②请写出该电池的负极反应式:
③将稀硫酸换成硫酸铜溶液,电极质量增加的是
 移向
移向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入足量 的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
①哪一段时间内反应速率最大:____ min(填“0~1”或“1~2”或“2~3”或“3~4” 或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是____ (填字母序号)。
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:
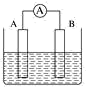
①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是_______ (填“铝片”或“镁片”)。
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:____ ;若该电池反应消耗了 0.1mol FeCl3, 则转移电子的数目为 _____ 。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:

①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:
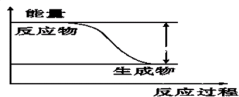
(1)该反应为______ 反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是______ (填字母)。
A.改铁片为铁粉 B.增大压强 C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____ 极(填“正”或“负”)。铜片上产生的现象为______ ,该极上发生的电极反应为______ 。

(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.增大压强 C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是_______ (填“离子键”或“共价键”)。
(2)下列化学反应在理论上可以设计成原电池的是_______(填字母)。
(3)如图为某燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为_______ (填物质名称),电解质溶液中的OH-移向_______ (“负”或“正”)。
②写出此氢氧燃料电池工作时总反应方程式:_______ 。
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是
(2)下列化学反应在理论上可以设计成原电池的是_______(填字母)。
A.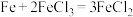 | B. |
C. | D.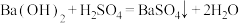 |

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
②写出此氢氧燃料电池工作时总反应方程式:
您最近一年使用:0次



