能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入足量 的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
①哪一段时间内反应速率最大:____ min(填“0~1”或“1~2”或“2~3”或“3~4” 或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是____ (填字母序号)。
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:
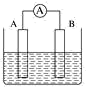
①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是_______ (填“铝片”或“镁片”)。
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:____ ;若该电池反应消耗了 0.1mol FeCl3, 则转移电子的数目为 _____ 。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:

①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:
更新时间:2020-07-08 09:47:54
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】白醋是照调中的酸味辅料,能改善调节人体的新陈代谢,其主要成分为CH3COOH,为一元弱酸,回答下列问题:
(1)25℃时,pH=5的醋酸溶液中,由水电离出的c(H+)=_____ mol∙L−1。
(2)已知CH3COOH的Ka=1.74×10−5,NH3∙H2O的Kb=1.74×10−5,则CH3COONH4的浓溶液呈_____ (填“酸性”或“中性”或“碱性”);将CH3COONH4加到Mg(OH)2悬浊液中,发现沉淀溶解,试解释原因:______ (用文字和方程式说明)。
(3)用如图所示装置测定Zn和4.0 mol∙L−1、2.0 mol∙L−1醋酸的反应速率:
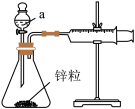
①仪器a的名称为_____ 。
②Zn和醋酸溶液反应的离子方程式为______ 。
③设计实验方案:在不同浓度醋酸溶液下,测定_____ (要求所测得的数据能直观体现反应速率大小)。
(1)25℃时,pH=5的醋酸溶液中,由水电离出的c(H+)=
(2)已知CH3COOH的Ka=1.74×10−5,NH3∙H2O的Kb=1.74×10−5,则CH3COONH4的浓溶液呈
(3)用如图所示装置测定Zn和4.0 mol∙L−1、2.0 mol∙L−1醋酸的反应速率:

①仪器a的名称为
②Zn和醋酸溶液反应的离子方程式为
③设计实验方案:在不同浓度醋酸溶液下,测定
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题
(1)甲烷可以和氯气在光照条件下发生反应,反应类型为:_____ ,产物之一CCl4的空间构型为:________ 。
(2)比较锌粒与不同浓度硫酸反应时的速率,可通过如下装置,测定收集等体积H2需要的时间来实现。该实验装置在加入试剂前需进行__________ ,该装置中仪器a的名称:__________ 。
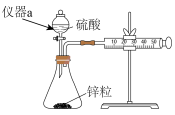
(3)在酸性KMnO4与H2C2O4(草酸,一种弱酸)反应时,可通过测定褪色时间来确定反应速率,请写出该反应的离子方程式:_________________ 。
(4)在地壳内SiO2和HF存在以下平衡: SiO2(s) +4HF(g) SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为_________ mol·Lˉ1·minˉ1。
(1)甲烷可以和氯气在光照条件下发生反应,反应类型为:
(2)比较锌粒与不同浓度硫酸反应时的速率,可通过如下装置,测定收集等体积H2需要的时间来实现。该实验装置在加入试剂前需进行

(3)在酸性KMnO4与H2C2O4(草酸,一种弱酸)反应时,可通过测定褪色时间来确定反应速率,请写出该反应的离子方程式:
(4)在地壳内SiO2和HF存在以下平衡: SiO2(s) +4HF(g)
 SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2触摸试管情况 观察结果 反应完成所需的时间
粉末状 很烫 剧烈反应,带火星的木条复燃 3.5min
块状 微热 反应较慢,火星红亮但木条未复燃 30min
(1)写出上述实验中发生反应的化学方程式:_____ ;
(2)实验结果表明,催化剂的催化效果与_____ 有关;
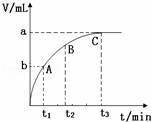
(3)某同学在10mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是_____ 。
MnO2触摸试管情况 观察结果 反应完成所需的时间
粉末状 很烫 剧烈反应,带火星的木条复燃 3.5min
块状 微热 反应较慢,火星红亮但木条未复燃 30min
(1)写出上述实验中发生反应的化学方程式:
(2)实验结果表明,催化剂的催化效果与
(3)某同学在10mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
(1)增加Fe的量,其正反应速率_________ (填“增大”“不变”或“减小”,下同),平衡________ 移动(填“不”“向正反应方向”或“向逆反应方向”,下同)。
(2)将容器的体积缩小一半,其正反应速率________ ,平衡________ 移动。
(3)保持体积不变,充入N2使体系压强增大,其正反应速率________ ,平衡____________ 移动。
(4)保持体积不变,充入水蒸气,其正反应速率________ ,平衡____________ 移动。
 Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:(1)增加Fe的量,其正反应速率
(2)将容器的体积缩小一半,其正反应速率
(3)保持体积不变,充入N2使体系压强增大,其正反应速率
(4)保持体积不变,充入水蒸气,其正反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定条件下,在1L密闭容器中发生反应:3A(g)+B(g) 2C(g)开始时加入4molA、6molB、2molC,在1min末测得C的物质的量是3mol。
2C(g)开始时加入4molA、6molB、2molC,在1min末测得C的物质的量是3mol。
(1)若该反应为放热反应,则反应过程中_______ 能转化为_______ 能。
(2)用B的浓度变化表示反应的平均速率为_______ mol/(L•min)填(“0.5”或“1.5”)
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”)
①降低温度,化学反应速率_______ ;
②充入1molA,化学反应速率_______ ;
③将容器的体积变为0.5L,化学反应速率_______
 2C(g)开始时加入4molA、6molB、2molC,在1min末测得C的物质的量是3mol。
2C(g)开始时加入4molA、6molB、2molC,在1min末测得C的物质的量是3mol。(1)若该反应为放热反应,则反应过程中
(2)用B的浓度变化表示反应的平均速率为
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”)
①降低温度,化学反应速率
②充入1molA,化学反应速率
③将容器的体积变为0.5L,化学反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
①哪一段时间内反应速率最大:___________ min。(填“0~ 1” “1~2”“2~3”“3~4”或“4~ 5”)
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是___________ 。(填字母序号)
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是___________ 反应 (填“放热”或“吸热”)
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称___________ , B 电极反应式:___________ ,该电池在工作时,溶液中Fe3+向___________ (填“A”、“B” )移动,A电极的质量将___________ 。 (填“增加”、“减小”或“不变”)
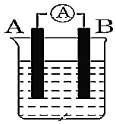
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
| 时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL (标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某实验小组同学进行如下实验:
(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是__ (填序号)。

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中__ (填A或B)处电极入口通甲烷,该原电池的正极电极反应式为___ 。当消耗标况下甲烷33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量__ mol。
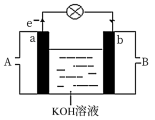
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
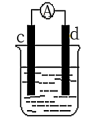
①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸,写出该原电池正极的电极反应式为___ 。
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为__ ;该原电池的负极反应式为___ 。
(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中

(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸,写出该原电池正极的电极反应式为
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】尝试分析如图所示的原电池的工作原理_________________________ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】发生化学反应时,物质变化的同时常常伴随有能量变化。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为___________ 能。
(2)某化学反应中,反应物的总能量为E1,生成物的总能量为E2,且E1<E2,则该反应是___________ (填“放热”或“吸热”)反应。
(3)已知:键能是指气态分子中1 mol化学键解离成气态原子所吸收的能量。
当H2和O2化合生成2 mol H2O(g)时,放出___________ kJ的能量。
(4)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
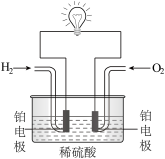
①通入H2的电极是电池的___________ (填“正”或“负”)极。通入O2的电极反应式是___________ 。
②如果电解质溶液为KOH溶液,写出通入H2的电极反应式是___________ 。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(2)某化学反应中,反应物的总能量为E1,生成物的总能量为E2,且E1<E2,则该反应是
(3)已知:键能是指气态分子中1 mol化学键解离成气态原子所吸收的能量。
| 化学键 | H-H | O=O | H-O |
| 键能/kJ·mol | 436 | 498 | 463 |
(4)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。

①通入H2的电极是电池的
②如果电解质溶液为KOH溶液,写出通入H2的电极反应式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列问题
(1)下列反应中,属于放热反应的是___________ ,属于吸热反应的是___________ 。
①Ba(OH)2·8H2O晶体与NH4Cl晶体 ②炸药爆炸 ③生石灰与水作用制熟石灰
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是___________ ,负极的电极反应式是 ___________ 。
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了6.5g,铜表面析出了氢气___________ L(标准状况),导线中通过___________ mol e-。
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为___________ 热反应,中和反应都是___________ 热反应,其实质是___________ (用离子方程式表示)。
(1)下列反应中,属于放热反应的是
①Ba(OH)2·8H2O晶体与NH4Cl晶体 ②炸药爆炸 ③生石灰与水作用制熟石灰
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了6.5g,铜表面析出了氢气
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】将铁片和银片插入某种电解质溶液,铁片和银片用导线相连形成原电池装置。

(1)若电解质溶液是稀硫酸,则发生氧化反应的是___ 极(填“铁”、“银”),银电极发生的电极反应式___ ,该电池的总反应方程式是___ 。
(2)若电解质溶液是硫酸铜溶液,银极上反应的电极反应方程式是___ ,该电池总反应方程式是___ 。当负极质量减轻5.6g时,正极的质量增加___ g。

(1)若电解质溶液是稀硫酸,则发生氧化反应的是
(2)若电解质溶液是硫酸铜溶液,银极上反应的电极反应方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】化学电源在生产生活中有着广泛的应用,请回答下列问颕:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_____ (填字母,下同)。
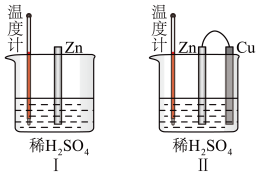
(2)为了探究化学反应中的能量变化,某同学设计了如图两个对比实验(除图Ⅱ中增加导线和铜片外,其余条件完全相同)。经过相同时间后,温度计示数:图I_____ 图Ⅱ(填“高于”、“等于”或“低于”),产生气体的速率:图I_____ 图Ⅱ(填“大于”、“等于”或“小于”)。
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是_____ (填化学式),电解质溶液是_____ (填化学式)溶液。
②正极上发生的电极反应为_____ 。
③若导线上转移的电子为1mol,则消耗的金属铜的质量为_____ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是
| A.Ba(OH)2+2NH4Cl=BaCl2+2NH3↑+2H2O | B.Cu+Ag+=Ag+Cu2+ |
| C.Zn+H2SO4=ZnSO4+H2↑ | D.CaO+H2O=Ca(OH)2 |

(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是
②正极上发生的电极反应为
③若导线上转移的电子为1mol,则消耗的金属铜的质量为
您最近一年使用:0次



