表为元素周期表的一部分。
请回答有关问题:
(1)元素⑥的最高价氧化物对应的水化物为_______ (填名称)。
(2)请写出元素①的简单氢化物的电子式:_______ ,该化合物中存在的化学键类型是_______ (填英文字母)。
A.离子键 B.共价键 C.离子键和共价键
(3)请写出碳元素在周期表中的位置:_______ 。
(4)②、⑥、⑦三种元素的简单氢化物稳定性由强到弱排序为_______ (用化学式及“>”表示)。
(5)元素⑤的单质与元素③最高价氧化物对应的水化物反应的离子方程式为_______ 。
(6)请写出元素⑧的单质与水反应的化学方程式:_______ 。
| I A | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ① | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 4 | ⑧ |
(1)元素⑥的最高价氧化物对应的水化物为
(2)请写出元素①的简单氢化物的电子式:
A.离子键 B.共价键 C.离子键和共价键
(3)请写出碳元素在周期表中的位置:
(4)②、⑥、⑦三种元素的简单氢化物稳定性由强到弱排序为
(5)元素⑤的单质与元素③最高价氧化物对应的水化物反应的离子方程式为
(6)请写出元素⑧的单质与水反应的化学方程式:
更新时间:2022-04-16 10:34:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分。
回答下列问题:
(1)Z元素在周期表中的位置为__________________ 。
(2)表中Y,硫和Z三种元素的简单离子半径由大到小的顺序是(填离子符号)____________ 。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________ ;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2mol Mg(OH)2和1mol气态烃。该烃分子中碳氢质量比为9∶1,烃的电子式为__________________ ,Q与水反应的化学方程式为__________________________ 。
| 碳 | 氮 | Y | |
| X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为
(2)表中Y,硫和Z三种元素的简单离子半径由大到小的顺序是(填离子符号)
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2mol Mg(OH)2和1mol气态烃。该烃分子中碳氢质量比为9∶1,烃的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】国家卫健委发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查,这些食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂,用于食品生产中,将更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)富硒酵母是一种新型添加剂,其中硒34Se元素在周期表中的位置为_______
(2)下列说法正确的是_______ 。
A.热稳定性:H2Se>H2S>H2O B.酸性:H2SeO4>H2SO4>HClO4
C.36S与74Se的中子数之和为60 D.还原性:Se2->S2- E.沸点高低:H2Se>H2S>H2O
(3)短周期元素d、e、f、g、h、x都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:

①d、e、f、g、h元素形成的简单离子中半径最大的是_______ (用化学式表示)。
②元素e与f相比较金属性较强的是e,下列不能证明这一事实的是_______ (填字母)。
A.e的最外层电子数比f少
B.e单质与水反应比f单质与水反应更剧烈
C.e最高价氧化物对应的水化物的碱性比f的强
③x和d组成的化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为___ 。
(1)富硒酵母是一种新型添加剂,其中硒34Se元素在周期表中的位置为
(2)下列说法正确的是
A.热稳定性:H2Se>H2S>H2O B.酸性:H2SeO4>H2SO4>HClO4
C.36S与74Se的中子数之和为60 D.还原性:Se2->S2- E.沸点高低:H2Se>H2S>H2O
(3)短周期元素d、e、f、g、h、x都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:

①d、e、f、g、h元素形成的简单离子中半径最大的是
②元素e与f相比较金属性较强的是e,下列不能证明这一事实的是
A.e的最外层电子数比f少
B.e单质与水反应比f单质与水反应更剧烈
C.e最高价氧化物对应的水化物的碱性比f的强
③x和d组成的化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,并回答下列问题:
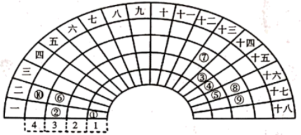
(1)元素②的名称为___________ ;元素⑩在常见周期表中的位置是___________ 。
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是___________ (填化学式,下同);元素④、⑧、⑨的最高价氧化物对应的水化物,酸性最强的是___________ 。
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应的化学方程式为___________ 。
(5)请设计简单实验,比较元素②、⑦的金属性强弱。

(1)元素②的名称为
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应的化学方程式为
(5)请设计简单实验,比较元素②、⑦的金属性强弱。
| 实验步骤 | 实验现象 | 实验结论 |
| 金属性:②>⑦ |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是_______ 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:_______ 。
(3)洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是_______。
(4)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因_______ 。常温下HClO的电离平衡常数为_______ 。洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式_______ 。
(5)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为_______ 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH
K2FeO4在水溶液中易水解:4 +10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
+10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______ 溶液(填序号)
a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
(6)消毒效率是物质单位质量得到的电子数,则Cl2与NaClO两种消毒剂的消毒效率之比为__ 。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:
(3)洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是_______。
| A.酸性:HF>HCl>HBr>HI | B.键能:H—F>H—Cl>H—Br>H—I |
| C.熔点:HF<HCl<HBr<HI | D.还原性:HF<HCl<HBr<HI |
(5)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH
K2FeO4在水溶液中易水解:4
 +10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
+10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
(6)消毒效率是物质单位质量得到的电子数,则Cl2与NaClO两种消毒剂的消毒效率之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。

(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是_____ ,最不活泼的元素是___________ 。
(2)第三周期元素除⑩外原子半径最小的是______ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________ (填化学式,下同),具有两性的是____________ ,最高价氧化物对应水化物中酸性最强的是__________ 。
(3)⑥⑦⑨形成的简单离子的由小到大的顺序是______________ (用离子符号回答问题),
⑧与⑨对应的氢化物比较稳定的是_________ (填化学式)。
(4)⑤和③可以形成两种化合物,其中可以做呼吸面具供氧剂的物质的电子式为_________ ,所含化学键的类型为 _______________ 。
(5)①与⑧形成的化合物的结构式__________ ,用电子式表示 ⑥与⑨所形成化合物的形成过程 _________________________ 。

(1)非金属性最强的元素是
(2)第三周期元素除⑩外原子半径最小的是
(3)⑥⑦⑨形成的简单离子的由小到大的顺序是
⑧与⑨对应的氢化物比较稳定的是
(4)⑤和③可以形成两种化合物,其中可以做呼吸面具供氧剂的物质的电子式为
(5)①与⑧形成的化合物的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分。
回答下列问题
(1)表中元素原子半径最大的是(写元素符号)__________ ,Z原子核外电子能量最高的电子亚层是__________ 。
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:_________________ ;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因______________________________________________________ 。
(4)硫酸工业生产中接触室内发生的反应方程式为______________________________________ ;
在实际生产中,操作温度选定400—500℃、压强通常采用常压的原因分别是__________________________________________________________________________________________________ 。
碳 | 氮 | Y | |
X | 硫 | Z |
(1)表中元素原子半径最大的是(写元素符号)
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:
(4)硫酸工业生产中接触室内发生的反应方程式为
在实际生产中,操作温度选定400—500℃、压强通常采用常压的原因分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空。
(1)前20号元素中气态氢化物最稳定的是:_____ (填化学式)。
(2)前20号元素中最高价氧化物对应水化物碱性最强的碱为:_____ (填写名称)。
(3)第Ⅵ A族元素所形成的氢化物中沸点最高的是:____ (填化学式)。
(4)短周期主族元素中原子半径最大的元素是:_____ (填写名称)。
(5)Fe在元素周期表中位置为:______ 。
(6)以下晶体,存在分子间作用力的共价化合物是_______ (填序号)。
①Ne晶体 ②NH4Cl晶体 ③CaCl2晶体 ④干冰 ⑤水晶
(7)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_______ (填序号)。
① HCl的溶解度比H2S的大
② HCl的酸性比H2S的强
③ HCl的稳定性比H2S的强
④ Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑤ HClO4的酸性比H2SO4的强
⑥ Cl2能与H2S反应生成S
(1)前20号元素中气态氢化物最稳定的是:
(2)前20号元素中最高价氧化物对应水化物碱性最强的碱为:
(3)第Ⅵ A族元素所形成的氢化物中沸点最高的是:
(4)短周期主族元素中原子半径最大的元素是:
(5)Fe在元素周期表中位置为:
(6)以下晶体,存在分子间作用力的共价化合物是
①Ne晶体 ②NH4Cl晶体 ③CaCl2晶体 ④干冰 ⑤水晶
(7)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
① HCl的溶解度比H2S的大
② HCl的酸性比H2S的强
③ HCl的稳定性比H2S的强
④ Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑤ HClO4的酸性比H2SO4的强
⑥ Cl2能与H2S反应生成S
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】规律提炼题组
(1)下列事实能说明氯元素原子得电子能力比硫元素原子强的是_____ (填序号)。
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大 ④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧 ⑨还原性:Cl-<S2-
(2)有三种金属元素A、B、C,在相同条件下,B的最高价氧化物的水化物的碱性比A的最高价氧化物的水化物的碱性强;若将A、C相连后投入稀硫酸中,发现C表面有明显气泡产生。则这三种金属元素的原子失电子能力由强到弱的顺序是________ 。
(1)下列事实能说明氯元素原子得电子能力比硫元素原子强的是
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大 ④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧 ⑨还原性:Cl-<S2-
(2)有三种金属元素A、B、C,在相同条件下,B的最高价氧化物的水化物的碱性比A的最高价氧化物的水化物的碱性强;若将A、C相连后投入稀硫酸中,发现C表面有明显气泡产生。则这三种金属元素的原子失电子能力由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】物质是由微观粒子构成的,人类对构成物质的微观粒子间结合方式的认识源远流长。
请按下列要求填空。
Ⅰ.有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)只含非极性共价键的物质是_________________ (填序号,下同)。
(2)由离子键和共价键构成的物质是_________________ 。
Ⅱ. 下列变化中:①蔗糖溶于水 ②氯化钠熔化 ③氨气液化④ 溶于水 ⑤
溶于水 ⑤  溶于水⑥
溶于水⑥ 溶于水
溶于水
(3)只有离子键被破坏的是_____________________ 。
(4)既有离子键被破坏,又有共价键被破坏的是_____________________ 。
Ⅲ.有下列微粒或物质:①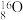 、
、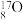 、
、 ②石墨、金刚石 ③
②石墨、金刚石 ③ 、
、 ④
④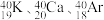
(5)互为同位素的是_____________________ ;互为同素异形体的是_____________________ 。
请按下列要求填空。
Ⅰ.有下列物质:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)只含非极性共价键的物质是
(2)由离子键和共价键构成的物质是
Ⅱ. 下列变化中:①蔗糖溶于水 ②氯化钠熔化 ③氨气液化④
 溶于水 ⑤
溶于水 ⑤  溶于水⑥
溶于水⑥ 溶于水
溶于水(3)只有离子键被破坏的是
(4)既有离子键被破坏,又有共价键被破坏的是
Ⅲ.有下列微粒或物质:①
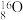 、
、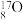 、
、 ②石墨、金刚石 ③
②石墨、金刚石 ③ 、
、 ④
④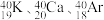
(5)互为同位素的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】正交硫和单斜硫是硫元素的两种常见单质,其晶状结构如左下图所示;构成晶体的微粒均是S8分子,其分子结构如右下图所示。回答下列问题:
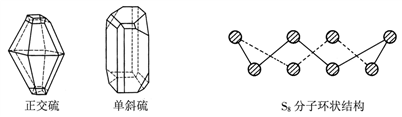
(1)正交硫和单斜硫互称为硫元素的________________ 。
(2)S8分子中,硫原子之间形成的化学键是_____ (填“离子键”或“共价键”)。
(3)已知正交硫的熔点为112.8 ℃,沸点为444.6 ℃,硬度较小。晶状的正交硫是________ 晶体,构成晶体的微粒间的相互作用力是___________________ 。
(4)已知:S8(正交) =S8(单斜) ΔH=+2.64 kJ·molˉ1。正交硫与单斜硫相比,相对比较稳定的是_______________ 。正交硫转化为单斜硫时,发生________ (填“物理变化”或“化学变化”)。
(5)已知通常状况下4g 硫粉完全燃烧放出37 kJ的热量,写出该反应的热化学方程式___________________________________________________ 。

(1)正交硫和单斜硫互称为硫元素的
(2)S8分子中,硫原子之间形成的化学键是
(3)已知正交硫的熔点为112.8 ℃,沸点为444.6 ℃,硬度较小。晶状的正交硫是
(4)已知:S8(正交) =S8(单斜) ΔH=+2.64 kJ·molˉ1。正交硫与单斜硫相比,相对比较稳定的是
(5)已知通常状况下4g 硫粉完全燃烧放出37 kJ的热量,写出该反应的热化学方程式
您最近一年使用:0次

 元素的原子序数为11,与之相邻的同族元素的原子序数是
元素的原子序数为11,与之相邻的同族元素的原子序数是 周期序数的元素有
周期序数的元素有

