Ⅰ.化学研究的对象是物质,下列物质:①HCl②NaOH③Cl2④H2O2⑤NH4Cl⑥P4⑦NH3·H2O⑧Na2O2⑨HClO⑩MgCl2中
(1)只存在离子键的是____ (填序号)。
(2)含有非极性键的共价化合物的是____ (填序号)。
(3)既存在离子键又存在共价键的是____ (填序号)。
(4)②熔化过程破坏____ (选填“离子键”、“极性键”、“非极性键”或“范德华力”)。
(5)③溶于水破坏____ (选填“离子键”、“极性键”、“非极性键”或“范德华力”)。
Ⅱ.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:

(6)电极d是____ (填“正极”或“负极”),电极c的电极反应式____ 。
(7)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为____ L。
(1)只存在离子键的是
(2)含有非极性键的共价化合物的是
(3)既存在离子键又存在共价键的是
(4)②熔化过程破坏
(5)③溶于水破坏
Ⅱ.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:

(6)电极d是
(7)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
更新时间:2022-04-18 21:49:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某学习小组对化学反应2Al+3H2SO4 = Al2(SO4)3+ 3H2↑进行研究。
(1)该反应的还原剂是________ ,发生_________ 反应(填“氧化”或“还原”)。若将该反应设计成原电池,用铜作电极材料之一,铜电极上的现象为_________ 。
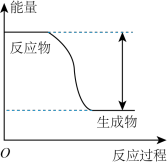
(2)该反应的能量变化如下图所示。该反应为__________ 反应(填“吸热”或“放热”)。
(3)下列措施中,能加快化学反应速率的是_________ (填字母序号)。
a 用等质量的铝粉代替铝块
b 将反应的试管放置在冰水中
c 往容器中加少量Na2SO4固体
d 往稀硫酸溶液中添加几滴98%的浓硫酸
(4)足量铝与20mL1.0mol/L稀硫酸的反应过程中,某20s内共收集到气体44.8mL(已换算成标况下)。请选用合适的物质表示此20s内的化学反应速率:______ 。
(1)该反应的还原剂是
(2)该反应的能量变化如下图所示。该反应为

(3)下列措施中,能加快化学反应速率的是
a 用等质量的铝粉代替铝块
b 将反应的试管放置在冰水中
c 往容器中加少量Na2SO4固体
d 往稀硫酸溶液中添加几滴98%的浓硫酸
(4)足量铝与20mL1.0mol/L稀硫酸的反应过程中,某20s内共收集到气体44.8mL(已换算成标况下)。请选用合适的物质表示此20s内的化学反应速率:
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】Ⅰ.电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。
(1)该电池的正极为__________ ,负极的电极反应式为___________ 。
(2)电池工作时,电池内部溶液中的OH−移向______ 极(填“Ag2O”或“Zn”),正极区域溶液的pH___ 填“增大”、“减小”或“不变”)。
Ⅱ.FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为________________ 。若将该反应设计成原电池,请在右图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液。__________

(1)该电池的正极为
(2)电池工作时,电池内部溶液中的OH−移向
Ⅱ.FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将在空气中久置的铝片投入足量稀硫酸中,该铝片与稀硫酸反应产生氢气的速率与反应时间可用下图来表示(已知该反应为放热反应),请回答下列问题。

(1)曲线由 段,用离子方程式表示不产生氢气的原因
段,用离子方程式表示不产生氢气的原因_______ 。
(2)曲线由 段,产生氢气的速率较慢的原因
段,产生氢气的速率较慢的原因_______ 。
(3)曲线由 段,产生氢气的速率增加较快的主要原因
段,产生氢气的速率增加较快的主要原因_______ 。
(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因_______ 。
(5)下列措施能加快上述反应的化学反应速率的是_______。

(1)曲线由
 段,用离子方程式表示不产生氢气的原因
段,用离子方程式表示不产生氢气的原因(2)曲线由
 段,产生氢气的速率较慢的原因
段,产生氢气的速率较慢的原因(3)曲线由
 段,产生氢气的速率增加较快的主要原因
段,产生氢气的速率增加较快的主要原因(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因
(5)下列措施能加快上述反应的化学反应速率的是_______。
| A.加入少量蒸馏水 | B.铝片改为铝粉 |
| C.加入少量饱和硫酸钠溶液 | D.加入少量硫酸铜溶液 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】从能量的变化和反应的快慢等角度研究反应:CH4+2O2=2H2O+CO2。
(1)下图能正确表示该反应中能量变化的是________ 。

(2)酸性甲烷燃料电池的总反应方程式为CH4+2O2 = 2H2O+CO2。其中,负极的电极反应式为________ ;正极发生________ 反应(填“氧化”或“还原”)。电路中每转移0.2 mol电子,标准状况下消耗O2的体积是________ L。
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应Cu+2Ag+=Cu2++2Ag设计一个化学电池,并回答下列问题:
①该电池的正极材料是________ ,负极材料是 ________ ,电解质溶液是 ________ 。
②正极的电极反应式为________ 。
(1)下图能正确表示该反应中能量变化的是

(2)酸性甲烷燃料电池的总反应方程式为CH4+2O2 = 2H2O+CO2。其中,负极的电极反应式为
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应Cu+2Ag+=Cu2++2Ag设计一个化学电池,并回答下列问题:
①该电池的正极材料是
②正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(1)丙装置中负极反应式为_________________ ,丁装置中负极反应式为__________________ 。
(2)电池的放电过程中,甲装置中溶液质量________ (填“增加”或“减少”);丁装置中溶液碱性________ (填“增强”或“减弱”)。
(3)当甲装置导线中转移0.3 mol电子时,正极生成气体________ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3 mol电子时,两电极质量相差________ g。


(1)丙装置中负极反应式为
(2)电池的放电过程中,甲装置中溶液质量
(3)当甲装置导线中转移0.3 mol电子时,正极生成气体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
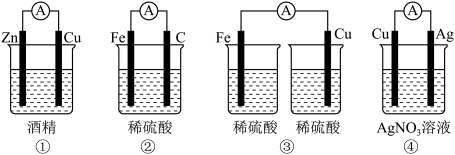
(1)如图装置中属于原电池的是____ (填序号)。
(2)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图1所示。
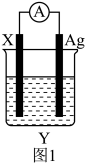
①电极X的材料是____ 。
②X电极的电极反应式为____ ;Ag电极上发生的是___ (填“氧化”或“还原”)反应。
③当有2.8 g铁溶解时,Ag电极增重____ g。
(3)以甲烷为燃料的新型电池得到广泛的研究,如图2是目前研究较多的一类燃料电池的工作原理示意图。
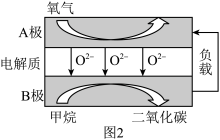
①A极为电池极____ (填“正”或“负”)。
②B极的电极反应式为____ ;若消耗标准状况下的CH411.2 L,则电路中转移____ mol电子。
(1)如图装置中属于原电池的是

(2)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图1所示。

①电极X的材料是
②X电极的电极反应式为
③当有2.8 g铁溶解时,Ag电极增重
(3)以甲烷为燃料的新型电池得到广泛的研究,如图2是目前研究较多的一类燃料电池的工作原理示意图。

①A极为电池极
②B极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】许多金属及他们的化合物在科学研究和工业生产中具有许多用途,回答下列有关问题
 下列有关的说法正确的是
下列有关的说法正确的是 ______
A、第一电离能大小: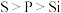
B、因为晶格能CaO比KCl高,所以KCl比CaO熔点低
C、 与
与 的化学性质类似,分子结构也都呈直线型,相同条件下
的化学性质类似,分子结构也都呈直线型,相同条件下 的溶解度更大
的溶解度更大
D、分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
 镍
镍 可形成多种配合物,且各种配合物有广泛的用途。某镍配合物结构如图所示,分子内含有的作用力有
可形成多种配合物,且各种配合物有广泛的用途。某镍配合物结构如图所示,分子内含有的作用力有 ______  填序号
填序号

A.氢键 离子键
离子键 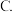 共价键 D.金属键
共价键 D.金属键  配位键
配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是______  甲基
甲基 中C原子的杂化方式为
中C原子的杂化方式为 ______
 铁和铜在生产和生活中有重要应用,基态
铁和铜在生产和生活中有重要应用,基态 的M层电子排布式为
的M层电子排布式为 ______ ,用晶体的x射线衍射发可以测得阿伏加 德罗常数,对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为 提示:
提示: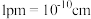 ,
, ,又知铜的密度为
,又知铜的密度为 ,则铜晶胞的质量是
,则铜晶胞的质量是 ______  保留两位小数
保留两位小数 ;阿伏加 德罗常数为
;阿伏加 德罗常数为 ______  保留两位小数
保留两位小数 。
。
 下列有关的说法正确的是
下列有关的说法正确的是 A、第一电离能大小:
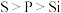
B、因为晶格能CaO比KCl高,所以KCl比CaO熔点低
C、
 与
与 的化学性质类似,分子结构也都呈直线型,相同条件下
的化学性质类似,分子结构也都呈直线型,相同条件下 的溶解度更大
的溶解度更大D、分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
 镍
镍 可形成多种配合物,且各种配合物有广泛的用途。某镍配合物结构如图所示,分子内含有的作用力有
可形成多种配合物,且各种配合物有广泛的用途。某镍配合物结构如图所示,分子内含有的作用力有  填序号
填序号

A.氢键
 离子键
离子键 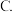 共价键 D.金属键
共价键 D.金属键  配位键
配位键组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是
 甲基
甲基 中C原子的杂化方式为
中C原子的杂化方式为  铁和铜在生产和生活中有重要应用,基态
铁和铜在生产和生活中有重要应用,基态 的M层电子排布式为
的M层电子排布式为  提示:
提示: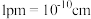 ,
, ,又知铜的密度为
,又知铜的密度为 ,则铜晶胞的质量是
,则铜晶胞的质量是  保留两位小数
保留两位小数 ;阿伏加 德罗常数为
;阿伏加 德罗常数为  保留两位小数
保留两位小数 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列四种物质中,①硫化钾、②干冰、③氩、④氢氧化钠 存在共价键的分子晶体是_____ ,只存在离子键的是_____ ,既存在离子键又存在共价键的是_____ ,不存在化学键的是_____ (请用序号填空)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请用下列10种物质的序号填空:
①O2 ②H2 ③ He ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦Al ⑧NaF ⑨NH3 ⑩I2。
(1)其中由共价键形成的单质是__________ ,既有离子键又有极性键的是_____ 。属于离子化合物的是_______________ .常温下是固态分子的是____________ 。
(2)NH3 的电子式是________________ 根据以上物质总结出的下列结论正确的有______________
①离子化合物只含有离子键
②只要有离子键的化合物就是离子化合物
③只要有共价键的物质就是共价化合物
④共价化合物只有共价键
⑤极性键不可能存在于离子化合物中
⑥金属元素与非金属元素之间只能形成离子键
⑦非金属元素与非金属元素之间只能形成共价键.
①O2 ②H2 ③ He ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦Al ⑧NaF ⑨NH3 ⑩I2。
(1)其中由共价键形成的单质是
(2)NH3 的电子式是
①离子化合物只含有离子键
②只要有离子键的化合物就是离子化合物
③只要有共价键的物质就是共价化合物
④共价化合物只有共价键
⑤极性键不可能存在于离子化合物中
⑥金属元素与非金属元素之间只能形成离子键
⑦非金属元素与非金属元素之间只能形成共价键.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)下列7种化学符号: H、
H、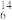 C、
C、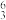 Li、
Li、 Mg、
Mg、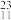 Na、
Na、 N、
N、 Li。其中表示核素的符号共
Li。其中表示核素的符号共_____ 种,互为同位素的是____ 和_____ ,中子数相等,但质子数不相等的核素是_____ 和_____ 。
(2)请选择下列物质中合适的物质直接填空:NaOH、氯化钡、氮气、CO2、H2O2、氯化铵。只含有离子键的有_____ (请用化学式填写,下同),既含有离子键又含有共价键的有_____ ,只含有极性键的有_____ ,含有非极性键的有_____ 。
(1)下列7种化学符号:
 H、
H、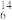 C、
C、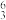 Li、
Li、 Mg、
Mg、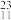 Na、
Na、 N、
N、 Li。其中表示核素的符号共
Li。其中表示核素的符号共(2)请选择下列物质中合适的物质直接填空:NaOH、氯化钡、氮气、CO2、H2O2、氯化铵。只含有离子键的有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
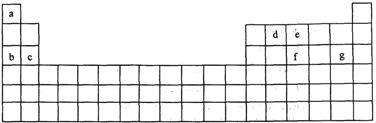
(1)元素的原子间反应最容易形成离子键的是下列中的( ) ,元素的原子间反应容易形成共价键的是下列中的( )
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是( ) 。
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为__________________ 。
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式_______ ,化学键类型为____ ,与稀盐酸反应的方程式为_____________________ .

(1)元素的原子间反应最容易形成离子键的是下列中的
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.下列是中学化学中熟悉的物质,请用序号完成下列问题
①O2②Na2O2③NH4Cl④HCl⑤NaOH⑥CaCl2⑦氦气
(1)这些物质中,只含共价键的是_______ 。只含离子键的是_______ 。既含共价键又含离子键的是_______ 。
(2)属于离子化合物的是_______ 。
II.已知拆开1 mol H﹣H键、1 mol I﹣I、1 mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1 mol HI需要_______ (填“放出”或“吸收”)_______ kJ的热量。
①O2②Na2O2③NH4Cl④HCl⑤NaOH⑥CaCl2⑦氦气
(1)这些物质中,只含共价键的是
(2)属于离子化合物的是
II.已知拆开1 mol H﹣H键、1 mol I﹣I、1 mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1 mol HI需要
您最近一年使用:0次



