用短线“−”表示共用电子对,用“∙∙”表示未成键孤电子对的式子叫路易斯结构式。R分子路易斯结构式可以表示为 ,下列叙述错误的是
,下列叙述错误的是
 ,下列叙述错误的是
,下列叙述错误的是| A.R可以是AsH3 | B.键角小于109°28' |
| C.R是由非极性键构成的极性分子 | D.R分子的中心原子为sp3杂化 |
更新时间:2022-04-21 22:01:04
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列化学用语的表达正确的是
A.氨气分子的比例模型 |
B.铍原子最外层的电子云图: |
| C.羰基硫(COS)的结构式O=C=S |
D.由H和Cl形成化学键的过程:H+Cl→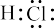 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列化学用语正确的是
| A.乙醇的结构简式:C2H6O |
B.HF的电子式: |
C.丙烷分子的球棍模型为:  |
| D.N2的结构式:∶N≡N∶ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】能说明BF3分子中四个原子在同一平面的理由是
| A.三个B―F键的键能相同 | B.B―F键是非极性共价键 |
| C.任意两个键的夹角为120° | D.三个B―F键的键长相等 |
您最近一年使用:0次
【推荐2】有关乙炔分子的说法中,错误的是
| A.所有原子在同一直线 | B.所有的化学键都是共价键 |
| C.碳碳叁键比碳碳单键活泼 | D.碳碳叁键的键能等于三个碳碳单键的键能之和 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】利用 可实现人工合成金刚石。下列关于该反应的说法错误的是
可实现人工合成金刚石。下列关于该反应的说法错误的是
 可实现人工合成金刚石。下列关于该反应的说法错误的是
可实现人工合成金刚石。下列关于该反应的说法错误的是| A.C(金刚石)属于共价晶体 |
| B.该反应利用了Na的强还原性 |
C.晶体硅和金刚石中的Si、C的杂化方式都是 |
D.NaCl晶体中每个 周围与它最接近且距离相等的 周围与它最接近且距离相等的 有12个 有12个 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】1865 年,提出苯的环状结构设想的科学家是
| A.居里夫人 | B.门捷列夫 | C.凯库勒 | D.阿伏加德罗 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】短周期元素W、X、Y和Z的原子序数依次增大。W是宇宙中最丰富的元素,W2X是维持生命过程的必需物质,WY可用于玻璃的刻蚀,ZX2是酸雨的主要形成原因之一,室温下化合物ZY4是气体。下列说法错误的是( )
| A.Y的第一电离能在四种元素中最大 |
| B.W2X和ZX2的中心原子分别为sp3和sp2杂化 |
| C.W2X2为极性分子 |
| D.ZY4分子中原子均为8电子结构 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法中正确的是( )
| A.含有非极性键的分子一定是非极性分子 |
| B.非极性分子中一定含有非极性键 |
| C.由极性键形成的双原子分子一定是极性分子 |
| D.两个原子之间共用两对电子,形成的化学键一定有极性 |
您最近一年使用:0次


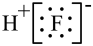
 的结构示意图:
的结构示意图: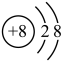
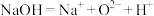
 是具有正四面体结构的非极性分子
是具有正四面体结构的非极性分子 杂化
杂化 溶液褪色
溶液褪色


