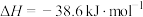如图为两种制备硫酸的途径(反应条件略)。下列说法不正确的是
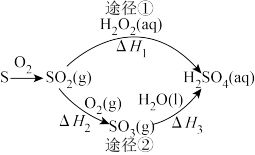

| A.途径①和途径②的反应热是不相等的 |
| B.含1molHCl的稀盐酸、含0.5molH2SO4的稀硫酸,分别与足量的NaOH溶液反应,二者放出的热量是相等的 |
| C.1molS(g)在空气中燃烧放出的热量大于1molS(s)在空气中燃烧放出的热量 |
| D.若△H1<△H2+△H3,则2H2O2(aq)=2H2O(1)+O2(g)为放热反应 |
更新时间:2022-04-24 22:05:25
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列有关能量的判断和表示方法正确的是( )
| A.由C(s,石墨)=C(s,金刚石)ΔH=+1.9kJ·mol-1,可知:石墨比金刚石更稳定 |
| B.等质量的C2H5OH(g)和C2H5OH(l)分别完全燃烧,后者放出的热量更多 |
| C.由H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1,可知:含1molCH3COOH的溶液与含1molNaOH的溶液混合,放出热量等于57.3kJ |
| D.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l)ΔH=-285.8kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列热化学方程式书写正确的是( )
| A.2NO2=2NO+O2△H=-184.6kJ/mol(反应热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=57.3kJ/mol(中和热) |
C.C(s)+ O2(g)=CO(g)△H=-184.6kJ/mol(燃烧热) O2(g)=CO(g)△H=-184.6kJ/mol(燃烧热) |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-893kJ/mol(燃烧热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
真题
名校
【推荐1】下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在生产和生活中,人们广泛利用着化学反应释放的能量。下列说法正确的是
| A.物质发生化学变化并不一定都伴随着能量变化 |
| B.应用盖斯定律可计算某些难以直接测量的反应焓变 |
| C.只要有能量变化的都是化学变化 |
| D.任何反应中的能量变化都表现为热量变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知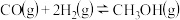 反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断错误的是
反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断错误的是
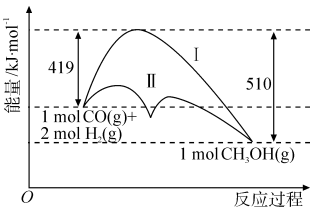
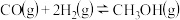 反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断错误的是
反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断错误的是
A.加入催化剂,该反应的 不变 不变 |
| B.加入催化剂,正、逆反应的活化能均减小 |
C.该反应的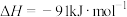 |
D.如果该反应生成液态 ,则 ,则 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列依据热化学方程式得出的结论正确的是
A.已知2SO2(g)+O2(g) 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)=C(金刚石,s) △H﹥0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH–(aq)=H2O(1) △H = -57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3kJ |
D.一定条件下2SO2(g)+O2(g)  2SO3(g) △H1 ,2SO2(g)+O2(g) 2SO3(g) △H1 ,2SO2(g)+O2(g)  2SO3(l) △H2 则△H1>△H2 2SO3(l) △H2 则△H1>△H2 |
您最近一年使用:0次

 在光照和点燃条件下的
在光照和点燃条件下的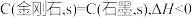 ,则石墨比金刚石稳定
,则石墨比金刚石稳定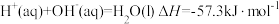 可知,稀醋酸与
可知,稀醋酸与 溶液反应生成
溶液反应生成 液态水时释放
液态水时释放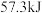 的热量
的热量 ,表示甲烷的燃烧热为
,表示甲烷的燃烧热为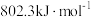
 下,
下,
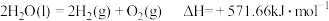
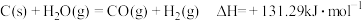
 ,则金刚石比石墨稳定
,则金刚石比石墨稳定
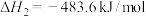 ,则
,则 的燃烧热为241.8kJ/mol
的燃烧热为241.8kJ/mol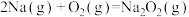
 ;
;
 ,则
,则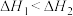
 和1.5mol
和1.5mol  置于密闭容器中充分反应生
置于密闭容器中充分反应生 (g),放热19.3kJ,其热化学方程式为
(g),放热19.3kJ,其热化学方程式为