在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示:
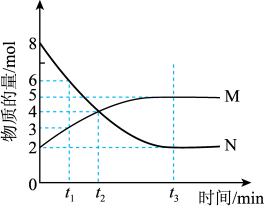
(1)该反应的化学方程式为____ 。
(2)t2时刻,正逆反应速率大小关系为V正____ V逆(填“>”、“=”、“<”) 。
(3)若t2=2min,计算反应开始至t2时刻,M的平均化学反应速率为:____ 。
(4)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
①前5min内A的转化率为____ 。
②化学方程式中n的值为____ 。

(1)该反应的化学方程式为
(2)t2时刻,正逆反应速率大小关系为V正
(3)若t2=2min,计算反应开始至t2时刻,M的平均化学反应速率为:
(4)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)
 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:①前5min内A的转化率为
②化学方程式中n的值为
更新时间:2022-04-27 14:38:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】在2L密闭容器内,800℃时发生反应:2NO(g)+O2(g)=2NO2(g),体系中NO物质的量n(NO)随时间的变化如下表:
(1)上述反应_______ (填“是"或“不是”)可逆反应。
(2)在第5s时,NO的转化率为_______ 。
(3)0-2s内,用O2表示反应的平均速率v(O2)=______ mol/(L·s)。
时间/(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)在第5s时,NO的转化率为
(3)0-2s内,用O2表示反应的平均速率v(O2)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某温度时,在一个2 L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。
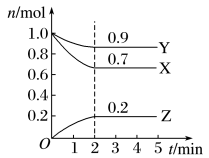
根据图中数据,试填写下列空白:
(1)该反应的化学方程式为________________________ 。
(2)从开始到2 min,Z的平均反应速率为_______________ ;
(3)平衡时,X的浓度为________ 。
(4)在第4 min时Z的消耗速率和生产速率____ (填>,=,<)
(5)下列叙述能说明该反应已达到化学平衡状态的是________ (填字母)。
A.体系总物质的质量不变化 B.同一时刻,X 与Y的反应速率相等
C.X的物质的量浓度不再发生变化 D.相同时间内Z的消耗速率等于生成速率

根据图中数据,试填写下列空白:
(1)该反应的化学方程式为
(2)从开始到2 min,Z的平均反应速率为
(3)平衡时,X的浓度为
(4)在第4 min时Z的消耗速率和生产速率
(5)下列叙述能说明该反应已达到化学平衡状态的是
A.体系总物质的质量不变化 B.同一时刻,X 与Y的反应速率相等
C.X的物质的量浓度不再发生变化 D.相同时间内Z的消耗速率等于生成速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g)  N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)写出上述反应的平衡常数表达式___________ 。
(2)在2L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
①结合表中数据,判断该反应的ΔH___________ 0(填“>”或“<”),理由是___________
②判断该反应达到平衡的依据是___________ 。
A.容器内气体密度恒定 B.容器内各气体浓度恒定
C.容器内压强恒定 D.2υ正(NO)= υ逆(N2)
(3)700℃时,若向2L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
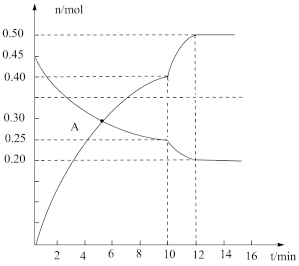
①0~10min内的CO2平均反应速率υ=___________ 。
②图中A点υ(正)___________ υ(逆)(填“>”“<”或“=”)。
③第10min时,外界改变的条件可能是___________ 。
A.加催化剂 B.增大C(s)的物质的量
C.减小CO2的物质的量 D.升温 E.降温
(4)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ∙mol−1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=−192.9 kJ∙mol−1
O2(g)=CO2(g)+2H2(g) ΔH=−192.9 kJ∙mol−1
又知③H2O(g)=H2O(l) ΔH=−44 kJ∙mol−1
则甲醇燃烧生成液态水的热化学方程式___________
 N2(g)+CO2(g)。
N2(g)+CO2(g)。(1)写出上述反应的平衡常数表达式
(2)在2L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
| 实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
| 1 | 700 | 0.40 | 0.09 |
| 2 | 800 | 0.24 | 0.08 |
①结合表中数据,判断该反应的ΔH
②判断该反应达到平衡的依据是
A.容器内气体密度恒定 B.容器内各气体浓度恒定
C.容器内压强恒定 D.2υ正(NO)= υ逆(N2)
(3)700℃时,若向2L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g)
 C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
①0~10min内的CO2平均反应速率υ=
②图中A点υ(正)
③第10min时,外界改变的条件可能是
A.加催化剂 B.增大C(s)的物质的量
C.减小CO2的物质的量 D.升温 E.降温
(4)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ∙mol−1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) ΔH=−192.9 kJ∙mol−1
O2(g)=CO2(g)+2H2(g) ΔH=−192.9 kJ∙mol−1又知③H2O(g)=H2O(l) ΔH=−44 kJ∙mol−1
则甲醇燃烧生成液态水的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如图表示800℃时,一个反应体系内A、B、C三种气体物质的浓度随时间变化的情况,t是反应时间。请回答:

(1)该反应的反应物是_______ 。
(2)该反应的化学方程式为_______ 。
(3)达到平衡状态的所需时间是2min,则该2min内A物质的平均反应速率为_______ 。

(1)该反应的反应物是
(2)该反应的化学方程式为
(3)达到平衡状态的所需时间是2min,则该2min内A物质的平均反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)对于反应:2SO2(g)+O2(g) 2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=
2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________________________ ;υ(SO3)=_______________________ 。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
(3)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______ 。
a、体系压强保持不变 b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变 d、每消耗1 mol SO3的同时生成1 mol NO
(1)对于反应:2SO2(g)+O2(g)
 2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=
2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=(2)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-12NO(g)+O2(g)
 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1则反应NO2(g)+SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=(3)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a、体系压强保持不变 b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变 d、每消耗1 mol SO3的同时生成1 mol NO
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】A与B反应生成C,假定反应由A、B开始,它们的初始浓度均为1.0mol·L-1。反应进行2min后A的浓度为0.8 mol·L-1,B的浓度为0.6 mol·L-1,C的浓度为0.6 mol·L-1。
⑴2min内的平均速率为V(A)=_________ ,V(B)=________ ,V(C)=________ ;
⑵V(A):V(B):V(C)=___________________ ;
⑶该反应的化学方程式为:_______________________________________ 。
⑴2min内的平均速率为V(A)=
⑵V(A):V(B):V(C)=
⑶该反应的化学方程式为:
您最近一年使用:0次



