工业上制取燃料气可以使用高温催化分解甲醇的方法,其反应原理为CH3OH(g) CO(g)+2H2(g),下列选项中表示该反应速率最快的是
CO(g)+2H2(g),下列选项中表示该反应速率最快的是
 CO(g)+2H2(g),下列选项中表示该反应速率最快的是
CO(g)+2H2(g),下列选项中表示该反应速率最快的是| A.v(CH3OH)=0.6 mol·L-1·s-1 | B.v(CO)=0.5 mol·L-1·s-1 |
| C.v(H2)=1 mol·L-1·s-1 | D.v(CH3OH)=24 mol·L-1·min-1 |
更新时间:2022-05-01 20:28:49
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在容积恒定的容器中发生反应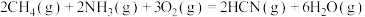 ,0~15 min内测得反应速率
,0~15 min内测得反应速率 ,下列叙述正确的是
,下列叙述正确的是
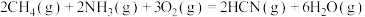 ,0~15 min内测得反应速率
,0~15 min内测得反应速率 ,下列叙述正确的是
,下列叙述正确的是| A.0~15 min内反应消耗氨气5.4 mol |
B.0~15 min内用 的浓度变化表示的反应速率 的浓度变化表示的反应速率 |
C.0~15 min内, |
D.15 min时氧气浓度下降到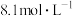 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将2molA和4molB在2L的密闭容器中混合,一定条件下发生反应: 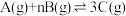 ,5min后测得A剩余0.8mol,B的平均反应速率为
,5min后测得A剩余0.8mol,B的平均反应速率为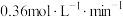 ,则n为
,则n为
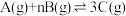 ,5min后测得A剩余0.8mol,B的平均反应速率为
,5min后测得A剩余0.8mol,B的平均反应速率为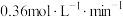 ,则n为
,则n为| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】反应4A(s)+3B(g)=2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L,对此反应速率的表示正确的是(s、g分别表示物质的状态为固体、气态)
| A.用A表示的反应速率为0.4 mol·L-1·min-1 |
| B.分别用B、C、D表示的反应速率其比值为1∶2∶3 |
| C.在2 min末的反应速率,用B表示是0.3 mol·L-1·min-1 |
| D.在这2 min内用D表示的反应速率是0.1 mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定条件下,反应4NH3(g)+5O2(g)⇋4NO(g)+6H2O(g)在5L密闭容器中进行,10s后 的物质的量增加了
的物质的量增加了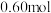 ,则10s内反应的速率
,则10s内反应的速率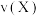 可表示为
可表示为
A. | B.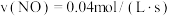 |
C.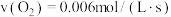 | D.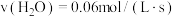 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】可逆反应2A(g)+3B(g)⇌3C(g)+D(g)在四种不同条件下的反应速率分别为:①v(A)=0.5mol·L-1·min-1;②v(B)=0.6mol·L-1·min-1;③v(C)=0.35mol·L-1·min-1;④v(D)=0.4mol·L-1·min-1。下列有关反应速率的比较中正确的是
| A.④>①>②>③ | B.④>①>③>② |
| C.①>②>③>④ | D.②>①>③>④ |
您最近一年使用:0次