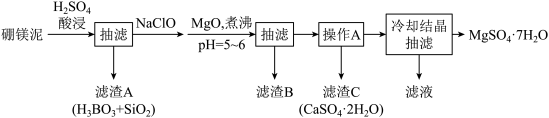
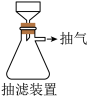
电镀废液中含有Cu2+、Mg2+、Ca2+、Ni2+和Fe3+,某专利申请用下列方法从该类废液中制备高纯度的铜粉。

已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
回答下列问题:
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥_______ (结果保留两位小数)。分离固液混合物时,需要用真空抽滤的方法提高过滤的速度和效果,其原因是_______ 。
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及其浓度相关,实验测得Cu2+与SO2反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
①由此可知,制备过程中进行电位检测时,要把溶液的氧化还原电位控制在_______ mV左右。
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是Cu2+直接被还原为Cu的原因是_______ 。反应生成Cu+的离子方程式是_______ 。
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有_______ 。为了使这些离子均除去,使水得到进一步的净化,应该在调节溶液pH使其他杂质离子沉淀后,再使Ca2+转化为_______ (填化学式)而除去。

已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
| Fe3+/Fe2+ | Cu2+/Cu+ | Cu2+/Cu |  /SO2 /SO2 | Fe2+/Fe | Ni2+/Ni | Mg2+/Mg | Ca2+/Ca |
| 0.77 | 0.52 | 0.34 | 0.17 | -0.44 | -0.23 | -2.38 | -2.76 |
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及其浓度相关,实验测得Cu2+与SO2反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
| 反应液的电位(mV) | 360 | 340 | 320 | 300 | 280 | 260 |
| 铜粉的回收率(%) | 86.5 | 90.2 | 95.6 | 97.2 | 97.3 | 97.4 |
| 产品的纯度(%) | 99.9 | 99.9 | 99.9 | 99.9 | 99.9 | 99.9 |
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是Cu2+直接被还原为Cu的原因是
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有
2022·河南·三模 查看更多[3]
河南省许昌济源平顶山2022届高三下学期第三次质量检测理科综合化学试题(已下线)第28讲 物质的分离、提纯和检验(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题十三水溶液中的离子平衡
更新时间:2022-05-03 17:19:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.盐类水解知识。
(1)氯化铁水溶液呈___________ 性,原因是用离子方程式表示:___________ ;把 溶液蒸干,灼烧,最后得到的主要固体产物是
溶液蒸干,灼烧,最后得到的主要固体产物是___________ ;普通泡沫灭火器是利用溶液跟溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是:___________ 。
Ⅱ.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(2)物质的量浓度均为 的四种溶液:pH
的四种溶液:pH由小到大 排列的顺序是___________ (用编号填写)
a. b.
b. c.NaClO d.
c.NaClO d.
(3)常温下,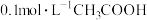 溶液加水稀释过程中,下列表达式的数据
溶液加水稀释过程中,下列表达式的数据变大 的是___________
A. B.
B. C.
C. D.
D. E.
E.
(4)25℃时,将 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为___________ 。
(1)氯化铁水溶液呈
 溶液蒸干,灼烧,最后得到的主要固体产物是
溶液蒸干,灼烧,最后得到的主要固体产物是Ⅱ.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
| 化学式 |  |  | HClO |
| 电离平衡常数 |  |   |  |
 的四种溶液:pH
的四种溶液:pHa.
 b.
b. c.NaClO d.
c.NaClO d.
(3)常温下,
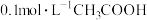 溶液加水稀释过程中,下列表达式的数据
溶液加水稀释过程中,下列表达式的数据A.
 B.
B. C.
C. D.
D. E.
E.
(4)25℃时,将
 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.回答下列问题:
(1) 溶液蒸干得到的固体物质是
溶液蒸干得到的固体物质是_______ ,原因是_______ 。
(2) 溶液蒸干灼烧得到的固体物质是
溶液蒸干灼烧得到的固体物质是_______ ,原因是_______ 。
(3)将 的
的 溶液加热蒸干灼烧最后所得的固体是
溶液加热蒸干灼烧最后所得的固体是_______ ,原因是_______ 。
Ⅱ. 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。请回答下列问题:
高效,且腐蚀性小。请回答下列问题:
 在溶液中分三步水解:
在溶液中分三步水解:
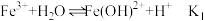

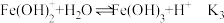
(4)以上水解反应的平衡常数 由大到小的顺序是
由大到小的顺序是_______ 。通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为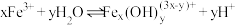 。欲使平衡正向移动可采用的方法是
。欲使平衡正向移动可采用的方法是_______ (填字母)。
a.降温 b.加水稀释 c.加入 d.加入
d.加入
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是_______ 。
(1)
 溶液蒸干得到的固体物质是
溶液蒸干得到的固体物质是(2)
 溶液蒸干灼烧得到的固体物质是
溶液蒸干灼烧得到的固体物质是(3)将
 的
的 溶液加热蒸干灼烧最后所得的固体是
溶液加热蒸干灼烧最后所得的固体是Ⅱ.
 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。请回答下列问题:
高效,且腐蚀性小。请回答下列问题: 在溶液中分三步水解:
在溶液中分三步水解: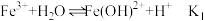

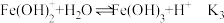
(4)以上水解反应的平衡常数
 由大到小的顺序是
由大到小的顺序是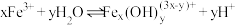 。欲使平衡正向移动可采用的方法是
。欲使平衡正向移动可采用的方法是a.降温 b.加水稀释 c.加入
 d.加入
d.加入
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)明矾可用于净水,原因是(用离子方程式表示):___________ ,把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是___________ 。
(2)用离子方程式表示泡沫灭火器灭火原理:___________ 。
(3)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示):___________ 。
(4)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入MgCO3固体,过滤后再加入足量盐酸。MgCO3固体能除去Fe3+的原因是___________ 。
(2)用离子方程式表示泡沫灭火器灭火原理:
(3)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示):
(4)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入MgCO3固体,过滤后再加入足量盐酸。MgCO3固体能除去Fe3+的原因是
您最近一年使用:0次
【推荐1】“绿水青山就是金山银山”已成为各地的标牌。
(1)硫酸工业排出的尾气(主要含SO2)有多种处理方式
①下列物质中可以吸收硫酸工业尾气的是___
a.饱和Na2SO3溶液 b.饱和NaCl溶液 c.稀H2SO4 d.浓氨水
②硫酸工业排出的尾气也可用软锰矿浆(主要成分为MnO2)吸收,生成MnSO4,写出反应的化学方程式___ 。
(2)治理汽车尾气中NO和CO的方法之一是在汽车的排气管上装一个催化转化装置,使NO和CO在催化剂作用下转化为无毒物质。写出该反应的化学方程式:___ 。
(3)用NaOH溶液亦可以吸收废气中的氮氧化物,化学方程式如下NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O
①上述两反应中分别消耗等量的NO2时,转移电子的物质的量之比为___ 。
②标准状况下5.6L混合气体(只有NO、NO2)被0.5mol•L﹣1NaOH溶液完全吸收,至少需要NaOH溶液的体积为___ L。
(1)硫酸工业排出的尾气(主要含SO2)有多种处理方式
①下列物质中可以吸收硫酸工业尾气的是
a.饱和Na2SO3溶液 b.饱和NaCl溶液 c.稀H2SO4 d.浓氨水
②硫酸工业排出的尾气也可用软锰矿浆(主要成分为MnO2)吸收,生成MnSO4,写出反应的化学方程式
(2)治理汽车尾气中NO和CO的方法之一是在汽车的排气管上装一个催化转化装置,使NO和CO在催化剂作用下转化为无毒物质。写出该反应的化学方程式:
(3)用NaOH溶液亦可以吸收废气中的氮氧化物,化学方程式如下NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O
①上述两反应中分别消耗等量的NO2时,转移电子的物质的量之比为
②标准状况下5.6L混合气体(只有NO、NO2)被0.5mol•L﹣1NaOH溶液完全吸收,至少需要NaOH溶液的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气是一种重要的化工原料。
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:________________________ ;氢气在氯气的燃烧观察的现象为:___________________ 。
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的CO2和H2O而失效,漂白粉失效过程的化学反应方程式为:_______________________________ 。
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空a、b、c、d中重合部分代表物质间反应,且氯水足量 。
。
①c过程的离子方程式_______________________________________________________ ,e过程中的化学方程式为 _____________________________________________________ 。
②d过程所观察到的现象为:___________________________________________________ 。b过程证明了氯水中存在______ 微粒。(填序号)
a.Cl2 b.Cl- c.HClO d.H+
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的CO2和H2O而失效,漂白粉失效过程的化学反应方程式为:
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空a、b、c、d中重合部分代表物质间反应,且氯水足量
 。
。
①c过程的离子方程式
②d过程所观察到的现象为:
a.Cl2 b.Cl- c.HClO d.H+
您最近一年使用:0次