Ⅰ.氮及其化合物在生产生活中应用广泛,工业上制硝酸的关键一步便是 的催化氧化,可用下图装置模拟
的催化氧化,可用下图装置模拟 的催化氧化,回答下列问题:
的催化氧化,回答下列问题:
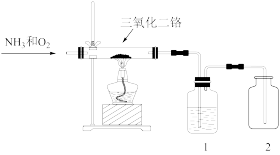
(1)玻璃管中发生反应的化学方程式是_______ ,停止加热后玻璃管内仍能保持红热,该反应是_______ 反应(填“吸热”或“放热”)。
(2)为保证在装置2中观察到红棕色气体,装置1应装入_______ ,作用是_______ 。
Ⅱ.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。

(3)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_______ (填图中数字序号)。
(4)下列关于海洋氮循环的说法正确的是_______ (填字母序号)。
a.海洋中的氮循环起始于氮的氧化
b.海洋中存在游离态的氮
c.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
d.海洋中的反硝化作用一定有氧气的参与
(5)有氧时,在硝化细菌作用下, 可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:
可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:_______ 。
 的催化氧化,可用下图装置模拟
的催化氧化,可用下图装置模拟 的催化氧化,回答下列问题:
的催化氧化,回答下列问题:
(1)玻璃管中发生反应的化学方程式是
(2)为保证在装置2中观察到红棕色气体,装置1应装入
Ⅱ.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。

(3)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(4)下列关于海洋氮循环的说法正确的是
a.海洋中的氮循环起始于氮的氧化
b.海洋中存在游离态的氮
c.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量d.海洋中的反硝化作用一定有氧气的参与
(5)有氧时,在硝化细菌作用下,
 可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:
可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:
更新时间:2022-05-07 08:18:59
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物与工农业生产、生活具有密切关系。
(1)下列变化属于“氮的固定”的是_______(填字母)。
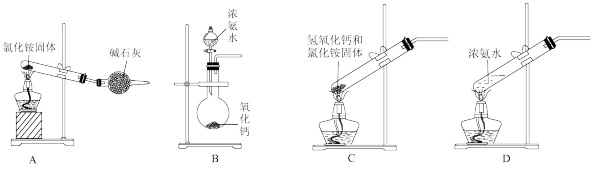
(2)如图是实验室制取氨气的装置和选用的试剂,其中不正确的是_______ (填字母)。
(3) 是常用的铵态氮肥,检验铵态氮肥中是否含有
是常用的铵态氮肥,检验铵态氮肥中是否含有 的方法是
的方法是_______ (写出实验操作、现象及结论)。
(4)治理 通常是在氧化剂作用下,将
通常是在氧化剂作用下,将 氧化成
氧化成 ,然后用水或碱液吸收脱氮。下列物质可用于氧化
,然后用水或碱液吸收脱氮。下列物质可用于氧化 的是
的是_______ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
若用 溶液氧化
溶液氧化 ,写出该反应的化学方程式并用双线桥法标出反应中电子转移的方向和数目
,写出该反应的化学方程式并用双线桥法标出反应中电子转移的方向和数目_______ 。
(5)用尿素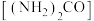 水溶液吸收氮氧化物也是一种可行的方法。将
水溶液吸收氮氧化物也是一种可行的方法。将 和
和 不同配比的混合气通入尿素溶液中,总氮还原率与配比关系如图。
不同配比的混合气通入尿素溶液中,总氮还原率与配比关系如图。

①用尿素水溶液吸收体积比为1∶1的 和
和 混合气,可将N元素转变为对环境无害的气体,发生反应的化学方程式为
混合气,可将N元素转变为对环境无害的气体,发生反应的化学方程式为_______ 。
②随着 和
和 配比的提高,总氮还原率降低的主要原因是
配比的提高,总氮还原率降低的主要原因是_______ 。
(1)下列变化属于“氮的固定”的是_______(填字母)。
| A.植物从土壤中吸收氮肥 |
| B.硝酸和氨气反应生成氮肥 |
| C.将空气中的氮气转变为氮的化合物 |
| D.大豆的根瘤菌将含氮的化合物转变为植物蛋白质 |

(3)
 是常用的铵态氮肥,检验铵态氮肥中是否含有
是常用的铵态氮肥,检验铵态氮肥中是否含有 的方法是
的方法是(4)治理
 通常是在氧化剂作用下,将
通常是在氧化剂作用下,将 氧化成
氧化成 ,然后用水或碱液吸收脱氮。下列物质可用于氧化
,然后用水或碱液吸收脱氮。下列物质可用于氧化 的是
的是A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液若用
 溶液氧化
溶液氧化 ,写出该反应的化学方程式并用双线桥法标出反应中电子转移的方向和数目
,写出该反应的化学方程式并用双线桥法标出反应中电子转移的方向和数目(5)用尿素
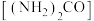 水溶液吸收氮氧化物也是一种可行的方法。将
水溶液吸收氮氧化物也是一种可行的方法。将 和
和 不同配比的混合气通入尿素溶液中,总氮还原率与配比关系如图。
不同配比的混合气通入尿素溶液中,总氮还原率与配比关系如图。
①用尿素水溶液吸收体积比为1∶1的
 和
和 混合气,可将N元素转变为对环境无害的气体,发生反应的化学方程式为
混合气,可将N元素转变为对环境无害的气体,发生反应的化学方程式为②随着
 和
和 配比的提高,总氮还原率降低的主要原因是
配比的提高,总氮还原率降低的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。
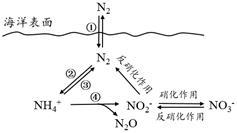
(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_______ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是__________ (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3-的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
________ NH4++ 5O2=2NO2-+ ________ H++__________ +__________
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本的监测数据:
硝化细菌去除氨氮的最佳反应温度是_____________ ,在最佳反应温度时,48 h内去除氨氮反应的平均速率是____________ mg·L-1·h-1。
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH4+)的示意图。
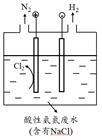
① 结合电极反应式简述间接氧化法去除氨氮的原理:_______________ 。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将___________ (填“增大”、“不变”或“减小”),请简述理由:_______________ 。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3-的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本的监测数据:
| 温度/℃ | 样本氨氮含量/mg | 处理24 h | 处理48 h |
| 氨氮含量/mg | 氨氮含量/mg | ||
| 20 | 1008 | 838 | 788 |
| 25 | 1008 | 757 | 468 |
| 30 | 1008 | 798 | 600 |
| 40 | 1008 | 977 | 910 |
硝化细菌去除氨氮的最佳反应温度是
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH4+)的示意图。

① 结合电极反应式简述间接氧化法去除氨氮的原理:
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】研究氮及其化合物在自然界中的循环对于生产生活意义重大。自然界中氮的循环示意图如下所示。
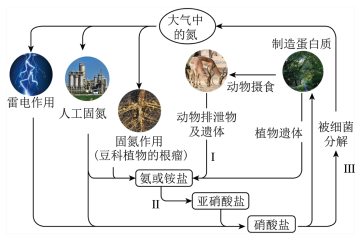
(1)农村有句谚语叫“雷雨肥庄稼”,体现了氮循环的部分过程,有关反应的化学方程式是________ 。
(2)尿素[CO(NH2)2]是过程Ⅰ的排泄物,其最终能水解为NH3和________ 。
(3)在农田土壤中,过程Ⅱ、Ⅲ涉及的变化示意如下:
硝化作用:
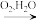

反硝化作用:
 N2
N2
①硝化作用中 的“O”部分来自O2、部分来自H2O,确认两种“O”在
的“O”部分来自O2、部分来自H2O,确认两种“O”在 中所占比例大小的方法是
中所占比例大小的方法是_________ 。
②以CH3OH为碳源能有效促进反硝化作用,CH3OH的主要作用是________ (填“提供电子”或“接受电子”)。
(4)水中氮、磷过多,造成水中藻类疯长,消耗溶解氧,水质恶化。化学耗氧量(COD)能衡量水体受污染的程度,它是指用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的量(O)/(mg·L-1)来表示。其测量过程如下所示:

①不能用盐酸酸化水样,原因是___________ 。
②“滴定”的反应如下,将其补充完整:_____ ,__ +__
+__ +___=___CO2↑+___Mn2++___。
+___=___CO2↑+___Mn2++___。
③经数据处理,氧化100mL水样消耗 a mol KMnO4,则该水样的COD的值为______ mg·L-1。

(1)农村有句谚语叫“雷雨肥庄稼”,体现了氮循环的部分过程,有关反应的化学方程式是
(2)尿素[CO(NH2)2]是过程Ⅰ的排泄物,其最终能水解为NH3和
(3)在农田土壤中,过程Ⅱ、Ⅲ涉及的变化示意如下:
硝化作用:


反硝化作用:

 N2
N2①硝化作用中
 的“O”部分来自O2、部分来自H2O,确认两种“O”在
的“O”部分来自O2、部分来自H2O,确认两种“O”在 中所占比例大小的方法是
中所占比例大小的方法是②以CH3OH为碳源能有效促进反硝化作用,CH3OH的主要作用是
(4)水中氮、磷过多,造成水中藻类疯长,消耗溶解氧,水质恶化。化学耗氧量(COD)能衡量水体受污染的程度,它是指用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的量(O)/(mg·L-1)来表示。其测量过程如下所示:

①不能用盐酸酸化水样,原因是
②“滴定”的反应如下,将其补充完整:
 +__
+__ +___=___CO2↑+___Mn2++___。
+___=___CO2↑+___Mn2++___。③经数据处理,氧化100mL水样消耗 a mol KMnO4,则该水样的COD的值为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。

请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则反应②的离子方程式是________________________ 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为________________________________ 。
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为______________ 。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:________________ 。

请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则反应②的离子方程式是
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系图如下。
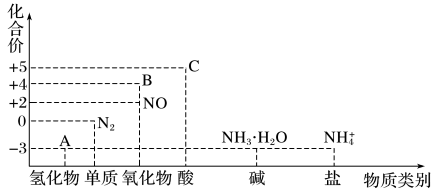
回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,该化学方程式是_______ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______ 。
(3)实验室中,检验溶液中含有 的操作方法是
的操作方法是_______ , 的电子式为
的电子式为_______ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______ 。当反应消耗3.36 L(标准状况)物质B时,转移电子的物质的量为_______ mol。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,该化学方程式是
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有
 的操作方法是
的操作方法是 的电子式为
的电子式为(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、D、E、X均为中学化学常见物质,相互转化关系如图所示(部分物质略去)。
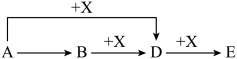
已知A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)B的电子式为:___________ ,实验室制取B的化学方程式为___________ 。
(2)D、E都是大气污染物,它们对环境造成的危害表现在___________ (填序号)。
a.引起酸雨 b.引起温室效应 c.形成光化学烟雾 d.引起水体富营养化
(3)为避免D、E等污染气体对环境造成影响,降低污染物排放,写出B与D反应的化学方程式:___________ 。
(4)E尾气可使用碱性的 溶液吸收,请写出相关反应的化学方程式
溶液吸收,请写出相关反应的化学方程式___________ 。
(5)在标准状况下进行如下反应,将一定量的铜粉投入一定量浓 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由 、
、 、
、 等组成的含氮混合气体,这些混合气体与11.2L氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
等组成的含氮混合气体,这些混合气体与11.2L氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为________ mol。
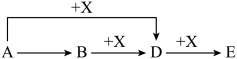
已知A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)B的电子式为:
(2)D、E都是大气污染物,它们对环境造成的危害表现在
a.引起酸雨 b.引起温室效应 c.形成光化学烟雾 d.引起水体富营养化
(3)为避免D、E等污染气体对环境造成影响,降低污染物排放,写出B与D反应的化学方程式:
(4)E尾气可使用碱性的
 溶液吸收,请写出相关反应的化学方程式
溶液吸收,请写出相关反应的化学方程式(5)在标准状况下进行如下反应,将一定量的铜粉投入一定量浓
 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后,收集到由 、
、 、
、 等组成的含氮混合气体,这些混合气体与11.2L氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
等组成的含氮混合气体,这些混合气体与11.2L氧气反应后通入水中完全转化为硝酸,则参加反应的铜的物质的量为
您最近一年使用:0次



