研究氮及其化合物在自然界中的循环对于生产生活意义重大。自然界中氮的循环示意图如下所示。
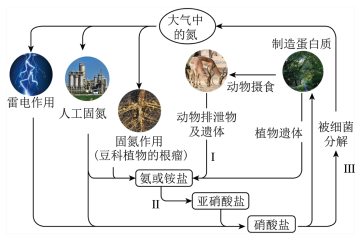
(1)农村有句谚语叫“雷雨肥庄稼”,体现了氮循环的部分过程,有关反应的化学方程式是________ 。
(2)尿素[CO(NH2)2]是过程Ⅰ的排泄物,其最终能水解为NH3和________ 。
(3)在农田土壤中,过程Ⅱ、Ⅲ涉及的变化示意如下:
硝化作用:

反硝化作用:
 N2
N2
①硝化作用中 的“O”部分来自O2、部分来自H2O,确认两种“O”在
的“O”部分来自O2、部分来自H2O,确认两种“O”在 中所占比例大小的方法是
中所占比例大小的方法是_________ 。
②以CH3OH为碳源能有效促进反硝化作用,CH3OH的主要作用是________ (填“提供电子”或“接受电子”)。
(4)水中氮、磷过多,造成水中藻类疯长,消耗溶解氧,水质恶化。化学耗氧量(COD)能衡量水体受污染的程度,它是指用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的量(O)/(mg·L-1)来表示。其测量过程如下所示:

①不能用盐酸酸化水样,原因是___________ 。
②“滴定”的反应如下,将其补充完整:_____ ,__ +__
+__ +___=___CO2↑+___Mn2++___。
+___=___CO2↑+___Mn2++___。
③经数据处理,氧化100mL水样消耗 a mol KMnO4,则该水样的COD的值为______ mg·L-1。

(1)农村有句谚语叫“雷雨肥庄稼”,体现了氮循环的部分过程,有关反应的化学方程式是
(2)尿素[CO(NH2)2]是过程Ⅰ的排泄物,其最终能水解为NH3和
(3)在农田土壤中,过程Ⅱ、Ⅲ涉及的变化示意如下:
硝化作用:


反硝化作用:

 N2
N2①硝化作用中
 的“O”部分来自O2、部分来自H2O,确认两种“O”在
的“O”部分来自O2、部分来自H2O,确认两种“O”在 中所占比例大小的方法是
中所占比例大小的方法是②以CH3OH为碳源能有效促进反硝化作用,CH3OH的主要作用是
(4)水中氮、磷过多,造成水中藻类疯长,消耗溶解氧,水质恶化。化学耗氧量(COD)能衡量水体受污染的程度,它是指用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的量(O)/(mg·L-1)来表示。其测量过程如下所示:

①不能用盐酸酸化水样,原因是
②“滴定”的反应如下,将其补充完整:
 +__
+__ +___=___CO2↑+___Mn2++___。
+___=___CO2↑+___Mn2++___。③经数据处理,氧化100mL水样消耗 a mol KMnO4,则该水样的COD的值为
更新时间:2024-03-15 09:46:25
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:___ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是___ (填字母)。
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
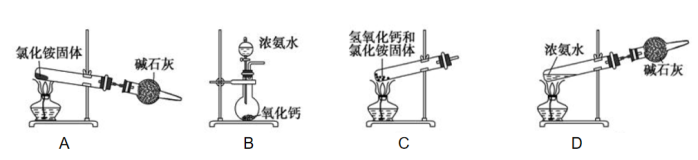
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是___ (填字母)。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验 的方法是
的方法是___ 。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是

(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验
 的方法是
的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】已知氮元素及其化合物的转化关系如下图所示,回答下列问题。
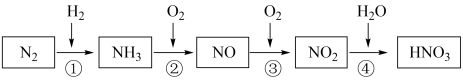
(1)①~④各步转化中,属于氮的固定的是_______ (填序号)。
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是_______ 。
②干燥氨气不可选用的试剂是_______ (填字母)。
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)工业制硝酸时尾气中含有NO、 ,可用以下方法吸收:
,可用以下方法吸收:
①水吸收法。结合化学方程式说明用水吸收 的缺陷
的缺陷_______ 。
②NaOH溶液吸收法。发生的反应有: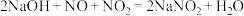 ,
,
_______ 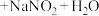 (填化学式,不需要配平方程式)。
(填化学式,不需要配平方程式)。______
③用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如下图:
含量不同的尾气,关系如下图:

(α表示尾气里NO、 中
中 的含量)
的含量)
i.根据上图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______

(1)①~④各步转化中,属于氮的固定的是
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是
②干燥氨气不可选用的试剂是
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)工业制硝酸时尾气中含有NO、
 ,可用以下方法吸收:
,可用以下方法吸收:①水吸收法。结合化学方程式说明用水吸收
 的缺陷
的缺陷②NaOH溶液吸收法。发生的反应有:
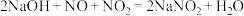 ,
,
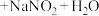 (填化学式,不需要配平方程式)。
(填化学式,不需要配平方程式)。③用不同浓度的NaOH溶液吸收
 含量不同的尾气,关系如下图:
含量不同的尾气,关系如下图:
(α表示尾气里NO、
 中
中 的含量)
的含量)i.根据上图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大ii.当α小于50%时,加入
 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是
您最近一年使用:0次
【推荐3】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_____ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是_____ (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量
(3)有氧时,在硝化细菌作用下,NH 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+
____________________________________________________________
(4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH )示意图。
)示意图。

①结合电极反应式简述间接氧化法去除氨氮的原理:_____ 。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将______ 填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量(3)有氧时,在硝化细菌作用下,NH
 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+ (4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH
 )示意图。
)示意图。
①结合电极反应式简述间接氧化法去除氨氮的原理:
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某探究小组模拟制备三氯乙醛(CCl3CHO)的实验装置如图(夹持、加热装置均已略去)。
Ⅰ.制备原理: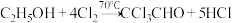 。
。
可能发生的副反应:ⅰ. ;
;
ⅱ.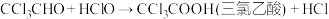 。
。
Ⅱ.相关物质的相对分子质量及部分物理性质如表所示:
回答下列问题:
(1)装置A中发生反应的离子方程式为______ ,仪器m中水流的出口为______ (填“a”或“b”)。
(2)装置B中盛装的试剂为饱和食盐水,若撤去装置C,会导致CCl3CHO的产率降低,试分析可能原因:______ 。
(3)装置D处宜采用的加热方法为______ (填“直接加热”或“水浴加热”);若实验结束后装置E中溶液含有的含氯元素的阴离子仅有ClO-和X,检验阴离子X的方法为______ 。
(4)称取0.40g制得的产品,配成待测溶液,向待测液中加入适量NaOH溶液,再用滴定管向待测溶液中加入30.00mL 碘标准溶液,使反应
碘标准溶液,使反应 ,
, 充分进行。完全反应后,加盐酸调节溶液的pH,加入淀粉溶液作指示剂,并立即用
充分进行。完全反应后,加盐酸调节溶液的pH,加入淀粉溶液作指示剂,并立即用 的Na2S2O3溶液滴定过量的I2至终点,发生反应:
的Na2S2O3溶液滴定过量的I2至终点,发生反应: 。
。
重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。
①取用碘标准溶液和Na2S2O3溶液所用滴定管分别为______ (填标号)。
a.酸式滴定管、酸式滴定管 b.碱式滴定管、碱式滴定管
c.酸式滴定管、碱式滴定管 d.碱式滴定管、酸式滴定管
②实验到达滴定终点的现象是______ ,测得产品的纯度为______ (保留三位有效数字)。
③若取用碘标准溶液的滴定管用蒸馏水洗净后没有用碘标准溶液润洗,则测定结果将______ (填“偏大”“偏小”或“不变”)。

Ⅰ.制备原理:
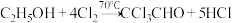 。
。可能发生的副反应:ⅰ.
 ;
;ⅱ.
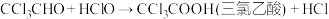 。
。Ⅱ.相关物质的相对分子质量及部分物理性质如表所示:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)装置A中发生反应的离子方程式为
(2)装置B中盛装的试剂为饱和食盐水,若撤去装置C,会导致CCl3CHO的产率降低,试分析可能原因:
(3)装置D处宜采用的加热方法为
(4)称取0.40g制得的产品,配成待测溶液,向待测液中加入适量NaOH溶液,再用滴定管向待测溶液中加入30.00mL
 碘标准溶液,使反应
碘标准溶液,使反应 ,
, 充分进行。完全反应后,加盐酸调节溶液的pH,加入淀粉溶液作指示剂,并立即用
充分进行。完全反应后,加盐酸调节溶液的pH,加入淀粉溶液作指示剂,并立即用 的Na2S2O3溶液滴定过量的I2至终点,发生反应:
的Na2S2O3溶液滴定过量的I2至终点,发生反应: 。
。重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。
①取用碘标准溶液和Na2S2O3溶液所用滴定管分别为
a.酸式滴定管、酸式滴定管 b.碱式滴定管、碱式滴定管
c.酸式滴定管、碱式滴定管 d.碱式滴定管、酸式滴定管
②实验到达滴定终点的现象是
③若取用碘标准溶液的滴定管用蒸馏水洗净后没有用碘标准溶液润洗,则测定结果将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】苯甲酸可用于医药、染料载体、增塑剂、果汁饮料的保香剂和食品防腐剂等的生产。某化学兴趣小组欲在实验室制备苯甲酸、回收二氧化锰并测定其纯度,进行如下实验(实验装置如下图所示)。

已知:①苯甲酸实验室制备原理为:

②甲苯的密度是0.872 g / mL;苯甲酸微溶于冷水,溶于热水。
实验步骤:
I.在50mL三颈烧瓶中加入1.5mL甲苯、20mL水和5.0g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1, 滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,得到滤渣2;将滤液处理后得到苯甲酸晶体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中, 加热灼烧,所得固体与干燥后的滤渣1合并,称重得2.5g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5g回收的二氧化锰,放于烧杯中,再加入25.00mL 0.4 mol/L草酸钠溶液及足量稀硫酸,加热至二氧化碳不再产生,将反应后溶液稀释至100 mL,量取20.00mL于锥形瓶中,用0.0200mol/L的高锰酸钾标准液滴定,平行滴定3次,平均消耗高锰酸钾标准液20.00mL。
已知:MnO2 + C2O + 4H+ = Mn2+ + 2CO2↑+ 2H2O
+ 4H+ = Mn2+ + 2CO2↑+ 2H2O
2MnO + 5C2O
+ 5C2O +16H+ = 2Mn2++10CO2↑+ 8H2O
+16H+ = 2Mn2++10CO2↑+ 8H2O
回答下列问题:
(1)仪器A的名称为_______ 。该装置的作用是_______ 。
(2)步骤I中甲苯与KMnO4反应生成苯甲酸钾、二氧化锰,写出反应方程式_______ 。
(3)步骤I中,判断反应结束的现象是_______ 。
(4)补齐步骤Ⅱ中处理滤液获得到纯苯甲酸晶体的实验方案:将滤液转入烧杯中,________ (供选用的试剂与用品有:稀硫酸、稀盐酸、BaCl2溶液、pH试纸、蒸馏水、冰水混合液)。
(5)用高锰酸钾标准液滴定时,滴定终点的现象是_______ 。
(6)列式计算二氧化锰的纯度______ 。

已知:①苯甲酸实验室制备原理为:

②甲苯的密度是0.872 g / mL;苯甲酸微溶于冷水,溶于热水。
实验步骤:
I.在50mL三颈烧瓶中加入1.5mL甲苯、20mL水和5.0g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1, 滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,得到滤渣2;将滤液处理后得到苯甲酸晶体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中, 加热灼烧,所得固体与干燥后的滤渣1合并,称重得2.5g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5g回收的二氧化锰,放于烧杯中,再加入25.00mL 0.4 mol/L草酸钠溶液及足量稀硫酸,加热至二氧化碳不再产生,将反应后溶液稀释至100 mL,量取20.00mL于锥形瓶中,用0.0200mol/L的高锰酸钾标准液滴定,平行滴定3次,平均消耗高锰酸钾标准液20.00mL。
已知:MnO2 + C2O
 + 4H+ = Mn2+ + 2CO2↑+ 2H2O
+ 4H+ = Mn2+ + 2CO2↑+ 2H2O2MnO
 + 5C2O
+ 5C2O +16H+ = 2Mn2++10CO2↑+ 8H2O
+16H+ = 2Mn2++10CO2↑+ 8H2O回答下列问题:
(1)仪器A的名称为
(2)步骤I中甲苯与KMnO4反应生成苯甲酸钾、二氧化锰,写出反应方程式
(3)步骤I中,判断反应结束的现象是
(4)补齐步骤Ⅱ中处理滤液获得到纯苯甲酸晶体的实验方案:将滤液转入烧杯中,
(5)用高锰酸钾标准液滴定时,滴定终点的现象是
(6)列式计算二氧化锰的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酰硫酸( ,
, )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
ⅱ.实验室制备亚硝酰硫酸的原理为 ,
,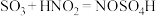 。
。
(1)仪器Ⅰ的名称为______ ,按照气流从左到右的顺序,上述仪器的连接顺序为______ (填仪器接口的字母,字母之间用“→”连接,部分仪器可以重复使用)。
(2)为了控制通入B中的 的通入速率,可以采取的措施是
的通入速率,可以采取的措施是______ 。
(3)装置B中三颈烧瓶需置于冷水浴中并维持反应体系温度不得高于20℃,若装置B中温度过高将导致产品产率降低,可能的原因是______ (任写一个原因即可得分)。
(4)装置C的作用为防止亚硝酰硫酸遇水反应,请写出亚硝酰硫酸与水反应化学方程式______ 。
(5)测定亚硝酰硫酸的纯度:
步骤①:准确称取25.4g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL溶液于锥形瓶中,加入60.00mL未知浓度 溶液(过量)和10.00mL25%的
溶液(过量)和10.00mL25%的 溶液,摇匀,发生反应
溶液,摇匀,发生反应
步骤③:向该溶液中滴加 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为20.00mL。
溶液的体积为20.00mL。
步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗 溶液的体积为60.00mL。滴定终点时的现象为
溶液的体积为60.00mL。滴定终点时的现象为______ ,亚硝酰硫酸的纯度为______ (精确到0.1%)。
 ,
, )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
ⅱ.实验室制备亚硝酰硫酸的原理为
 ,
,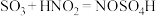 。
。(1)仪器Ⅰ的名称为
(2)为了控制通入B中的
 的通入速率,可以采取的措施是
的通入速率,可以采取的措施是(3)装置B中三颈烧瓶需置于冷水浴中并维持反应体系温度不得高于20℃,若装置B中温度过高将导致产品产率降低,可能的原因是
(4)装置C的作用为防止亚硝酰硫酸遇水反应,请写出亚硝酰硫酸与水反应化学方程式
(5)测定亚硝酰硫酸的纯度:
步骤①:准确称取25.4g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL溶液于锥形瓶中,加入60.00mL未知浓度
 溶液(过量)和10.00mL25%的
溶液(过量)和10.00mL25%的 溶液,摇匀,发生反应
溶液,摇匀,发生反应
步骤③:向该溶液中滴加
 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为20.00mL。
溶液的体积为20.00mL。步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗
 溶液的体积为60.00mL。滴定终点时的现象为
溶液的体积为60.00mL。滴定终点时的现象为
您最近一年使用:0次



