氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:___ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是___ (填字母)。
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
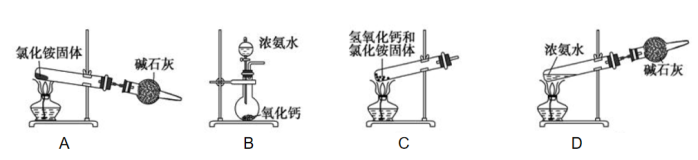
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是___ (填字母)。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验 的方法是
的方法是___ 。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是

(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验
 的方法是
的方法是
更新时间:2021-04-01 22:01:14
|
相似题推荐
【推荐1】如图所示的氮循环是生态系统物质循环的重要组成部分,人类活动加剧了氮循环中的物质转化。
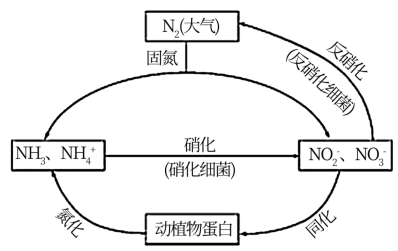
(1)结合上图判断下列说法正确的是____________ (填字母序号)。
A 固氮过程中,N2只作氧化剂
B 在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C 反硝化过程有助于弥补人工固氮对氮循环造成的影响
D 同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的化学方程式为____________ 。
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:
5CH3OH+6NO

____ N2↑+4HCO +
+_____ +______ 。
(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:____________
(5)已知,氨气易液化,可做制冷剂,试比较NH3的沸点______ (选填“高于”或“低于”)PH3,原因是_______________________ 。
(6)已知:①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H1= -a kJ/mol
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2= -bkJ/mol;
③H2(g)+ O2(g)=H2O(g) △H3= -c kJ/mol
O2(g)=H2O(g) △H3= -c kJ/mol
④H2(g)+ O2(g)=H2O(l) △H4= -d kJ/mol
O2(g)=H2O(l) △H4= -d kJ/mol
有关下列叙述不正确的是_____________ 。
a.由上述热化学方程式可知△H3<△H4
b.H2的燃烧热为d kJ/mol
c.4NH3(g)+4O2(g)=2NO(g)+N2(g)+6H2O(g) △H=(-a-b) kJ/mol
d.4NH3(g) 2N2(g)+6H2(g) △H =(6d-b)kJ/mol
2N2(g)+6H2(g) △H =(6d-b)kJ/mol

(1)结合上图判断下列说法正确的是
A 固氮过程中,N2只作氧化剂
B 在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C 反硝化过程有助于弥补人工固氮对氮循环造成的影响
D 同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的化学方程式为
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:
5CH3OH+6NO


 +
+(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:
| 共价键 | N≡N | H-H | N-H |
| 断开1 mol共价键所需能量(kJ) | 946 | 436 | 391 |
(6)已知:①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H1= -a kJ/mol
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2= -bkJ/mol;
③H2(g)+
 O2(g)=H2O(g) △H3= -c kJ/mol
O2(g)=H2O(g) △H3= -c kJ/mol④H2(g)+
 O2(g)=H2O(l) △H4= -d kJ/mol
O2(g)=H2O(l) △H4= -d kJ/mol有关下列叙述不正确的是
a.由上述热化学方程式可知△H3<△H4
b.H2的燃烧热为d kJ/mol
c.4NH3(g)+4O2(g)=2NO(g)+N2(g)+6H2O(g) △H=(-a-b) kJ/mol
d.4NH3(g)
 2N2(g)+6H2(g) △H =(6d-b)kJ/mol
2N2(g)+6H2(g) △H =(6d-b)kJ/mol
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用图表示。
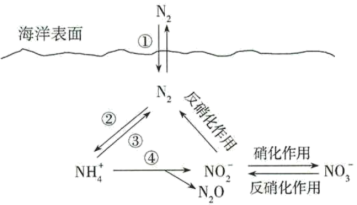
(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_______ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是_______ (填字母序号)。
a. 海洋中存在游离态的氮
b. 海洋中的氮循环起始于氮的氧化
c. 向海洋排放含NO 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量
(3)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,表为对10 L人工海水样本的监测数据:
硝化细菌去除氨氮的最佳反应温度是_______ ,在最佳反应温度时,48 h内去除氨氮反应的平均速率是_______ mg·L-1·h-1。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a. 海洋中存在游离态的氮
b. 海洋中的氮循环起始于氮的氧化
c. 向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量(3)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,表为对10 L人工海水样本的监测数据:
| 温度/℃ | 样本氨氮含量/mg | 处理24 h | 处理48 h |
| 氨氮含量/mg | 氨氮含量/mg | ||
| 20 | 1008 | 838 | 788 |
| 25 | 1008 | 757 | 468 |
| 30 | 1008 | 798 | 600 |
| 40 | 1008 | 977 | 910 |
硝化细菌去除氨氮的最佳反应温度是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如图所示的氮循环是生态系统物质循环的重要组成部分,人类活动加剧了氮循环中的物质转化。
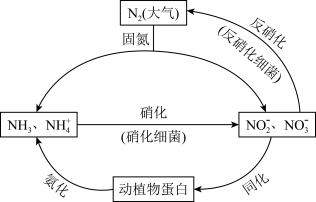
(1)结合图象判断下列说法正确的是________ (填字母序号)。
A.固氮过程中,N2只做氧化剂
B.在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C.反硝化过程有助于弥补人工固氮对氮循环造成的影响
D.同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的反应的化学方程式为_______ 。
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:
5CH3OH + 6NO3- N2↑ + 4HCO3-+
N2↑ + 4HCO3-+______ +______
(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:_______ 。
(5)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图所示:
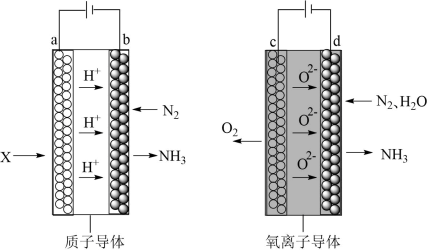
①图中,a电极上通入的X为_______ 。
②图中,d电极上的电极反应式为_______ 。

(1)结合图象判断下列说法正确的是
A.固氮过程中,N2只做氧化剂
B.在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C.反硝化过程有助于弥补人工固氮对氮循环造成的影响
D.同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的反应的化学方程式为
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:
5CH3OH + 6NO3-
 N2↑ + 4HCO3-+
N2↑ + 4HCO3-+(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:
| 共价键 | N≡N | H-H | N-H |
| 断开1mol共价键所需能量(kJ) | 946 | 436 | 391 |
(5)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图所示:

①图中,a电极上通入的X为
②图中,d电极上的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】研究氮的循环和转化对生产,生活有重要的价值。
Ⅰ.(1)写出实验室制备氨气的化学方程式:_______ 。
Ⅱ.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。
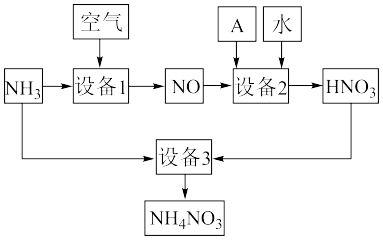
(2)设备1、3中 发生反应的化学方程式分别是_______ 。设备2中通入的物质 A 是_______ 。
Ⅲ.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH 和NH3·H2O 的形式存在。某工厂处理氨氮废水的流程如图:
和NH3·H2O 的形式存在。某工厂处理氨氮废水的流程如图:
含NH 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标
(3)过程①的目的是将 NH 转化为NH3,并通过鼓入大量空气将氨气吹出,写出 NH
转化为NH3,并通过鼓入大量空气将氨气吹出,写出 NH 转化为NH3的离子方程式:
转化为NH3的离子方程式:_______ 。
(4)过程②加入NaClO 溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为______ 、__________
(5)含余氯废水的主要成分是 NaClO以及 HClO,X可选用以下哪种溶液以达到去除余氯的目的_______ (填字母)。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
写出其中一个反应的离子方程式:_______
Ⅰ.(1)写出实验室制备氨气的化学方程式:
Ⅱ.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。

(2)设备1、3中 发生反应的化学方程式分别是
Ⅲ.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH
 和NH3·H2O 的形式存在。某工厂处理氨氮废水的流程如图:
和NH3·H2O 的形式存在。某工厂处理氨氮废水的流程如图:含NH
 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标(3)过程①的目的是将 NH
 转化为NH3,并通过鼓入大量空气将氨气吹出,写出 NH
转化为NH3,并通过鼓入大量空气将氨气吹出,写出 NH 转化为NH3的离子方程式:
转化为NH3的离子方程式:(4)过程②加入NaClO 溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为
(5)含余氯废水的主要成分是 NaClO以及 HClO,X可选用以下哪种溶液以达到去除余氯的目的
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
写出其中一个反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】磺酰胺[SO2(NH2)2]易溶于醇,溶于热水,不溶于冷水,在酸性、中性、碱性水溶液中性质稳定,主要用于制造医药、农药、染料等。制备磺酰胺的装置如下,其原理为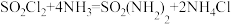 。已知:磺酰氯(SO2Cl2)熔点为-54.1℃,沸点为69.1℃,遇潮湿空气会水解产生酸雾。
。已知:磺酰氯(SO2Cl2)熔点为-54.1℃,沸点为69.1℃,遇潮湿空气会水解产生酸雾。
Ⅰ.磺酰胺的制备____________ 。
(2)装置B中盛放的试剂为____________ (填字母)。
a.碱石灰 b.浓硫酸 c.P2O5 d.无水CaCl2
(3)写出 SO2Cl2水解的化学方程式:____________ 。
(4)装置C中多孔球泡的作用是____________ 。
Ⅱ.用如下装置测定产品SO2(NH2)2的含量(假设只含NH4Cl杂质,部分装置已省略)____________ ,单向阀的作用是____________ 。
(6)滴定:将液封装置2中的水放入锥形瓶中,再将锥形瓶中的溶液倒入容量瓶中配制成500 mL的溶液,取20 mL溶液用c2 mol/L的NaOH标准溶液滴定过量的H2SO4,共消耗NaOH标准溶液V2 mL,产品中SO2(NH2)2的含量是____________ (列出计算式)。
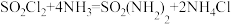 。已知:磺酰氯(SO2Cl2)熔点为-54.1℃,沸点为69.1℃,遇潮湿空气会水解产生酸雾。
。已知:磺酰氯(SO2Cl2)熔点为-54.1℃,沸点为69.1℃,遇潮湿空气会水解产生酸雾。Ⅰ.磺酰胺的制备

(2)装置B中盛放的试剂为
a.碱石灰 b.浓硫酸 c.P2O5 d.无水CaCl2
(3)写出 SO2Cl2水解的化学方程式:
(4)装置C中多孔球泡的作用是
Ⅱ.用如下装置测定产品SO2(NH2)2的含量(假设只含NH4Cl杂质,部分装置已省略)
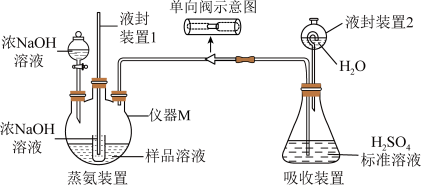
(6)滴定:将液封装置2中的水放入锥形瓶中,再将锥形瓶中的溶液倒入容量瓶中配制成500 mL的溶液,取20 mL溶液用c2 mol/L的NaOH标准溶液滴定过量的H2SO4,共消耗NaOH标准溶液V2 mL,产品中SO2(NH2)2的含量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】管道工人曾经用浓氨水检测氯气管道是否漏气。某化学兴趣小组利用下图装置探究氯气与氨气之间的反应原理。其中A、F分别为氨气和氯气的发生装置,C为氧气与氨气的反应装置。
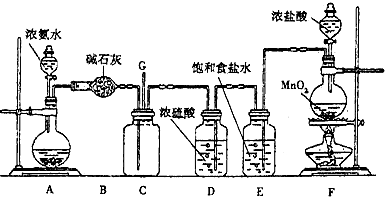
请回答下列问题:
(1)装置A中的烧瓶内固体可以选用______ (选填序号).
A.二氧化锰 B.碱石灰 C.五氧化二磷
(2)装置F中发生反应的离子方程式为__________________________________ ;装置E的作用是______________________________ ;
(3)通入装置C的两根导管左边较长、右边较短,目的是________________________ 。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:_____________________________________________ ;该反应中,氧化剂与还原剂的物质的量之比为_________ 。从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?__________ 。

请回答下列问题:
(1)装置A中的烧瓶内固体可以选用
A.二氧化锰 B.碱石灰 C.五氧化二磷
(2)装置F中发生反应的离子方程式为
(3)通入装置C的两根导管左边较长、右边较短,目的是
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色溶液X,由K+、NH4+、Ba2+、Al3+、Fe3+、CO32-、SO42-中的若干离子组成,取该溶液进行如下实验:

(1)白色沉淀甲是___ ;
(2)试写出实验过程中生成气体A、B的离子方程式___ ;
(3)通过上述实验,可确定X溶液中一定存在的阴离子是___ ;尚未确定是否存在的离子是___ ;
(4)若要检验溶液中是否含有CO32-离子,其方法是___ 。

(1)白色沉淀甲是
(2)试写出实验过程中生成气体A、B的离子方程式
(3)通过上述实验,可确定X溶液中一定存在的阴离子是
(4)若要检验溶液中是否含有CO32-离子,其方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O] 比 FeSO4稳定,不易被氧气氧化,常用于代替 FeSO4作分析试剂。某小组在实验室制备(NH4)2Fe(SO4)2·6H2O 并探究其分解产物。
Ⅰ.按以下流程制备硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]
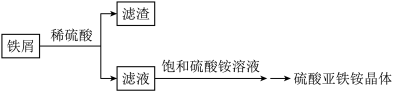
(1)铁屑溶于稀硫酸过程中,适当加热的目的是________ 。
(2)流程中,需将滤液转移到____ (填写仪器名称)中,迅速加入饱和硫酸铵溶液,直接加热蒸发混合溶液,观察到____ ,停止加热。
II.查阅资料可知硫酸亚铁铵晶体加热主要发生反应:(NH4)2Fe(SO4)2 — Fe2O3+ SO2↑+ NH3↑+ N2↑+ H2O但伴有副反应发生,生成少量SO3和O2。设计以下实验探究分解的产物:
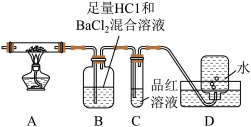
(3)配平,完整写出上述分解反应的化学方程式_______ 。
(4)加热过程,A 中固体逐渐变为________ 色。待晶体完全分解后,为验证A中残留物是否含有FeO,需选用的试剂有______ (填字母)。
A KSCN溶液 B 稀硫酸 C 浓盐酸 D 酸性KMnO4溶液
(5)B中有白色沉淀生成,写出生成该白色沉淀的离子方程式:_______ 。
(6)C的作用是___________ 。
(7)D中集气瓶能收集到氧气,________ (填“能”或“不能”)用带火星木条检验。
(8)上述反应结束后,继续证明分解产物中含有 NH3的方法是_______ 。
Ⅰ.按以下流程制备硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]

(1)铁屑溶于稀硫酸过程中,适当加热的目的是
(2)流程中,需将滤液转移到
II.查阅资料可知硫酸亚铁铵晶体加热主要发生反应:(NH4)2Fe(SO4)2 — Fe2O3+ SO2↑+ NH3↑+ N2↑+ H2O但伴有副反应发生,生成少量SO3和O2。设计以下实验探究分解的产物:

(3)配平,完整写出上述分解反应的化学方程式
(4)加热过程,A 中固体逐渐变为
A KSCN溶液 B 稀硫酸 C 浓盐酸 D 酸性KMnO4溶液
(5)B中有白色沉淀生成,写出生成该白色沉淀的离子方程式:
(6)C的作用是
(7)D中集气瓶能收集到氧气,
(8)上述反应结束后,继续证明分解产物中含有 NH3的方法是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】如图为某些中学常见物质的转化关系(部分反应条件或生成物略去)。其中A、B、C为常见单质,其余物质为化合物,C为黑色固体,气体D溶于水所得溶液显碱性,E为常用调味剂且焰色试验为黄色火焰,J为细小的白色晶体,常用作食物膨松剂,F常温下为无色无味液体。回答下列问题:
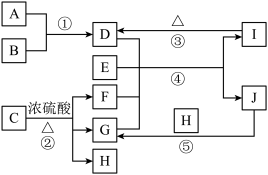
(1)H中含有的化学键为_______ (填“离子键”“共价键”或“离子键和共价键”)。
(2)实验室检验I中所含阳离子的方法为_________ 。
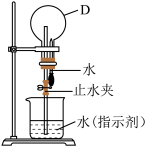
(3)反应①的化学方程式为________ ,以气体D与蒸馏水利用如图装置进行喷泉实验,引发喷泉的操作为________ 。
(4)反应②的化学方程式为________ ,其中氧化产物和还原产物的物质的量之比为________ 。
(5)反应④的化学方程式为_______ ,该反应可以发生的原因为________ 。
(6)向J的溶液中通入过量H时发生反应的离子方程式为________ 。

(1)H中含有的化学键为
(2)实验室检验I中所含阳离子的方法为
(3)反应①的化学方程式为

(4)反应②的化学方程式为
(5)反应④的化学方程式为
(6)向J的溶液中通入过量H时发生反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】氨是化肥工业和基本有机化工的重要原料,合成氨反应是化学上最重要的反应之一

(1)N2和H2在常温常压下反应极慢,为提高合成氨反应的速率,工业上除采取增大压强以提高浓度外,还可采取的措施是____________ (答一条即可)
(2)已知反应N2(g)+3H2(g) 2NH3(g)的反应速率与时间的变化关系如图a所示,浓度随时间的变化如图b所示
2NH3(g)的反应速率与时间的变化关系如图a所示,浓度随时间的变化如图b所示
①图a中N点对应的时间是图b中的____________ (填“t1”“t2”或“t3”)
②图b中,0~t1内平均速率v正(N2)=mol•L-1•min-1,则t1~t2内平均速率v正(N2)应____________ (填标号)mol•L-1•min-1
A.大于uB.等于uC.小于u
(3)往恒温恒容密闭容器中通入1molN2和3molH2,充分反应后,测得压强为起始时压强的75%,N2的转化率为____________ 。
(4)某兴趣小组同学设计了如图所示装置模拟工业上合成氨。

①流经橡胶管处的气体成分为____________ (填化学式)
②能说明有氨生成的现象是____________ 。

(1)N2和H2在常温常压下反应极慢,为提高合成氨反应的速率,工业上除采取增大压强以提高浓度外,还可采取的措施是
(2)已知反应N2(g)+3H2(g)
 2NH3(g)的反应速率与时间的变化关系如图a所示,浓度随时间的变化如图b所示
2NH3(g)的反应速率与时间的变化关系如图a所示,浓度随时间的变化如图b所示①图a中N点对应的时间是图b中的
②图b中,0~t1内平均速率v正(N2)=mol•L-1•min-1,则t1~t2内平均速率v正(N2)应
A.大于uB.等于uC.小于u
(3)往恒温恒容密闭容器中通入1molN2和3molH2,充分反应后,测得压强为起始时压强的75%,N2的转化率为
(4)某兴趣小组同学设计了如图所示装置模拟工业上合成氨。

①流经橡胶管处的气体成分为
②能说明有氨生成的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】研究氮及其化合物的性质,能有效改善人类的生存环境。氮元素化合价—物质类别关系图如下。
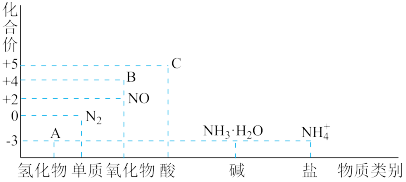
回答下列问题:
(1)工业用过量的A的水溶液消除燃煤烟气中二氧化硫,反应离子方程式为_______ 。
(2)大气中氮元素含量丰富,写出常见人工固氮的化学方程式_______ 。
(3)NO是制硝酸原料,还是扩张血管的因子,实验室里可以用亚硝酸钠与稀硫酸反应来制备,同时生成硝酸,化学方程式为_______ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______ 。
(5)C中阴离子的检验方法——棕色环实验的原理是:C被硫酸亚铁还原为NO,硫酸亚铁与NO反应即生成深棕色的硫酸亚硝基铁。写出C与硫酸亚铁反应的离子方程式_______ 。

回答下列问题:
(1)工业用过量的A的水溶液消除燃煤烟气中二氧化硫,反应离子方程式为
(2)大气中氮元素含量丰富,写出常见人工固氮的化学方程式
(3)NO是制硝酸原料,还是扩张血管的因子,实验室里可以用亚硝酸钠与稀硫酸反应来制备,同时生成硝酸,化学方程式为
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
(5)C中阴离子的检验方法——棕色环实验的原理是:C被硫酸亚铁还原为NO,硫酸亚铁与NO反应即生成深棕色的硫酸亚硝基铁。写出C与硫酸亚铁反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室模拟合成氨和氨催化氧化的流程如下:


已知:实验室用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)仪器k的名称是____ 。
(2)从图中选择制取气体的合适装置:氮气_____ 、氢气_____ 。
(3)实验室制取氨的化学方程式是_________ 。
(4)如图是某学生设计收集氨的几种装置,其中可行的是______ 。

(5)用甲装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入甲装置的锥形瓶内,能使铂丝保持红热的原因是:_____ ,锥形瓶中还可观察到的现象是:___ 。
(6)写出甲装置中氨催化氧化的化学方程式:________ 。


已知:实验室用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)仪器k的名称是
(2)从图中选择制取气体的合适装置:氮气
(3)实验室制取氨的化学方程式是
(4)如图是某学生设计收集氨的几种装置,其中可行的是

(5)用甲装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入甲装置的锥形瓶内,能使铂丝保持红热的原因是:
(6)写出甲装置中氨催化氧化的化学方程式:
您最近一年使用:0次



