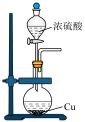
实验室做锌与浓硫酸反应的实验时,有同学认为产生二氧化硫,有同学认为除二氧化硫外,还可能产生氢气。为了验证两位同学的判断是否正确,设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去。E、F瓶中试剂相同)下列说法错误的是


A.生成二氧化硫的化学方程式为Zn+2H2SO4(浓)  ZnSO4+SO2↑+2H2O ZnSO4+SO2↑+2H2O |
| B.装置E、F中加入的试剂为品红溶液,作用是检验SO2的存在以及是否除尽 |
| C.装置H中白色粉末变蓝可以说明X中含有氢气 |
| D.装置I中加入的试剂是碱石灰,作用是防止空气中的水蒸气进入H |
更新时间:2022-05-06 22:09:52
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】如图是铜与浓硫酸反应的实验装置。已知:铜片足量,浓硫酸(浓度为 )为50mL。下列有关判断正确的是
)为50mL。下列有关判断正确的是

 )为50mL。下列有关判断正确的是
)为50mL。下列有关判断正确的是
A.装置B中盛装的是浓硫酸,作用是干燥 |
| B.装置C为安全瓶,防止装置D中的液体倒吸入装置B中 |
C.品红溶液可检验生成的 ,碱性棉球的作用是吸收未反应的 ,碱性棉球的作用是吸收未反应的 气体 气体 |
| D.充分反应后,被还原的硫酸等于0.45mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列制取 、验证其还原性、收集并进行尾气处理的装置和原理能达到实验目的的是
、验证其还原性、收集并进行尾气处理的装置和原理能达到实验目的的是
 、验证其还原性、收集并进行尾气处理的装置和原理能达到实验目的的是
、验证其还原性、收集并进行尾气处理的装置和原理能达到实验目的的是
|
|
A.制取 | B.验证还原性 |
|
|
C.收集 | D.尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
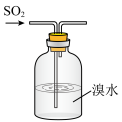
【推荐1】气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),若洗气瓶中有沉淀生成,则气体F可能为下列气体中的

①CO2②NO2③NH3④O2⑤Cl2⑥HCl

①CO2②NO2③NH3④O2⑤Cl2⑥HCl
| A.①②③④ | B.②③④⑤ | C.②③④⑥ | D.②④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应的离子方程式正确的是
A.碘化亚铁溶液与等物质的量的氯气: |
B.将氯气通入冷的石灰乳中制漂白粉: |
C.向次氯酸钙溶液通入足量二氧化碳: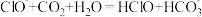 |
D.向硫化钠溶液通入足量二氧化硫: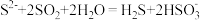 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.常温下铁与浓硫酸不反应 | B.钠与氧气反应的产物与反应条件无关 |
| C.漂白粉暴露在空气中会变质 | D.硫单质能直接和氧气反应生成三氧化硫 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知锌与硫酸有如下两个反应:
①Zn+H2SO4(稀)=ZnSO4+H2↑
②Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O,
下列说法不正确的是
①Zn+H2SO4(稀)=ZnSO4+H2↑
②Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O,
下列说法不正确的是
| A.浓硫酸和稀硫酸均有氧化性,所以硫酸是氧化性酸 |
| B.过量的锌在浓硫酸中反应可得二氧化硫和氢气 |
| C.锌与稀硫酸反应的氧化产物是硫酸锌 |
| D.不管是浓硫酸还是稀硫酸,若反应过程中被还原的硫酸物质的量相等,则生成气体的物质的量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 将 与稀盐酸反应得到的气体通入到澄清石灰水中 与稀盐酸反应得到的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 非金属性:Cl>C |
| B | 将气体X通入品红溶液中 | 品红溶液褪色 | X一定是 |
| C | 将少量表面被氧化的钠投入蒸馏水中 | 有气泡产生 | 钠表面有 生成 生成 |
| D | 将浓硫酸加入滴有几滴水的蔗糖中 | 蔗糖逐渐变黑形成“黑面包”,产生有刺激性气体 | 浓硫酸的性质:脱水性、强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将石蜡油分解后的气体通入Br2的CCl4溶液 | 溶液褪色 | 石蜡油分解产生了乙烯 |
| B | 室温下,向0.1mol·L-1HCl溶液中加入少量镁粉 | 产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
| D | 向2支盛有2mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液 | 一支试管中产生黄色沉淀,另一支中无明显现象 | Ksp(AgI)>Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:Fe3+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+(几乎无色);[Fe(H2O)6]3+水解生成[Fe(H2O)6-n(OH)n]3-n(黄色);[FeCl4(H2O)2]-(黄色)。下列实验所得结论不正确 的是
注:加热为微热,忽略体积变化。
| ① | ② | ③ | ④ |
 |  |  |  |
| 加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色变深 | 加热前溶液为黄色,加热后溶液颜色变深 |
| A.实验①中,Fe2(SO4)3溶液显浅黄色原因是[Fe(H2O)6]3+发生了水解反应 |
| B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响 |
C.实验③中,存在可逆反应:Fe3++4Cl-+2H2O [FeCl4(H2O)2]- [FeCl4(H2O)2]- |
| D.实验④,可证明升高温度,Fe3+水解平衡正向移动 |
您最近一年使用:0次