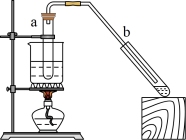
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。

完成下列填空:
(1)实验时,浓硫酸用量不能过多,原因是_______ 。
(2)饱和 溶液的作用是
溶液的作用是_______ 、_______ 、_______ 。
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,_______ 、_______ ,然后分液。
(4)若用b装置制备乙酸乙酯,其缺点有_______ 、_______ 。由b装置制得的乙酸乙酯粗产品经饱和碳酸钠溶液洗涤后,还可能含有的有机杂质是_______ ,分离乙酸乙酯与该杂质的方法是_______ 。

完成下列填空:
(1)实验时,浓硫酸用量不能过多,原因是
(2)饱和
 溶液的作用是
溶液的作用是(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,
(4)若用b装置制备乙酸乙酯,其缺点有
更新时间:2022-05-08 09:20:05
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
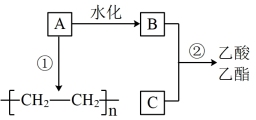
【推荐1】A的产量可以用来衡量一个国家石油化工发展水平,以A为主要原料合成一种具有果香味的物质E的生产流程如下:

(1)D的官能团名称:___________ 。
(2)写出反应②的化学方程式___________ 。
(3)步骤④的反应类型:___________ 。
(4)同学欲用如图装置制备物质E,请回答以下问题:
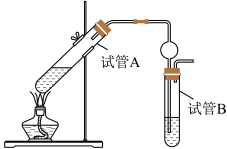
①试管A发生反应的化学方程式:___________ 。
②试管B中的试剂为饱和 溶液,其作用除了降低乙酸乙酯的溶解度,便于分层之外,还有
溶液,其作用除了降低乙酸乙酯的溶解度,便于分层之外,还有___________ 。
③试管A中加几块碎瓷片的目的是___________ 。

(1)D的官能团名称:
(2)写出反应②的化学方程式
(3)步骤④的反应类型:
(4)同学欲用如图装置制备物质E,请回答以下问题:

①试管A发生反应的化学方程式:
②试管B中的试剂为饱和
 溶液,其作用除了降低乙酸乙酯的溶解度,便于分层之外,还有
溶液,其作用除了降低乙酸乙酯的溶解度,便于分层之外,还有③试管A中加几块碎瓷片的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
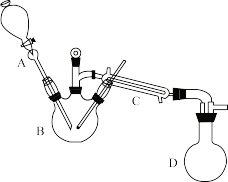
【推荐2】实验室可用乙酸和乙醇为原料制备乙酸乙酯,制备装置如图所示(夹持和加热装置已省略)。
I.在三颈烧瓶中加入适量的乙醇,再缓慢加入浓硫酸,使其混合均好实验仪器。
II.通过仪器A向三颈烧瓶中加入乙醇和冰醋酸的混合液,小火加热至110~120℃,控制A中液体的滴速和馏出速率大致相等,滴加完毕后,继续加热15分钟。
II.依次用饱和Na2CO3溶液、饱和食盐水和饱和CaCl2溶液洗涤馏出液。
IV.分液,向分液后的有机层中加入无水氯化镁,静置,过滤除去氯化镁固体,进一步蒸馏纯化,收集馏分。
回答下列问题:
(1)仪器A和C的名称分别是_______ 、_______ ,冷水从C仪器_______ (填“上”或“下”)口进。
(2)反应发生装置B的加热方式是_______ ,为了减少产物乙酸乙酯的挥发,可以对仪器D采取的措施是_______ 。
(3)在加热反应过程中控制滴速和馏出速率大致相等的原因是_______ 。
(4)用饱和Na2CO3溶液洗涤时,反应的离子方程式为_______ 。
(5)用CaCl2溶液洗涤除去乙醇之前,先要用饱和食盐水洗涤,原因是_______ 。加入无水氯化镁的作用是_______ 。

I.在三颈烧瓶中加入适量的乙醇,再缓慢加入浓硫酸,使其混合均好实验仪器。
II.通过仪器A向三颈烧瓶中加入乙醇和冰醋酸的混合液,小火加热至110~120℃,控制A中液体的滴速和馏出速率大致相等,滴加完毕后,继续加热15分钟。
II.依次用饱和Na2CO3溶液、饱和食盐水和饱和CaCl2溶液洗涤馏出液。
IV.分液,向分液后的有机层中加入无水氯化镁,静置,过滤除去氯化镁固体,进一步蒸馏纯化,收集馏分。
回答下列问题:
(1)仪器A和C的名称分别是
(2)反应发生装置B的加热方式是
(3)在加热反应过程中控制滴速和馏出速率大致相等的原因是
(4)用饱和Na2CO3溶液洗涤时,反应的离子方程式为
(5)用CaCl2溶液洗涤除去乙醇之前,先要用饱和食盐水洗涤,原因是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某化合物I可通过如图合成路线合成:

回答下列问题:
(1)A~I中,属于烃的是___________ (填标号)。
(2)E→F的反应类型属于___________ (填“1,2-加成”或“1,4-加成”)。
(3)写出②、⑦、⑧发生反应的化学方程式和反应类型:②___________ 、⑦___________ 、⑧___________ 。
(4)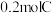 完全燃烧消耗标准状况下
完全燃烧消耗标准状况下 体积
体积___________ L。
(5)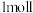 最多可与
最多可与________  反应,所得产物为
反应,所得产物为________ 、________ 。
(6)H→I中浓硫酸的作用是___________ 。

回答下列问题:
(1)A~I中,属于烃的是
(2)E→F的反应类型属于
(3)写出②、⑦、⑧发生反应的化学方程式和反应类型:②
(4)
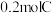 完全燃烧消耗标准状况下
完全燃烧消耗标准状况下 体积
体积(5)
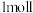 最多可与
最多可与 反应,所得产物为
反应,所得产物为(6)H→I中浓硫酸的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
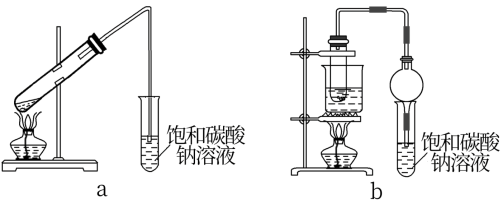
完成下列填空:
(1)写出制备乙酸乙酯反应的化学方程式___ ;反应类型____ 。
(2)饱和Na2CO3溶液的作用是___ 。
(3)写出用装置b制备乙酸乙酯的优点是___ 和___ 。
(4)若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生酯化反应,一段时间后,反应混合物中含有18O的分子有___ 。
A.1种 B.2种 C.3种 D.4种

完成下列填空:
(1)写出制备乙酸乙酯反应的化学方程式
(2)饱和Na2CO3溶液的作用是
(3)写出用装置b制备乙酸乙酯的优点是
(4)若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生酯化反应,一段时间后,反应混合物中含有18O的分子有
A.1种 B.2种 C.3种 D.4种
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】某有机化合物充分燃烧后的产物只有CO2和H2O,摩尔质量为90g/mol,含碳元素的质量分数为40%,氢元素的质量分数为6.67%。
(1)该化合物的分子式为___________ 。
(2)取相同质量的该化合物分别与足量的NaHCO3和Na反应,生成标准状况下的气体的量相同,则该有机物可能的结构简式为___________ 。
(3)该分子有多种同分异构体,写出满足下列条件的物质与足量乙酸反应的化学方程式:___________ :
Ⅰ.能与新制的银氨溶液反应生成光亮的银镜;
Ⅱ.该物质与足量的乙酸在一定条件下生成1mol有机产物时,质量增加84g;
Ⅲ.该物质有5种环境的氢。
(1)该化合物的分子式为
(2)取相同质量的该化合物分别与足量的NaHCO3和Na反应,生成标准状况下的气体的量相同,则该有机物可能的结构简式为
(3)该分子有多种同分异构体,写出满足下列条件的物质与足量乙酸反应的化学方程式:
Ⅰ.能与新制的银氨溶液反应生成光亮的银镜;
Ⅱ.该物质与足量的乙酸在一定条件下生成1mol有机产物时,质量增加84g;
Ⅲ.该物质有5种环境的氢。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室制备乙酰乙酸乙酯(CH3COCH2COOC2H5)的反应原理:
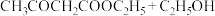 制备装置(烧瓶中物质充分反应后再滴加乙酸溶液)如下图所示:
制备装置(烧瓶中物质充分反应后再滴加乙酸溶液)如下图所示:

已知:①几种物质的部分性质:
②10 mL乙酸乙酯粗品中含乙酸乙酯8.8g和少量乙醇;
③CH3COCH2COOC2H5亚甲基上的H有一定的酸性,制备时部分形成乙酰乙酸乙酯的钠盐。
回答下列问题:
(1)仪器X的名称是_______ ,冷凝水从_______ (填“a”或“b”)端流进。
(2)装置Y盛放碱石灰的作用是_______ 。
(3)反应结束后,滴加50%乙酸至混合液呈弱酸性的原因是_______ 。
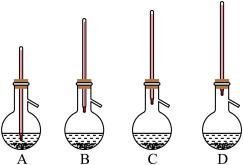
(4)提纯产品时需要进行蒸馏,下列装置中温度计位置正确的是_______ (填字母)。
(5)最终得到乙酰乙酸乙酯3.43 g,则上述实验中乙酰乙酸乙酯的产率为_______ (保留两位有效数字)。

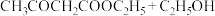 制备装置(烧瓶中物质充分反应后再滴加乙酸溶液)如下图所示:
制备装置(烧瓶中物质充分反应后再滴加乙酸溶液)如下图所示:
已知:①几种物质的部分性质:
| 物质 | 沸点/℃ | 相对分子质量 | 水中溶解性 |
| 乙酸乙酯 | 77.2 | 88 | 微溶 |
| 乙酰乙酸乙酯 | 181(温度超过95℃时易分解) | 130 | 微溶 |
| 乙酸 | 118 | 60 | 易溶 |
③CH3COCH2COOC2H5亚甲基上的H有一定的酸性,制备时部分形成乙酰乙酸乙酯的钠盐。
回答下列问题:
(1)仪器X的名称是
(2)装置Y盛放碱石灰的作用是
(3)反应结束后,滴加50%乙酸至混合液呈弱酸性的原因是
(4)提纯产品时需要进行蒸馏,下列装置中温度计位置正确的是

(5)最终得到乙酰乙酸乙酯3.43 g,则上述实验中乙酰乙酸乙酯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】今有下列六组仪器:①牛角管、②锥形瓶、③温度计、④冷凝管、⑤已组装固定好的铁架台、酒精灯和带塞(有孔)蒸馏烧瓶(垫有石棉网)、⑥带铁夹的铁架台。现要进行酒精和水混合物的分离实验。试回答下列问题:
(1)按仪器的安装先后顺序排列以上提供的各组仪器(填序号):___________________ 。
(2)冷凝管中冷凝水应___________ 。(填“下进上出”或“上进下出”)。
(3)蒸馏时,温度计水银球应位于_______________________________ 。
(4)在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是___________________________ 。
(5)蒸馏后在锥形瓶中收集到的液体是________ ,烧瓶中剩下的液体主要是____________ 。
(1)按仪器的安装先后顺序排列以上提供的各组仪器(填序号):
(2)冷凝管中冷凝水应
(3)蒸馏时,温度计水银球应位于
(4)在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是
(5)蒸馏后在锥形瓶中收集到的液体是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业水合肼法制备叠氮化钠的工艺流程如图所示:

一、合成水合肼
已知: (水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。
(水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。 (水合肼)熔点-40℃,沸点118.5℃。
(水合肼)熔点-40℃,沸点118.5℃。
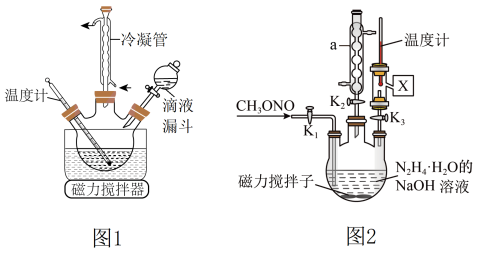
合成 的装置如图1所示。
的装置如图1所示。 碱性溶液与尿素
碱性溶液与尿素 水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
(1)写出 的结构式
的结构式____________ , 的电子式
的电子式____________
(2)①写出制取 的离子方程式
的离子方程式___________________________
②实验中通过滴液漏斗滴加的溶液是_________ 理由是_______________ 图1使用冷凝管的目的是____________________________________
③从反应后的混合溶分离出 ,应该采用的分离方法最合理的是
,应该采用的分离方法最合理的是________ 。
二、合成叠氮化钠(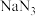 )晶体
)晶体
已知:相关物质的物理性质如下表
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是________________ 。(写出1点即可)
②图中 处连接的最合适装置应为下图中的
处连接的最合适装置应为下图中的__________ 。
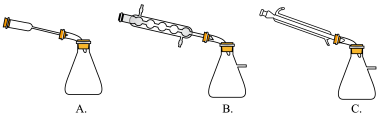
③步骤Ⅱ中制备叠氮化钠的操作是________ (填序号)步骤Ⅲ中溶液 进行蒸馏的合理操作顺序是
进行蒸馏的合理操作顺序是_______ 。(填序号)
①打开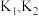 ,关闭
,关闭 ②打开
②打开 ③加热④关闭
③加热④关闭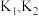
(4)步骤Ⅳ对溶液 加热蒸发至溶液体积的
加热蒸发至溶液体积的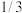 ,
,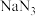 结晶析出。步骤Ⅴ可以用
结晶析出。步骤Ⅴ可以用________ 洗涤晶体。
A.水B.乙醚C.乙醇水溶液D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:
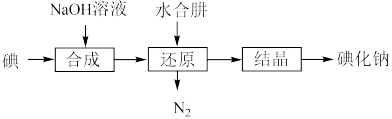
还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是______________________________________ 。


一、合成水合肼
已知:
 (水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。
(水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。 (水合肼)熔点-40℃,沸点118.5℃。
(水合肼)熔点-40℃,沸点118.5℃。合成
 的装置如图1所示。
的装置如图1所示。 碱性溶液与尿素
碱性溶液与尿素 水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。(1)写出
 的结构式
的结构式 的电子式
的电子式(2)①写出制取
 的离子方程式
的离子方程式②实验中通过滴液漏斗滴加的溶液是
③从反应后的混合溶分离出
 ,应该采用的分离方法最合理的是
,应该采用的分离方法最合理的是二、合成叠氮化钠(
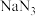 )晶体
)晶体已知:相关物质的物理性质如下表
| 熔点℃ | 沸点℃ | 溶解性 | |
 | -97 | 67.1 | 与水互溶 |
水合肼( ) ) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
亚硝酸甲酯(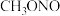 ) ) | -17 | -12 | 溶于乙醇、乙醚 |
| NaN3 | 与水互溶,不溶于乙醚、微溶于乙醇 |
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是
②图中
 处连接的最合适装置应为下图中的
处连接的最合适装置应为下图中的
③步骤Ⅱ中制备叠氮化钠的操作是
 进行蒸馏的合理操作顺序是
进行蒸馏的合理操作顺序是①打开
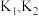 ,关闭
,关闭 ②打开
②打开 ③加热④关闭
③加热④关闭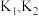
(4)步骤Ⅳ对溶液
 加热蒸发至溶液体积的
加热蒸发至溶液体积的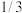 ,
,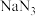 结晶析出。步骤Ⅴ可以用
结晶析出。步骤Ⅴ可以用A.水B.乙醚C.乙醇水溶液D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:

还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是
您最近一年使用:0次