填空。
(1)常压下,苯和甲苯的熔、沸点如下表;
晶体中分子间的作用力不仅取决于分子的大小,还取决于晶体中碳链的空间排列情况。请解释:
①苯的沸点比甲苯的沸点更低,主要原因是_______ 。
②苯晶体的熔点比甲苯的熔点更高,主要原因是_______ 。
(2)白磷晶体是由 分子(
分子(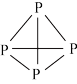 )组成的分子晶体,白磷以
)组成的分子晶体,白磷以 形式存在,而氮以
形式存在,而氮以 形式存在的原因
形式存在的原因_______ 。已知有关氮、磷的单键和叁键的键能( )如下表:
)如下表:
(1)常压下,苯和甲苯的熔、沸点如下表;
| 苯的模型 | 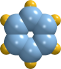 | 熔点:5.5℃ | 甲苯模型 |  | 熔点;-94.9℃ |
| 沸点:80.1℃ | 沸点:100.4℃ |
①苯的沸点比甲苯的沸点更低,主要原因是
②苯晶体的熔点比甲苯的熔点更高,主要原因是
(2)白磷晶体是由
 分子(
分子( )组成的分子晶体,白磷以
)组成的分子晶体,白磷以 形式存在,而氮以
形式存在,而氮以 形式存在的原因
形式存在的原因 )如下表:
)如下表:| N-N | N≡N | P-P | P≡P |
| 193 | 946 | 197 | 489 |
更新时间:2022-05-21 19:28:12
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】香豆素(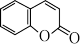 )是一种用途广泛的香料,可用于配制香精及制造化妆品等。某同学设计的制备香豆素的合成路线为:
)是一种用途广泛的香料,可用于配制香精及制造化妆品等。某同学设计的制备香豆素的合成路线为:
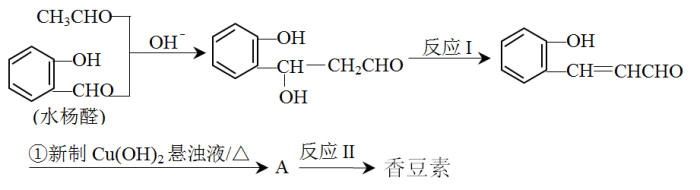
(1)反应I的反应类型为_______ 。
(2)反应II的化学方程式为_______ 。
(3)A在一定条件下可生成高分子酯,该高分子酯的结构简式为_______ 。
(4)水杨醛的芳香类同分异构体有_______ 种(不包含水杨醛本身),其中能与NaHCO3溶液反应的是 _______ (写结构简式)。
(5)水杨醛中含有苯环,苯环结构模型(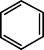 )最早由德国化学家凯库勒于1865年提出,该模型不能解释的事实是
)最早由德国化学家凯库勒于1865年提出,该模型不能解释的事实是_______ 。
A 苯不能使酸性高锰酸钾褪色
B 间二甲苯不存在同分异构体
C 苯分子空间构型为平面正六边形
D 苯与氯气在光照条件反应得到农药“六六六”(C6H6Cl6)
 )是一种用途广泛的香料,可用于配制香精及制造化妆品等。某同学设计的制备香豆素的合成路线为:
)是一种用途广泛的香料,可用于配制香精及制造化妆品等。某同学设计的制备香豆素的合成路线为:
(1)反应I的反应类型为
(2)反应II的化学方程式为
(3)A在一定条件下可生成高分子酯,该高分子酯的结构简式为
(4)水杨醛的芳香类同分异构体有
(5)水杨醛中含有苯环,苯环结构模型(
 )最早由德国化学家凯库勒于1865年提出,该模型不能解释的事实是
)最早由德国化学家凯库勒于1865年提出,该模型不能解释的事实是A 苯不能使酸性高锰酸钾褪色
B 间二甲苯不存在同分异构体
C 苯分子空间构型为平面正六边形
D 苯与氯气在光照条件反应得到农药“六六六”(C6H6Cl6)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构,为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为_____ ,能证明凯库勒观点错误的实验现象是_____ 。
(2)装置B的作用是_________ 。
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为_______ mL。(空气的平均相对分子质量为29)
(4)已知乳酸的结构简式为: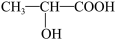 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:______ 。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为
(2)装置B的作用是
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为
(4)已知乳酸的结构简式为:
 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】蒽( 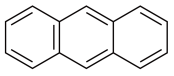 )与苯炔(
)与苯炔(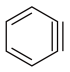 )反应生成化合物X(立体对称图形),如下图所示。
)反应生成化合物X(立体对称图形),如下图所示。
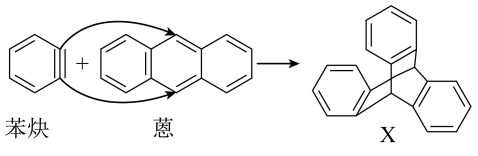
(1)蒽与X都属于___________。
(2)苯炔的分子式为___________ ,苯炔不具有的性质是___________ 。
A.能溶于水 B.能发生氧化反应 C.能发生加成反 D.常温常压下为气体
(3)苯是最简单的芳香烃,能证明其化学键不是单双键交替排列的事实是___________。
(4)下列属于苯的同系物的是___________(填字母符号)。
(5)能发生加成反应,也能发生取代反应,同时能使溴水因反应褪色,也能使酸性高锰酸钾溶液褪色的是___________。
(6)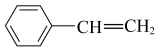 是生产某塑料的单体,写出合成该塑料的化学方程式:
是生产某塑料的单体,写出合成该塑料的化学方程式:___________ 。
 )与苯炔(
)与苯炔( )反应生成化合物X(立体对称图形),如下图所示。
)反应生成化合物X(立体对称图形),如下图所示。
(1)蒽与X都属于___________。
| A.环烃 | B.烷烃 | C.不饱和烃 |
A.能溶于水 B.能发生氧化反应 C.能发生加成反 D.常温常压下为气体
(3)苯是最简单的芳香烃,能证明其化学键不是单双键交替排列的事实是___________。
| A.它的对位二元取代物只有一种 | B.它的邻位二元取代物只有一种 |
| C.分子中所有碳碳键的键长均相等 | D.能发生取代反应和加成反应 |
A. | B.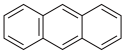 | C.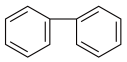 | D.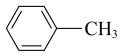 |
A.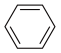 | B.C6H14 | C.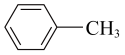 | D.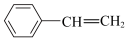 |
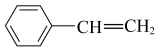 是生产某塑料的单体,写出合成该塑料的化学方程式:
是生产某塑料的单体,写出合成该塑料的化学方程式:
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)基态B原子的核外电子有_______ 种空间运动状态;基态Ni原子核外占据最高能层电子的电子云轮廓图的形状为_______ 。
(2)硼的卤化物的沸点如表所示:解释表中卤化物之间沸点差异的原因_______ ,BF3中B原子的杂化方式为_______ 。
(3)在石墨转化成金刚石的过程中,下列说法正确的是_______。
(4)铁酸钇是一种典型的单相多铁性材料其正交相晶胞结构如图所示。
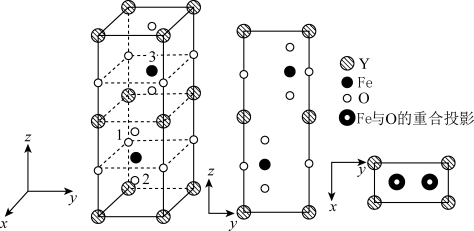
其中铁酸钇的化学式为_______ ,已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, -m,
-m, -n),则3号Fe原子的空间坐标为
-n),则3号Fe原子的空间坐标为_______ ,若晶胞参数分别为a pm、b pm和c pm,阿伏加德罗常数的值用NA表示,则该晶体的密度为_______  (列出表达式)
(列出表达式)
(1)基态B原子的核外电子有
(2)硼的卤化物的沸点如表所示:解释表中卤化物之间沸点差异的原因
| 卤化物 | BF3 | BCl3 | BBr3 |
| 沸点/℃ | -100.3 | 12.5 | 90 |
(3)在石墨转化成金刚石的过程中,下列说法正确的是_______。
| A.碳原子的杂化方式发生变化 | B.碳碳键的键能不变 |
| C.原子间成键方式未改变 | D.反应前后,物质的物理性质不变 |

其中铁酸钇的化学式为
 ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, -m,
-m, -n),则3号Fe原子的空间坐标为
-n),则3号Fe原子的空间坐标为 (列出表达式)
(列出表达式)
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知和碳元素同主族的X元素位于元素周期表中的第一个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成化合物的分子式是XY4.试回答:
(1)该化合物中是否存在氢键(填“是”或“否”)___________ ,分子为___________ (填“极性分子”或“非极性分子”)。
(2)该化合物在常温下为液体,该液体微粒间的作用力是___________ 。
(3)该化合物的沸点与SiCl4比较:___________ (填化学式)的高,原因是___________ 。
(1)该化合物中是否存在氢键(填“是”或“否”)
(2)该化合物在常温下为液体,该液体微粒间的作用力是
(3)该化合物的沸点与SiCl4比较:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
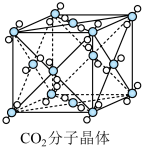
【推荐3】如图为干冰的晶胞结构:
(1)观察图形,确定在干冰中每个CO2分子周围有_______ 个与之紧邻且等距离的CO2分子,该结构单元平均占有_______ 个CO2分子。
(2)在干冰中撒入镁粉,用红热的铁棒引燃后,再盖上另一块干冰,出现的现象为_______ ,反应的化学方程式是_______ 。_______ CS2,填“>”或“<”),其原因是_______ 。
(4)在40GPa高压下,用激光器加热到1800K时,人们成功制得原子晶体干冰,其结构和性质与SiO2原子晶体相似,下列说法正确的是_______ 。
A.原子晶体干冰易升华,可用作制冷剂
B.原子晶体干冰有很高的熔点和沸点
C.原子晶体干冰的硬度小,不能用作耐磨材料
D.原子晶体干冰在一定条件下可与氢氧化钠反应
E.每摩尔原子晶体干冰中含有4molC—O键
(1)观察图形,确定在干冰中每个CO2分子周围有
(2)在干冰中撒入镁粉,用红热的铁棒引燃后,再盖上另一块干冰,出现的现象为
(4)在40GPa高压下,用激光器加热到1800K时,人们成功制得原子晶体干冰,其结构和性质与SiO2原子晶体相似,下列说法正确的是
A.原子晶体干冰易升华,可用作制冷剂
B.原子晶体干冰有很高的熔点和沸点
C.原子晶体干冰的硬度小,不能用作耐磨材料
D.原子晶体干冰在一定条件下可与氢氧化钠反应
E.每摩尔原子晶体干冰中含有4molC—O键
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】单质 Z 是一种常见的半导体材料,可由 X 通过如下图所示的路线制备,其中 X 为 Z 的氧化物,Y 为氢化物,分子结构与甲烷相似,回答下列问题:
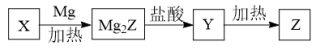
(1)能与 X 发生化学反应的酸是___________ ;在实验室中该酸保存在___________ 。
(2)由 Mg2Z 生成 Y 的化学反应方程式为___________ ,Y 分子的电子式为___________ 。
(3)晶体 Z 和 X 中熔点相对较高的是___________ (填写化学式)。

(1)能与 X 发生化学反应的酸是
(2)由 Mg2Z 生成 Y 的化学反应方程式为
(3)晶体 Z 和 X 中熔点相对较高的是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛(22Ti)铝合金在航空领域应用广泛,回答下列问题:
(1)基态Ti原子的核外电子排布式为[Ar]_____ ,其中s轨道上总共有______ 个电子。
(2)六氟合钛酸钾(K2TiF6)中存在[TiF6]2- 配离子,则钛元素的化合价是____ ,配位体____ 。
(3)TiCl3 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应: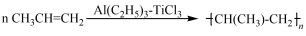 ,该反应中涉及的物质中碳原子的杂化轨道类型有
,该反应中涉及的物质中碳原子的杂化轨道类型有_______________ ;反应中涉及的元素中电负性最大的是_________ 。三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的是____________ 。
(4)钛与卤素形成的化合物的熔沸点如下表所示,

分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定规律的原因是___________________________ 。
(5)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是钛晶体的一种晶胞,晶胞参数a=0.295nm,c =0.469 nm,则该钛晶体的密度为__________________ g·cm-3(用NA 表示阿伏伽德罗常数的值,列出计算式即可)。

(1)基态Ti原子的核外电子排布式为[Ar]
(2)六氟合钛酸钾(K2TiF6)中存在[TiF6]2- 配离子,则钛元素的化合价是
(3)TiCl3 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:
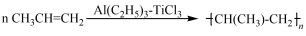 ,该反应中涉及的物质中碳原子的杂化轨道类型有
,该反应中涉及的物质中碳原子的杂化轨道类型有(4)钛与卤素形成的化合物的熔沸点如下表所示,

分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定规律的原因是
(5)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是钛晶体的一种晶胞,晶胞参数a=0.295nm,c =0.469 nm,则该钛晶体的密度为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氯化钠是一种典型且极具魅力的晶体,我们通过学习氯化钠可以更好地了解其他类似物质的结构。已知氯化钠的晶胞如下图1所示。

图1
(1)下列关于氯化钠的说法正确的是_______。
(2)已知 的密度为
的密度为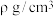 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在
,则在 晶体里
晶体里 和
和 的最短距离为
的最短距离为_______  。
。
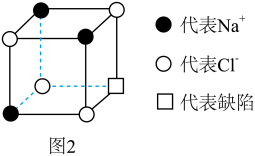
(3)温度升高时, 晶体出现缺陷,如图2所示,当图中方格内填入
晶体出现缺陷,如图2所示,当图中方格内填入 时,恰好构成氯化钠晶胞的1/8。
时,恰好构成氯化钠晶胞的1/8。 晶体出现缺陷时,其导电性大大增强,原因是
晶体出现缺陷时,其导电性大大增强,原因是_______ 。
(4) 、
、 的晶体类型与氯化钠相同,
的晶体类型与氯化钠相同, 和
和 的离子半径分别为
的离子半径分别为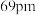 和
和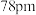 ,则熔点:
,则熔点:
_______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(5)钡在氧气中燃烧时得到一种钡的氧化物 晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为
晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为_______ 。

图1
(1)下列关于氯化钠的说法正确的是_______。
A.基态 的电子有5种空间运动状态 的电子有5种空间运动状态 |
| B.钠是第一电离能最大的碱金属元素 |
C.氯原子的价电子排布式可写成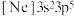 |
| D.每个氯离子周围与它最近且等距的氯离子有12个 |
 的密度为
的密度为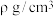 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在
,则在 晶体里
晶体里 和
和 的最短距离为
的最短距离为 。
。(3)温度升高时,
 晶体出现缺陷,如图2所示,当图中方格内填入
晶体出现缺陷,如图2所示,当图中方格内填入 时,恰好构成氯化钠晶胞的1/8。
时,恰好构成氯化钠晶胞的1/8。 晶体出现缺陷时,其导电性大大增强,原因是
晶体出现缺陷时,其导电性大大增强,原因是
(4)
 、
、 的晶体类型与氯化钠相同,
的晶体类型与氯化钠相同, 和
和 的离子半径分别为
的离子半径分别为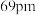 和
和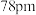 ,则熔点:
,则熔点:
 (填“>”“<”或“=”)
(填“>”“<”或“=”)(5)钡在氧气中燃烧时得到一种钡的氧化物
 晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为
晶体,其阴阳离子的排布与氯化钠相同,其中存在的化学键的类型为
您最近半年使用:0次



