2020年,全球爆发的新型冠状病毒肺炎疫情严重影响人们的身体健康。“84消毒液”能有效杀灭各种细菌和病毒,某同学购买了一瓶某品牌的“84消毒液”,其瓶体上的消毒液说明如图:
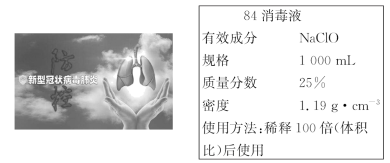
(1)工业上制备“84消毒液”的化学方程式为____ 。
(2)该“84消毒液”中的NaClO的物质的量浓度为____ 。
(3)该同学取100mL“84消毒液”稀释后用于消毒,稀释后的溶液的物质的量浓度_____ 。

(1)工业上制备“84消毒液”的化学方程式为
(2)该“84消毒液”中的NaClO的物质的量浓度为
(3)该同学取100mL“84消毒液”稀释后用于消毒,稀释后的溶液的物质的量浓度
21-22高一·全国·假期作业 查看更多[1]
(已下线)第05讲 物质的量浓度-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
更新时间:2022-06-17 13:24:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氯及其化合物的价类二维图如图,回答下列问题:

(1)不同浓度的盐酸可与NaClO溶液发生反应,其反应有① 、②
、②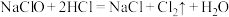 ,反应①属于
,反应①属于___________ (填四大基本反应类型);反应②中HCl体现的性质是___________ 。
(2)溶质质量分数为36.5%、密度为1.2 的浓盐酸中,盐酸的物质的量浓度为
的浓盐酸中,盐酸的物质的量浓度为_______  ,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是
,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______ (填标号)。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中 的数目 D.溶液的密度
的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500mL0.3 稀盐酸。该学生需要用量筒量取
稀盐酸。该学生需要用量筒量取_________ mL上述浓盐酸进行配制。完成此实验需用到的玻璃仪器除了量筒、烧杯、玻璃棒外,还需要_________ 。
(4)现将200mL0.3 盐酸与300mL0.4
盐酸与300mL0.4
 溶液混合,溶液体积变化忽略不计,所得溶液中
溶液混合,溶液体积变化忽略不计,所得溶液中 的物质的量浓度是
的物质的量浓度是___________  。
。

(1)不同浓度的盐酸可与NaClO溶液发生反应,其反应有①
 、②
、②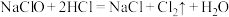 ,反应①属于
,反应①属于(2)溶质质量分数为36.5%、密度为1.2
 的浓盐酸中,盐酸的物质的量浓度为
的浓盐酸中,盐酸的物质的量浓度为 ,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是
,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中
 的数目 D.溶液的密度
的数目 D.溶液的密度(3)若用(2)中浓盐酸配制500mL0.3
 稀盐酸。该学生需要用量筒量取
稀盐酸。该学生需要用量筒量取(4)现将200mL0.3
 盐酸与300mL0.4
盐酸与300mL0.4
 溶液混合,溶液体积变化忽略不计,所得溶液中
溶液混合,溶液体积变化忽略不计,所得溶液中 的物质的量浓度是
的物质的量浓度是 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】计算后填空:
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为________ 。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为________ 。
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为__________ 。
(4)500mL Fe2(SO4)3溶液中含Fe3+ 28 g,则溶液中SO42-的物质的量浓度为________ mol·L-1。
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为________ 、________ 。
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为
(4)500mL Fe2(SO4)3溶液中含Fe3+ 28 g,则溶液中SO42-的物质的量浓度为
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.淀粉是人类膳食中糖类主要来源,在体内被酶水解为葡萄糖( )供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
)供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
(1)该病人血清葡萄糖GLU的物质的量浓度为_______ 。
(2)27g葡萄糖中含碳原子的物质的量为_______ ,含氢原子数为_______ 。
(3)0.5 mol葡萄糖在人体内完全转化为二氧化碳的体积(标准状况)是_______ 。
Ⅱ.现需500mL 0.2mol/L的KI溶液,用KI固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒。
(4)还缺少的仪器有_______ (写名称),所需KI固体的质量为_______ 。
(5)在配制过程中,下列操作会导致所配制溶液的浓度偏小的是_______。
 )供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
)供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:| 项目 | 测定值 | 单位 | 参考范围 |
| 血清葡萄糖GLU | 2.16↑ | g/L | 0.65~1.10 |
| 甘油三酯TG | 2.25↑ | g/L | 5~2.17 |
| 总胆固醇TCH | 1.79 | g/L | 1.5~2.2 |
(1)该病人血清葡萄糖GLU的物质的量浓度为
(2)27g葡萄糖中含碳原子的物质的量为
(3)0.5 mol葡萄糖在人体内完全转化为二氧化碳的体积(标准状况)是
Ⅱ.现需500mL 0.2mol/L的KI溶液,用KI固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒。
(4)还缺少的仪器有
(5)在配制过程中,下列操作会导致所配制溶液的浓度偏小的是_______。
| A.未洗涤烧杯和玻璃棒 |
| B.使用前,容量瓶中有少量蒸馏水 |
| C.定容时俯视凹液面 |
| D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________ 。
(2)该溶液中NaOH的质量分数为________ 。
(3)从该溶液中取出10 mL,含NaOH的质量为________ ,含NaOH的物质的量为________ 。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________ 。
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中NaOH的质量分数为
(3)从该溶液中取出10 mL,含NaOH的质量为
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸___ g(结果精确到1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得___ (实验条件下二氧化碳的密度为2g/L)?(写出计算过程,结果精确到0.01g)
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是不同温度下水的离子积常数:
试回答以下问题:
(1)若25℃<T1<T2,则a___________ 1×10-14(填“>”、“<”或“=”),做此判断的理由是___________ 。
(2)25℃时,某Na2SO4溶液中c(SO )=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=___________ 。
(3)若T2温度下,向水中滴入稀盐酸,测得溶液中c(H+)=1.0×10-3mol/L,则溶液中c(OH-)=___________ mol/L。
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
(1)若25℃<T1<T2,则a
(2)25℃时,某Na2SO4溶液中c(SO
 )=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=(3)若T2温度下,向水中滴入稀盐酸,测得溶液中c(H+)=1.0×10-3mol/L,则溶液中c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我们生活中处处都与化学有密切关系。
(1)消防员的防毒面具中放有过氧化钠,过氧化钠的作用是____________________ 。
(2)Fe(OH)3胶体可用作净水剂,是因为Fe(OH)3胶体具有________________ ,取少量Fe(OH)3胶体置于试管中,向试管中逐渐滴加稀盐酸至过量,产生的现象为_______________________ 。
(3)洪灾过后,饮用水可用漂白粉消毒。
①工业上将氯气通入石灰乳[Ca(OH)2]中制取漂白粉,反应的化学方程式为___________________ 。
②Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2 是否泄漏,有关反应的化学方程式为3Cl2(g)+8NH3(g)=6NH4Cl+N2(g),若反应中消耗Cl2 1.5 mol,则被氧化的NH3 的体积为_______________________ L(标准状况)。
(1)消防员的防毒面具中放有过氧化钠,过氧化钠的作用是
(2)Fe(OH)3胶体可用作净水剂,是因为Fe(OH)3胶体具有
(3)洪灾过后,饮用水可用漂白粉消毒。
①工业上将氯气通入石灰乳[Ca(OH)2]中制取漂白粉,反应的化学方程式为
②Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2 是否泄漏,有关反应的化学方程式为3Cl2(g)+8NH3(g)=6NH4Cl+N2(g),若反应中消耗Cl2 1.5 mol,则被氧化的NH3 的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】过氧化钠与次氯酸均具有强氧化性和漂白性。
(1)将包有少量Na2O2固体的脱脂棉放在石棉网上,用长玻璃管向脱脂棉中通入微热潮湿的CO2,可以观察到的现象是________ ,该反应中氧化剂与还原剂的物质的量之比为______ 。
(2)次氯酸具有杀菌消毒、漂白作用,但其性质非常不稳定。在氯气与水反应原理的基础上制备漂白粉和漂白液,写出实验室用KMnO4( →Mn2+)和浓盐酸制备氯气的反应中的还原剂是
→Mn2+)和浓盐酸制备氯气的反应中的还原剂是______ (填化学式)。将氯气通入冷的石灰乳中可制备漂白粉,该反应的化学方程式是______ ,漂白粉的有效成分是______ (填化学式),用文字说明其能漂白的原因:_______ 。
(1)将包有少量Na2O2固体的脱脂棉放在石棉网上,用长玻璃管向脱脂棉中通入微热潮湿的CO2,可以观察到的现象是
(2)次氯酸具有杀菌消毒、漂白作用,但其性质非常不稳定。在氯气与水反应原理的基础上制备漂白粉和漂白液,写出实验室用KMnO4(
 →Mn2+)和浓盐酸制备氯气的反应中的还原剂是
→Mn2+)和浓盐酸制备氯气的反应中的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】关注饮用水,保证人民的生活质量。回答下列两个问题:
(1)饮用水中的NO3- 对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
①上述反应中的氧化剂为_________________________________ 。
②上述反应中若生成标况下3.36LN2,则转移的电子数为_____________________________ 。
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上制取氯气的化学反应方程式为_______________________________________________ 。
②漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应的离子方程式为_________________________________________________________________________________________________________________________________________________________________ 。
(1)饮用水中的NO3- 对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
①上述反应中的氧化剂为
②上述反应中若生成标况下3.36LN2,则转移的电子数为
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上制取氯气的化学反应方程式为
②漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应的离子方程式为
您最近一年使用:0次



