将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________ 。
(2)该溶液中NaOH的质量分数为________ 。
(3)从该溶液中取出10 mL,含NaOH的质量为________ ,含NaOH的物质的量为________ 。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________ 。
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中NaOH的质量分数为
(3)从该溶液中取出10 mL,含NaOH的质量为
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为
更新时间:2020-02-23 11:54:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.X、Y、Z三种可溶性盐,其阳离子分别是 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 ,中的某一种。现进行以下实验:
,中的某一种。现进行以下实验:
①将三种盐各取少量,分别溶于盛有5mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
回答下列问题:
(1)根据上述事实,推断这三种盐的化学式:X_______ ,Y_______ ,Z_______ 。
(2)写出下列反应的离子方程式。
X与氢氧化钡溶液反应:_______ 。
Y与盐酸反应:_______ 。
Ⅱ.有关物质的量的计算
(3) 和
和 一定条件下可以发生反应
一定条件下可以发生反应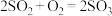 ,若有a mol
,若有a mol  与b mol
与b mol  充分反应,则反应后硫原子与氧原子的个数比为
充分反应,则反应后硫原子与氧原子的个数比为_______ (用含a、b的代数式表示)。
(4)36g CO与 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与 的混合气体的总物质的量为
的混合气体的总物质的量为_______ mol,其中的CO在标准状况下的体积为_______ L。
(5)用质量分数为98%,密度为1.84g/mL的浓硫酸配制1mol/L的稀硫酸500mL,则需用量筒量取浓硫酸的体积为_______ 。
 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 ,中的某一种。现进行以下实验:
,中的某一种。现进行以下实验:①将三种盐各取少量,分别溶于盛有5mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
回答下列问题:
(1)根据上述事实,推断这三种盐的化学式:X
(2)写出下列反应的离子方程式。
X与氢氧化钡溶液反应:
Y与盐酸反应:
Ⅱ.有关物质的量的计算
(3)
 和
和 一定条件下可以发生反应
一定条件下可以发生反应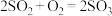 ,若有a mol
,若有a mol  与b mol
与b mol  充分反应,则反应后硫原子与氧原子的个数比为
充分反应,则反应后硫原子与氧原子的个数比为(4)36g CO与
 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与 的混合气体的总物质的量为
的混合气体的总物质的量为(5)用质量分数为98%,密度为1.84g/mL的浓硫酸配制1mol/L的稀硫酸500mL,则需用量筒量取浓硫酸的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识填写下列空白。
(1)在标准状况下,67.2L 是
是_______ mol,质量为_______ g,含有_______ 个 分子。
分子。
(2)在标准状况下,1.7g氨气所占的体积约为_______ L,它与相同条件下_______ mol  含有相同的氢原子数。
含有相同的氢原子数。
(3)某气态氧化物化学式为 ,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(4)在_______ mol  中含0.3mol
中含0.3mol  ,含
,含 约
约_______ 个。
(5)将标准状况下a L的HCl(g)溶于1000g水,得到的盐酸的密度为b ,则该盐酸的物质的量浓度为
,则该盐酸的物质的量浓度为_______  。
。
(6) 个
个 的物质的量为
的物质的量为_______ mol,质量为_______ g。
(1)在标准状况下,67.2L
 是
是 分子。
分子。(2)在标准状况下,1.7g氨气所占的体积约为
 含有相同的氢原子数。
含有相同的氢原子数。(3)某气态氧化物化学式为
 ,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为(4)在
 中含0.3mol
中含0.3mol  ,含
,含 约
约(5)将标准状况下a L的HCl(g)溶于1000g水,得到的盐酸的密度为b
 ,则该盐酸的物质的量浓度为
,则该盐酸的物质的量浓度为 。
。(6)
 个
个 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图为某市售盐酸试剂瓶标签上的部分数据。
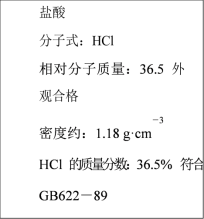
回答下列问题:
(1)该盐酸的物质的量浓度为___________ 。
(2)下列实验操作会导致实验结果偏低的是___________ (填序号)。
①配制 100 g 10%的 CuSO4 溶液,称取 10 g 硫酸铜晶体溶于 90 g 水中;
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮;
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为 0.2 g, 所得溶液的浓度;
④用酸式滴定管量取用 98%,密度为 1.84 g·cm-3 的浓 H2SO4 配制 200 mL 2mol·L-1 的稀 H2SO4 时,先平视后仰视。
(3)已知 CO 和 CO2 的混合气体 14.4 g,在标准状况下所占的体积为 8.96 L。则该混合气体中,CO 的质量为____ g,CO2 的物质的量为______ mol。
(4)1 mol 氧气在放电条件下,有 30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是___________ (填字母)。
A.16 B.17.8 C.18.4 D.35.6
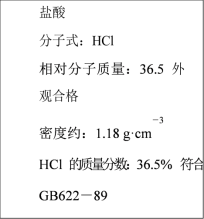
回答下列问题:
(1)该盐酸的物质的量浓度为
(2)下列实验操作会导致实验结果偏低的是
①配制 100 g 10%的 CuSO4 溶液,称取 10 g 硫酸铜晶体溶于 90 g 水中;
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮;
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为 0.2 g, 所得溶液的浓度;
④用酸式滴定管量取用 98%,密度为 1.84 g·cm-3 的浓 H2SO4 配制 200 mL 2mol·L-1 的稀 H2SO4 时,先平视后仰视。
(3)已知 CO 和 CO2 的混合气体 14.4 g,在标准状况下所占的体积为 8.96 L。则该混合气体中,CO 的质量为
(4)1 mol 氧气在放电条件下,有 30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是
A.16 B.17.8 C.18.4 D.35.6
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空:
(1)0. 5 mol NH3分子中所含氮原子数为__________ 个;
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是__________ ;
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是__________ ;
(4)新制氯水在阳光照射下产生的无色气体是__________ ;
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度__________ (选填“偏高、偏低、无影响”);
(6)实验室制备氯气时,收集氯气常采用__________ 法。
(1)0. 5 mol NH3分子中所含氮原子数为
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是
(4)新制氯水在阳光照射下产生的无色气体是
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度
(6)实验室制备氯气时,收集氯气常采用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空。
Ⅰ.现有下列10种物质:①熔融的氢氧化钠②蔗糖③盐酸④金属钠⑤硫酸⑥二氧化硫⑦硫粉⑧石膏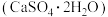 ⑨酒精溶液⑩液氨
⑨酒精溶液⑩液氨
(1)属于电解质的是_______________ (填序号,下同)。
(2)属于非电解质的是_____________ 。
(3)上述状态下能导电的是__________ 。
Ⅱ.已知某“84消毒液”瓶体部分标签如图所示。请回答下列问题:
(1) 的物质的量浓度约为
的物质的量浓度约为________  (保留两位有效数字)。
(保留两位有效数字)。
(2)某同学参阅该“84消毒液”的配方,欲用 固体配制
固体配制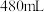 含
含 质量分数为25%的消毒液。下列说法正确的是
质量分数为25%的消毒液。下列说法正确的是___________ (填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器

B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量 固体的质量为
固体的质量为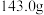
E.配制过程中,定容时俯视刻度线会使得溶液浓度偏大
Ⅰ.现有下列10种物质:①熔融的氢氧化钠②蔗糖③盐酸④金属钠⑤硫酸⑥二氧化硫⑦硫粉⑧石膏
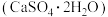 ⑨酒精溶液⑩液氨
⑨酒精溶液⑩液氨(1)属于电解质的是
(2)属于非电解质的是
(3)上述状态下能导电的是
Ⅱ.已知某“84消毒液”瓶体部分标签如图所示。请回答下列问题:
| 84消毒液 [有效成分]  [规格]  [质量分数]25% [密度]  |
(1)
 的物质的量浓度约为
的物质的量浓度约为 (保留两位有效数字)。
(保留两位有效数字)。(2)某同学参阅该“84消毒液”的配方,欲用
 固体配制
固体配制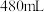 含
含 质量分数为25%的消毒液。下列说法正确的是
质量分数为25%的消毒液。下列说法正确的是A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器

B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量
 固体的质量为
固体的质量为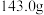
E.配制过程中,定容时俯视刻度线会使得溶液浓度偏大
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)SO2的摩尔质量为_________ ,1mol SO2中含有氧原子的个数为_________ ,标况下5.6L SO2的质量为_______ 。
(2)用20g烧碱配制成500mL溶液,其物质的量浓度为_____________ mol/L;从中取出1mL,其物质的量浓度为_____________________ mol/L;若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为______________ mol/L。
(2)用20g烧碱配制成500mL溶液,其物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列10种物质①熔融的氢氧化钠 ②蔗糖 ③纯净的盐酸 ④金属钠 ⑤硫酸 ⑥二氧化硫 ⑦硫粉 ⑧胆矾 ⑨酒精溶液 ⑩液氮
(1)①属于电解质的有_______
②属于非电解质的有_______
(2)完成以下计算
①等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为___
②配置100mL1mol⋅L−1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g⋅mL−1,质量分数为98%)的体积为___ mL.
(1)①属于电解质的有
②属于非电解质的有
(2)完成以下计算
①等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为
②配置100mL1mol⋅L−1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g⋅mL−1,质量分数为98%)的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】84 消毒液是一种常见的含氯消毒剂。下图为某品牌 84 消毒液的说明书中部分内容。

(1)84 消毒液中含有的物质除了 H2O 还有______________ (用化学式表示)
(2)常温,将氯气通入 NaOH 溶液中可制得“84”消毒液。写出离子方程式:______________ 。
(3)某同学研究 84 消毒液的漂白性,实验如下。
资料:①84 消毒液中含氯微粒主要有 ClO- 、Cl- 、HClO;
②相同浓度时,HClO 的氧化性强于 ClO-;
③ORP 是反映水溶液中所有物质表现出来的氧化—还原性, ORP 值越大,氧化性越强。
Ⅰ.将 2 ml 84 消毒液中加 2 ml 水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.将 2 ml 84 消毒液中加入 2 ml 白醋后,放入红色纸片,观察到纸片迅速褪色。
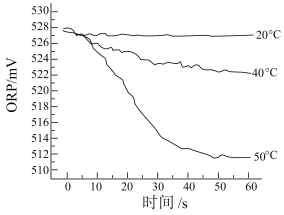
Ⅲ.测得 84 消毒液在不同温度时 ORP 随时间的变化曲线如下图。
① 已知白醋(主要成分 CH3COOH)显酸性,不具有漂白性。结合化学用语和必要的文字说明,解释实验Ⅱ中纸片褪色比实验Ⅰ更快的原因是______________ 。
②实验表明,向84消毒液中加入较多硫酸时会产生氯气,生成氯气的离子方程式是______________ 。
③由实验Ⅲ可得出的结论是______________ 。ORP 值不同的原因可能是 ______________ 。
(4)针对不同物品的消毒,84 消毒液需要稀释到不同的浓度来使用。取次氯酸钠含量为14.9 g/L 的 84 消毒液 1 mL ,加水稀释至 100 mL,则稀释后的溶液中次氯酸钠的物质的量浓度为______________ mol/L。
| 产品特点 本品是以次氯酸钠为有效成分的液体消毒剂。可杀灭肠道致病菌、化脓性球菌、致病性酵母菌,并能灭活病毒。 注意事项 1. 本品易使有色衣物脱色,禁止用于丝、毛、麻织物的消毒。 2. 不得将本品与酸性产品(如洁厕类清洁产品)同时使用。 3. 置于避光、阴凉处保存。 4. 需稀释后使用,勿口服。 |

(1)84 消毒液中含有的物质除了 H2O 还有
(2)常温,将氯气通入 NaOH 溶液中可制得“84”消毒液。写出离子方程式:
(3)某同学研究 84 消毒液的漂白性,实验如下。
资料:①84 消毒液中含氯微粒主要有 ClO- 、Cl- 、HClO;
②相同浓度时,HClO 的氧化性强于 ClO-;
③ORP 是反映水溶液中所有物质表现出来的氧化—还原性, ORP 值越大,氧化性越强。
Ⅰ.将 2 ml 84 消毒液中加 2 ml 水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.将 2 ml 84 消毒液中加入 2 ml 白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得 84 消毒液在不同温度时 ORP 随时间的变化曲线如下图。

① 已知白醋(主要成分 CH3COOH)显酸性,不具有漂白性。结合化学用语和必要的文字说明,解释实验Ⅱ中纸片褪色比实验Ⅰ更快的原因是
②实验表明,向84消毒液中加入较多硫酸时会产生氯气,生成氯气的离子方程式是
③由实验Ⅲ可得出的结论是
(4)针对不同物品的消毒,84 消毒液需要稀释到不同的浓度来使用。取次氯酸钠含量为14.9 g/L 的 84 消毒液 1 mL ,加水稀释至 100 mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
您最近一年使用:0次



