某次硫酸铜晶体结晶水含量的测定实验中,相对偏差为-1.8%,原因可能是
| A.两次称量结果相差0.001g时,即认为达到恒重标准 |
| B.加热后固体颜色有少量变黑 |
| C.粉末未完全变白就停止加热 |
| D.晶体表面有水 |
更新时间:2022-06-02 06:36:45
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.碳酸钡可用于肠胃X射线造影检查 | B.工业上用水吸收 制取 制取 |
| C.工业上用饱和石灰水制备漂白粉 | D.饱和氯水中加入 固体会逸出氯气 固体会逸出氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是
①金属钠投入到FeCl3溶液中 ②过量Ba(OH)2浓溶液和AlNH4(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中 ⑤Na2S2O3溶液中加入稀硫酸
①金属钠投入到FeCl3溶液中 ②过量Ba(OH)2浓溶液和AlNH4(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中 ⑤Na2S2O3溶液中加入稀硫酸
| A.只有①②④⑤ | B.只有③ | C.只有②③ | D.只有①④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列措施不合理 的是
| A.水泥制备时需加入石膏调节水泥硬化速率 |
| B.用硫酸清洗锅炉中的水垢 |
| C.高温下用焦炭还原SiO2制取粗硅 |
| D.常温下,用铁制或铝制容器储运浓硝酸、浓硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】为测定含镁3%~5%的铝镁合金中镁的质量分数,设计了2种实验方案,下列说法不正确 的是
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量m g铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体质量增重。
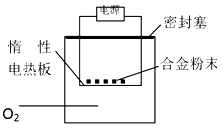
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量m g铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体质量增重。

| A.方案一中若称取5.4 g合金粉末样品,投入V mL 2.0 mol/L NaOH溶液中反应,则V≥100 mL |
| B.方案一中测定剩余固体质量时,过滤后未洗涤固体就干燥、称量,则镁的质量分数偏高 |
| C.方案二中欲计算镁的质量分数,实验中还需测定灼烧后固体的质量 |
| D.方案二中若用空气代替O2进行实验,则测定结果偏高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。下列说法不正确 的是
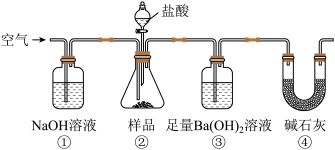

| A.必须在①②间添加吸收HCl的装置 |
| B.④的作用是防止空气中的气体影响实验的精确度 |
| C.通入空气的作用是保证②中产生的气体完全转移到③中 |
| D.称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】通过测定混合气中O2含量可计算已变质的Na2O2(含Na2CO3)纯度,实验装置如图(Q为弹性良好的气囊)。下列分析不正确的是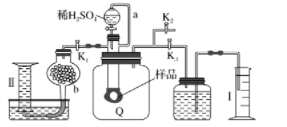

| A.Q气球中产生的气体主要成分为O2、CO2 |
| B.测定气体总体积必须关闭K1、K2,打开K3 |
| C.量筒Ⅰ用于测二氧化碳的量,干燥管b中装入碱石灰,量筒Ⅱ用于测氧气的量 |
| D.读完气体总体积后,打开K2,再缓缓打开K1;可观察到Q气球慢慢缩小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一块钠久置后变质为1.55g钠、氧化钠、过氧化钠的混合物,将此混合物用足量的水溶解后,产生标况下气体336mL,在所得溶液中加入50mL、1mol/L的盐酸,恰呈中性.则原钠块的质量为( )
| A.0.92g | B.1.07g | C.1.15g | D.1.23g |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,在pH=1的某溶液中除H+外还可能有Na+、Fe3+、Fe2+、I-、Cl-、CO 中的几种,现取100 mL该溶液进行如下实验。
中的几种,现取100 mL该溶液进行如下实验。

下列判断正确的是( )
 中的几种,现取100 mL该溶液进行如下实验。
中的几种,现取100 mL该溶液进行如下实验。
下列判断正确的是( )
| A.Fe2+、I-、Cl-三种离子一定存在 |
B.CO 一定不存在,不能确定Na+和Cl-是否存在 一定不存在,不能确定Na+和Cl-是否存在 |
| C.Fe3+与Fe2+至少有一种 |
| D.该溶液中c(Cl-)至少为0.3 mol·L-1 |
您最近一年使用:0次



