有A、B、C、D、E、F、G,7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl3、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。试回答下面问题。(已知AgOH微溶于水)
(1)A的化学式是____ ,G的化学式是_____ 。判断理由是_________________ 。
(2)写出其余几种物质的化学式。B:_____ ,C:_____ ,D:_____ ,E:_____ ,F:_____ 。
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | ↓ | ↓ | ↓ |
| C | - | - | ― | ↓ | — | ↓ | ↓ |
| D | - | ↓ | - | ↓ | ↓ | ↓ | |
| E | - | ↓ | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
(1)A的化学式是
(2)写出其余几种物质的化学式。B:
12-13高二·全国·课时练习 查看更多[2]
更新时间:2016-12-09 04:21:50
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】为除去粗盐中的CaCl2、MgCl2、硫酸盐以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:

(1)第①步中,操作A是__________ ,第⑤步中,操作B是__________ 。
(2)判断试剂X过量的方法是________________________ 。
(3)写出第④步中涉及反应的化学方程式____________________ 。
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、__________ (填化学式)。
(5)此实验方案尚需完善,具体步骤是__________________ 。

(1)第①步中,操作A是
(2)判断试剂X过量的方法是
(3)写出第④步中涉及反应的化学方程式
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、
(5)此实验方案尚需完善,具体步骤是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:
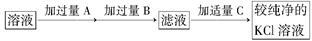
(1)写出三种试剂的化学式:A________ ,B________ ,C________ 。
(2)加过量A的原因是:__________________ ,
有关反应的化学方程式为:__________________ ,_________________ 。
(3)加过量B的原因是:__________________________ ,
有关反应的化学方程式为:_________________________ 。

(1)写出三种试剂的化学式:A
(2)加过量A的原因是:
有关反应的化学方程式为:
(3)加过量B的原因是:
有关反应的化学方程式为:
您最近一年使用:0次
【推荐3】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量K+、Ca2+、Mg2+、SO 等杂质离子,实验室提纯NaCl的流程如图:
等杂质离子,实验室提纯NaCl的流程如图:
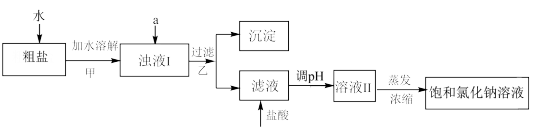
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。
(1)欲除去粗盐溶解后形成溶液中的Ca2+、Mg2+、SO 离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:
离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:____ 、____ 、____ (只填化学式)。为检测SO 离子是否沉淀完全,请你写出检验方法:
离子是否沉淀完全,请你写出检验方法:____ 。
(2)上述流程中,甲、乙两个过程均要用到玻璃棒,玻璃棒的作用分别是甲____ ,乙____ 。
(3)饱和食盐水通过____ 可以得到的NaCl晶体。
(4)食盐是无机化工生产之母,电解饱和食盐水的装置如图所示。

写出电解饱和食盐水的化学方程式____ ;若在U形管中滴加酚酞溶液,电解一段时间后,U形管_____ (填电极“X”或“Y”)边的溶液变红。检验电解食盐水X电极产物的方法是____ ;若电解时消耗了117克氯化钠,则理论上得到氯气的最大体积为____ (标准状况)。
 等杂质离子,实验室提纯NaCl的流程如图:
等杂质离子,实验室提纯NaCl的流程如图:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。
(1)欲除去粗盐溶解后形成溶液中的Ca2+、Mg2+、SO
 离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:
离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为: 离子是否沉淀完全,请你写出检验方法:
离子是否沉淀完全,请你写出检验方法:(2)上述流程中,甲、乙两个过程均要用到玻璃棒,玻璃棒的作用分别是甲
(3)饱和食盐水通过
(4)食盐是无机化工生产之母,电解饱和食盐水的装置如图所示。

写出电解饱和食盐水的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】某无色透明溶液中可能大量存在Ag+、Mg2+、Fe3+、Na+、Cl-、CO32-、OH-和NO3-中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是______ ,有关的离子方程式______ 。
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有______ ,有关的离子方程式为______ 。
(4)综上所述,原溶液中一定存在的离子有______ ,可能存在的离子是______ 。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有
(4)综上所述,原溶液中一定存在的离子有
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】有混合物的水溶液,可能含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 ,现取三份各100mL溶液进行如下实验:
,现取三份各100mL溶液进行如下实验:
①向第一份中加入 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
②向第二份中加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);
③向第三份中加入足量 溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g。
溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g。
试回答下列问题:
(1)肯定存在的离子有_______ ,肯定不存在的离子有_______ 。
(2)可能存在的离子是_______ ,为确定该离子是否存在,可取少许原溶液,然后可以进行如下操作,其中正确的是_______ (填序号)。
a.加入足量硝酸钡溶液,过滤,向滤液中加入足量稀硝酸后再滴加硝酸银溶液
b.先加入足量的硝酸溶液,再滴加硝酸银溶液
c.先加入足量盐酸,再加入氯化钡溶液
(3)试分别确定原溶液中各阳离子的物质的量浓度:_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 ,现取三份各100mL溶液进行如下实验:
,现取三份各100mL溶液进行如下实验:①向第一份中加入
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;②向第二份中加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);
③向第三份中加入足量
 溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g。
溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g。试回答下列问题:
(1)肯定存在的离子有
(2)可能存在的离子是
a.加入足量硝酸钡溶液,过滤,向滤液中加入足量稀硝酸后再滴加硝酸银溶液
b.先加入足量的硝酸溶液,再滴加硝酸银溶液
c.先加入足量盐酸,再加入氯化钡溶液
(3)试分别确定原溶液中各阳离子的物质的量浓度:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】甲同学发布了三份无色溶液检测报告,结果如下(水电离的H+、OH-忽略不计):
溶液(1)中所含全部离子及其浓度
溶液(2)中所含全部离子及其浓度
溶液(3)中所含全部离子及其浓度
试分析判断:上述三份检测结果是否可靠,若不可靠,说出理由。
I.溶液(1)结果是否可靠________ ,理由________ 。
溶液(2)结果是否可靠_________ ,理由________ 。
溶液(3)结果是否可靠_________ ,理由________ 。
II.乙同学对可能含有下列6种离子的溶液进行如下实验:Cl-,SO42-,NH4+,CO32-,K+,Na+;
已知:NH4++OH- NH3↑+H2O
NH3↑+H2O
a.取200mL上述溶液,向其中加入足量BaCl2溶液,反应后将沉淀过滤,洗涤,干燥,得沉淀4.30g,向沉淀中加入足量的盐酸,有2.33g沉淀不溶。
b.向a的滤液中加入足量的NaOH溶液,加热,产生标况下的气体1.12L(假定气体全部逸出 )
(1)溶液中一定存在的离子有_____ ,可能存在的离子有_____ 。
(2)原溶液中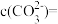
___  ,
,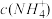
___ 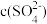 (填“>”“<”“=”,下同)
(填“>”“<”“=”,下同)
(3)如果上述6种离子都存在,则
____ 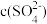 。
。
溶液(1)中所含全部离子及其浓度
| 离子 | 浓度mol/L | 离子 | 浓度mol/L |
| Na+ | 0.1 | Cu2+ | 0.2 |
| Ba2+ | 0.5 | NO3- | 1.5 |
| Mg2+ | 0.3 | Cl- | 0.6 |
| 离子 | 浓度mol/L | 离子 | 浓度mol/L |
| Na+ | 0.1 | Cl- | 0.9 |
| Ag+ | 0.5 | NO3- | 0.3 |
| Mg2+ | 0.3 |
| 离子 | 浓度mol/L | 离子 | 浓度mol/L |
| Na+ | 0.1 | Cl- | 0.2 |
| K+ | 0.5 | NO3- | 0.3 |
| Mg2+ | 0.3 | SO42- | 0.4 |
I.溶液(1)结果是否可靠
溶液(2)结果是否可靠
溶液(3)结果是否可靠
II.乙同学对可能含有下列6种离子的溶液进行如下实验:Cl-,SO42-,NH4+,CO32-,K+,Na+;
已知:NH4++OH-
 NH3↑+H2O
NH3↑+H2Oa.取200mL上述溶液,向其中加入足量BaCl2溶液,反应后将沉淀过滤,洗涤,干燥,得沉淀4.30g,向沉淀中加入足量的盐酸,有2.33g沉淀不溶。
b.向a的滤液中加入足量的NaOH溶液,加热,产生标况下的气体1.12L(假定气体全部逸出 )
(1)溶液中一定存在的离子有
(2)原溶液中
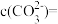
 ,
,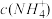
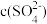 (填“>”“<”“=”,下同)
(填“>”“<”“=”,下同)(3)如果上述6种离子都存在,则

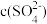 。
。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】有关物质的转化关系如下图所示(部分生成物和反应条件已略去)。A 为由两种元素组成的固体,含非金属质量分数为39.13%;D、E、L均为无色气体,E 和L难溶于水;F 为常见金属;G、I、J焰色反应显黄色;M 为红褐色固体。
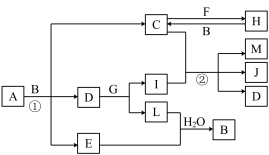
请回答下列问题:
(1)M的化学式为_________ 。
(2)G的电子式为_________ 。
(3)写出反应①的化学方程式:_____________ 。
(4)写出反应②的离子方程式:_____________ 。

请回答下列问题:
(1)M的化学式为
(2)G的电子式为
(3)写出反应①的化学方程式:
(4)写出反应②的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
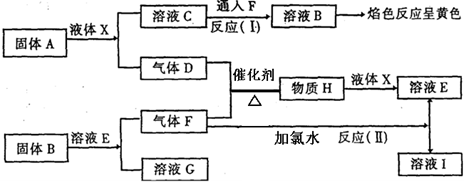
【推荐2】化合物X( )由3种元素组成,某学习小组开展如下探究实验:
)由3种元素组成,某学习小组开展如下探究实验:
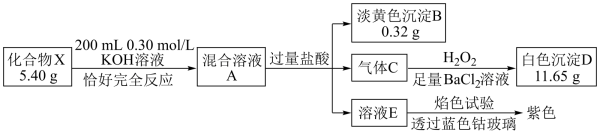
已知:混合溶液A由相对分子质量相差32的甲、乙两种溶质组成;X、甲和乙所含元素完全相同。
请回答:
(1)淡黄色沉淀B的化学式是_______ ,溶液E中所含溶质是_______ (用化学式表示)。
(2)写出气体C生成白色沉淀D的离子方程式_______ 。
(3)写出X与KOH溶液反应的化学方程式_______ 。
(4)实验室常用_______ (填写试剂名称)检验气体C的存在,请写出检验的过程_______ 。
 )由3种元素组成,某学习小组开展如下探究实验:
)由3种元素组成,某学习小组开展如下探究实验:
已知:混合溶液A由相对分子质量相差32的甲、乙两种溶质组成;X、甲和乙所含元素完全相同。
请回答:
(1)淡黄色沉淀B的化学式是
(2)写出气体C生成白色沉淀D的离子方程式
(3)写出X与KOH溶液反应的化学方程式
(4)实验室常用
您最近一年使用:0次