H2SO4具有多种性质,回答下列问题:
(1)浓H2SO4使蔗糖变黑,体现了浓H2SO4的什么性质_______ 。黑色物质为炭粉,炭粉与浓硫酸继续反应的化学方程式为_______ 。
(2)浓H2SO4是常见的气体干燥剂,但它不能干燥H2S和HI,原因是_______ 。
(1)浓H2SO4使蔗糖变黑,体现了浓H2SO4的什么性质
(2)浓H2SO4是常见的气体干燥剂,但它不能干燥H2S和HI,原因是
更新时间:2022-06-28 20:33:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】将下列性质的选项,填入各小题后面对应的括号中:A.脱水性;B.强酸性;C.二元酸;D.氧化性;E.吸水性
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色。( )
(2)NaOH与H2SO4反应,可生成Na2SO4和NaHSO4这两种盐。( )
(3)在冷浓HNO3中放入铝片没明显现象。( )
(4)浓H2SO4敞口久置会增重。( )
(5)用稀硫酸清洗金属表面的氧化物( )
(6)在烧杯中放入蔗糖,滴入浓H2SO4变黑,并产生大量气体。( )
(7)在稀HNO3中放入铜片产生NO。( )
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色。
(2)NaOH与H2SO4反应,可生成Na2SO4和NaHSO4这两种盐。
(3)在冷浓HNO3中放入铝片没明显现象。
(4)浓H2SO4敞口久置会增重。
(5)用稀硫酸清洗金属表面的氧化物
(6)在烧杯中放入蔗糖,滴入浓H2SO4变黑,并产生大量气体。
(7)在稀HNO3中放入铜片产生NO。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)将下列现象中硫酸表现出来的性质填写在空格内:敞口放置的浓硫酸,溶液质量增加_________________ ;浓硫酸与蔗糖放出大量热,并出现黑色固体____________ ;
(2)将一瓶二氧化硫和一瓶硫化氢气体瓶口对接进行混合,瓶壁上能观察到有_________________ 和_________________ 生成,其化学反应方程式为:____________________________ , 此反应中SO2作____________ 剂, 1 mol 二氧化硫和硫化氢完全反应时,有_________ mol电子发生转移。
(3)当雨水的pH________ 时,我们称之为“酸雨”。某环保小组测定某次雨水中硫酸的物质的量浓度为5×10-6 mol/L,这次雨__________ 酸雨(选填“属于”或“不属于”)。常温下若把0.1mol/L的盐酸溶液稀释100倍,此时的溶液的pH=__________ 。
(4)将一充满氨气的大试管倒立在水槽中,可以看到现象_________________ ,说明_______________ ,若在此溶液中滴入酚酞试液,溶液呈_______ 色,其电离方程式___________________________ 。
(2)将一瓶二氧化硫和一瓶硫化氢气体瓶口对接进行混合,瓶壁上能观察到有
(3)当雨水的pH
(4)将一充满氨气的大试管倒立在水槽中,可以看到现象
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据硫元素及其化合物有关知识填空:
(1)往纯净的 溶液中加入
溶液中加入 溶液,溶液
溶液,溶液___________ (填“变”或“不变”)色,再往其中通入氯气,溶液变___________ (填“红”或“黄”)色。
(2)浓硫酸与碳共热时发生反应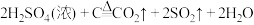 ,在该反应中,浓硫酸表现出
,在该反应中,浓硫酸表现出___________ (填“酸性”或“强氧化性”)。
(3)蓝矾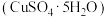 的摩尔质量是
的摩尔质量是___________ (填“160”或“250”) ,把浓硫酸滴在蓝矾固体上,固体表面变
,把浓硫酸滴在蓝矾固体上,固体表面变___________ (填“白”或“黑”),则浓硫酸表现___________ (填“吸水性”或“脱水性”);此反应是___________ (填“物理”或“化学”)变化。
(1)往纯净的
 溶液中加入
溶液中加入 溶液,溶液
溶液,溶液(2)浓硫酸与碳共热时发生反应
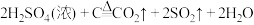 ,在该反应中,浓硫酸表现出
,在该反应中,浓硫酸表现出(3)蓝矾
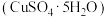 的摩尔质量是
的摩尔质量是 ,把浓硫酸滴在蓝矾固体上,固体表面变
,把浓硫酸滴在蓝矾固体上,固体表面变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。如图是硫元素价类二维图。请回答下列问题:

(1)已知物质 是一种可溶性正盐,能被酸性
是一种可溶性正盐,能被酸性 溶液氧化为
溶液氧化为 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式___________ 。
(2)实验室提供以下试剂: 的浓溶液、
的浓溶液、 的稀溶液、酸性
的稀溶液、酸性 溶液、
溶液、 溶液、
溶液、 、品红溶液。若要实现
、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是___________ 、___________ (填化学式);设计实验,证明能实现该转化的操作和现象为___________ 。
(3)某兴趣小组用如图所示装置模拟空气中二氧化硫含量的测定。当注入标准状况下 空气时,酸性
空气时,酸性 溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为
溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为___________ (用含 代数式表示,体积分数即物质的量分数)。
代数式表示,体积分数即物质的量分数)。

(4)某化工厂用如图所示工艺流程除去燃煤产生的 。
。
①过程Ⅰ发生的反应为 ,其氧化剂与还原剂的质量之比为
,其氧化剂与还原剂的质量之比为___________ 。
②过程Ⅱ发生反应的化学方程式为___________ 。


(1)已知物质
 是一种可溶性正盐,能被酸性
是一种可溶性正盐,能被酸性 溶液氧化为
溶液氧化为 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式(2)实验室提供以下试剂:
 的浓溶液、
的浓溶液、 的稀溶液、酸性
的稀溶液、酸性 溶液、
溶液、 溶液、
溶液、 、品红溶液。若要实现
、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是(3)某兴趣小组用如图所示装置模拟空气中二氧化硫含量的测定。当注入标准状况下
 空气时,酸性
空气时,酸性 溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为
溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为 代数式表示,体积分数即物质的量分数)。
代数式表示,体积分数即物质的量分数)。
(4)某化工厂用如图所示工艺流程除去燃煤产生的
 。
。①过程Ⅰ发生的反应为
 ,其氧化剂与还原剂的质量之比为
,其氧化剂与还原剂的质量之比为②过程Ⅱ发生反应的化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据题意回答下列问题
(1)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·nH2O)等化合物。三硅酸镁的氧化物形式为___________ 。
(2)Al2O3、MgO和SiO2都可以制耐火材料,其原因是___________ (填字母)。
a.Al2O3、MgO和SiO2都是白色固体
b.Al2O3、MgO和SiO2都是金属氧化物
c.Al2O3、MgO和SiO2都有很高的熔点
(3)用浓硫酸给竹筒“刻字”是利用浓硫酸的___________ 性。
(4)写出Cu与浓硫酸在加热条件下反应的化学方程式___________
(5)推测Si、N最简单氢化物的稳定性:___________ 强于___________ (填化学式)。
(1)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·nH2O)等化合物。三硅酸镁的氧化物形式为
(2)Al2O3、MgO和SiO2都可以制耐火材料,其原因是
a.Al2O3、MgO和SiO2都是白色固体
b.Al2O3、MgO和SiO2都是金属氧化物
c.Al2O3、MgO和SiO2都有很高的熔点
(3)用浓硫酸给竹筒“刻字”是利用浓硫酸的
(4)写出Cu与浓硫酸在加热条件下反应的化学方程式
(5)推测Si、N最简单氢化物的稳定性:
您最近一年使用:0次

 :
:
 :
: :
: :
: :
: :
:

