铁
(1)位置与物理性质_______ 。
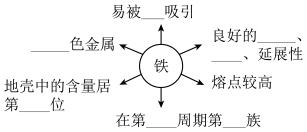
(2)化学性质:比较活泼,常表现变价,重要化学反应为。
(1)位置与物理性质

(2)化学性质:比较活泼,常表现变价,重要化学反应为。
| 铁 | 非金属 |  : : 点燃:  : :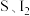 : : |
| 水 | ||
| 酸 |  : :浓硝酸、浓硫酸与铁反应:常温下 | |
| 盐 |  : : : : |
更新时间:2023-03-09 22:06:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。
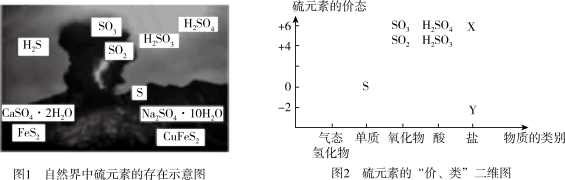
(1)从图1中选择符合图2要求的X、Y代表的物质:X_______ ,Y_______ 。
(2)硫酸是重要的化工原料,查阅资料,工业制硫酸的过程如图:
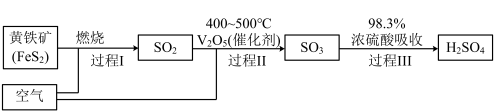
①上述过程中,发生氧化还原反应的是_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
②下列对浓硫酸的叙述不正确的是_______ (填字母)。
a.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
b.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
c.浓硫酸与亚硫酸钠反应制取SO2时,浓硫酸表现出强氧化性
d.过量的锌和浓硫酸反应,产生的气体含有SO2和H2
(3)铜跟浓硫酸反应的化学方程式:_______ ,被还原的元素是_______ 。

(1)从图1中选择符合图2要求的X、Y代表的物质:X
(2)硫酸是重要的化工原料,查阅资料,工业制硫酸的过程如图:

①上述过程中,发生氧化还原反应的是
②下列对浓硫酸的叙述不正确的是
a.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
b.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
c.浓硫酸与亚硫酸钠反应制取SO2时,浓硫酸表现出强氧化性
d.过量的锌和浓硫酸反应,产生的气体含有SO2和H2
(3)铜跟浓硫酸反应的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】某些化学反应可表示为: .请回答下列问题:
.请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式_______
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式_______
(3)若A是金属单质,C是遇空气会变为红棕色的无色气体,写出该反应的离子方程式_______
(4)若C、D均为能使澄清石灰水变浑浊的气体,且D可以使品红褪色,则A与B反应的化学方程式为_______
 .请回答下列问题:
.请回答下列问题:(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式
(3)若A是金属单质,C是遇空气会变为红棕色的无色气体,写出该反应的离子方程式
(4)若C、D均为能使澄清石灰水变浑浊的气体,且D可以使品红褪色,则A与B反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列方程式:
(1)写出一个属于“工业固氮”的化学方程式:_______ 。
(2)硫酸工业中煅烧硫铁矿(FeS2)的化学方程式:_______ 。
(3)NO2与水反应的化学方程式为_______ 。
(4)浓硫酸跟碳反应_______ (用化学方程式表示)。
(5)氨的催化氧化_______ (用化学方程式表示)。
(1)写出一个属于“工业固氮”的化学方程式:
(2)硫酸工业中煅烧硫铁矿(FeS2)的化学方程式:
(3)NO2与水反应的化学方程式为
(4)浓硫酸跟碳反应
(5)氨的催化氧化
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列关于物质用途的说法中,正确的是___________ 。
A.铁的氧化物 Fe2O3、Fe3O4 都只有氧化性
B.Fe2O3常用作油漆、涂料、油墨和橡胶的红色颜料
C.还原铁粉可用于食品的脱氧剂
D.FeO不稳定,在空气里受热,能迅速氧化成Fe3O4
E.磁性氧化铁:四氧化三铁,为红棕色晶体
F.铁红:氧化亚铁,可用作红色油漆的颜料
G.铁的氧化物中 Fe2O3、Fe3O4 都有磁性
H.铁的氧化物FeO、Fe2O3、Fe3O4都可由碱受热分解制得
I.铁粉与水蒸气反应生成黑色的氧化亚铁
A.铁的氧化物 Fe2O3、Fe3O4 都只有氧化性
B.Fe2O3常用作油漆、涂料、油墨和橡胶的红色颜料
C.还原铁粉可用于食品的脱氧剂
D.FeO不稳定,在空气里受热,能迅速氧化成Fe3O4
E.磁性氧化铁:四氧化三铁,为红棕色晶体
F.铁红:氧化亚铁,可用作红色油漆的颜料
G.铁的氧化物中 Fe2O3、Fe3O4 都有磁性
H.铁的氧化物FeO、Fe2O3、Fe3O4都可由碱受热分解制得
I.铁粉与水蒸气反应生成黑色的氧化亚铁
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是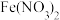 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______________ 。
(2)实验室配制 溶液时,如果没有隔绝空气,
溶液时,如果没有隔绝空气, 会被氧化为
会被氧化为________ (填写化学式)。在该溶液中加入________ 试剂,看到_________ 现象,证明溶液变质。写出检验 已经被氧化的离子方程式
已经被氧化的离子方程式_________ 。
(3)已知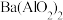 可溶于水,下图表示的是向
可溶于水,下图表示的是向 溶液中逐滴加入
溶液中逐滴加入 溶液时,生成沉淀的物质的量y与加入
溶液时,生成沉淀的物质的量y与加入 的物质的量x的关系。
的物质的量x的关系。

由图可知c点的沉淀是______ (填化学式),a-b过程中沉淀物质的量较大的是____ (填化学式),写出从开始滴加入 溶液至c点的总反应离子方程式
溶液至c点的总反应离子方程式_______ 。
(1)过量的铁和稀硝酸发生反应,产物是
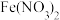 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)实验室配制
 溶液时,如果没有隔绝空气,
溶液时,如果没有隔绝空气, 会被氧化为
会被氧化为 已经被氧化的离子方程式
已经被氧化的离子方程式(3)已知
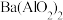 可溶于水,下图表示的是向
可溶于水,下图表示的是向 溶液中逐滴加入
溶液中逐滴加入 溶液时,生成沉淀的物质的量y与加入
溶液时,生成沉淀的物质的量y与加入 的物质的量x的关系。
的物质的量x的关系。
由图可知c点的沉淀是
 溶液至c点的总反应离子方程式
溶液至c点的总反应离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期律的重要性。如表列出了元期表中短周期的一部分,a~i代表9种短周期元素。
已知c与氢元素能组成生活中最常见的化合物X。回答下列问题:
(1)元素h在周期表中位于第_______ 族,g的原子结构示意图为_______ 。
(2)由元素d与e组成的化合物的电子式为_______ 。
(3)a~i中,非金属性最强的是_______ (填元素符号);f、g、h、i四种元素的最高价氧化物对应的水化物中,酸性最强的化合物的化学式为_______ 。
(4)因在元素a的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,a的单质与氧气共热时的化学方程式为_______ 。
(5)一定条件下,铁能与气态X发生反应,该反应的化学方程式为_______ 。
(6)设计实验比较元素i的单质和I2的氧化性,操作与现象是:取2mLKI溶液于试管中,_______ 。
| a | b | c | d | |||
| e | f | g | h | i |
(1)元素h在周期表中位于第
(2)由元素d与e组成的化合物的电子式为
(3)a~i中,非金属性最强的是
(4)因在元素a的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,a的单质与氧气共热时的化学方程式为
(5)一定条件下,铁能与气态X发生反应,该反应的化学方程式为
(6)设计实验比较元素i的单质和I2的氧化性,操作与现象是:取2mLKI溶液于试管中,
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:___________ ;
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:___________ ;
(3)制漂白粉原理:___________ ;
(4)高温下Fe与水蒸气反应:___________ 。
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:___________ ;
(6)Al粉与NaOH溶液反应:___________ ;
(7)酸性条件下,向含铬废水中加FeSO4,将 还原为Cr3+:
还原为Cr3+:___________ ;
(8)制Fe(OH)3胶体:___________ 。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:
(3)制漂白粉原理:
(4)高温下Fe与水蒸气反应:
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:
(6)Al粉与NaOH溶液反应:
(7)酸性条件下,向含铬废水中加FeSO4,将
 还原为Cr3+:
还原为Cr3+:(8)制Fe(OH)3胶体:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是_____ (填序号,下同);属于盐类的是______ ;相互间能发生反应的是________ 。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是_______________ ,该变化称为______ 反应。
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是__________________ 。
(4)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。
“消毒液”与“洁厕灵”同时使用会产生有毒的氯气,写出该反应的离子方程式:____________________________________________ 。
(5)纯碱(Na2CO3)、小苏打(NaHCO3)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程中,小苏打发生分解反应,该反应的化学方程式是_____________________________________ ;苏打饼干可以适当缓解人体胃酸(主要成分盐酸)过多症状,该反应的离子方程式是__________________________________________ 。
(6)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:______________ 。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是
(2)食盐不慎洒落在天然气的火焰上,观察的现象是
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(4)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。
“消毒液”与“洁厕灵”同时使用会产生有毒的氯气,写出该反应的离子方程式:
(5)纯碱(Na2CO3)、小苏打(NaHCO3)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程中,小苏打发生分解反应,该反应的化学方程式是
(6)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
您最近半年使用:0次



