根据硫元素及其化合物有关知识填空:
(1)往纯净的 溶液中加入
溶液中加入 溶液,溶液
溶液,溶液___________ (填“变”或“不变”)色,再往其中通入氯气,溶液变___________ (填“红”或“黄”)色。
(2)浓硫酸与碳共热时发生反应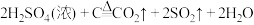 ,在该反应中,浓硫酸表现出
,在该反应中,浓硫酸表现出___________ (填“酸性”或“强氧化性”)。
(3)蓝矾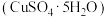 的摩尔质量是
的摩尔质量是___________ (填“160”或“250”) ,把浓硫酸滴在蓝矾固体上,固体表面变
,把浓硫酸滴在蓝矾固体上,固体表面变___________ (填“白”或“黑”),则浓硫酸表现___________ (填“吸水性”或“脱水性”);此反应是___________ (填“物理”或“化学”)变化。
(1)往纯净的
 溶液中加入
溶液中加入 溶液,溶液
溶液,溶液(2)浓硫酸与碳共热时发生反应
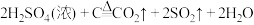 ,在该反应中,浓硫酸表现出
,在该反应中,浓硫酸表现出(3)蓝矾
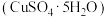 的摩尔质量是
的摩尔质量是 ,把浓硫酸滴在蓝矾固体上,固体表面变
,把浓硫酸滴在蓝矾固体上,固体表面变
更新时间:2024-05-24 15:56:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】补齐物质及其用途的连线如A-b。_______
| 物质 | 用途。 |
| A.乙醇 | a.食品膨松剂 |
| B.浓硫酸 | b.燃料 |
| C.碳酸氢钠 | c.吸水剂 |
| D.蛋白质 | d.基本营养物质 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有两支分别盛有相同体积浓硫酸和稀硫酸的试管,请用简单的方法区别它们._______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有_______ 性。用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有_______ 性。硝酸应保存在棕色试剂瓶中,这是因为硝酸具有_______ 性。
(2)硝酸铜是制备CuZnAl系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是_______ (填序号)。
①Cu+HNO3(浓)→Cu(NO3)2
②Cu+HNO3(稀)→Cu(NO3)2
③Cu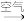 CuO
CuO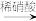 Cu(NO3)2
Cu(NO3)2
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式_______ 。
(4)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解。写出该反应的化学方程式_______ 。
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
(2)硝酸铜是制备CuZnAl系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是
①Cu+HNO3(浓)→Cu(NO3)2
②Cu+HNO3(稀)→Cu(NO3)2
③Cu
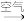 CuO
CuO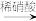 Cu(NO3)2
Cu(NO3)2(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式
(4)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解。写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)硫酸被人们誉为“化学工业之母”,在国民生产中发挥着重要作用。硫酸的性质有:A.高沸点;B.强酸性;C.吸水性;D.脱水性;E.强氧化性。在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
①硫酸可用作气体干燥剂___________ ;
②往晶体硫酸铜中加液硫酸,晶体变白___________ ;
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑___________ ;
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生___________ ;
⑤浓硫酸与FeO反应____________ ;
⑥运用铁制槽车和铝制槽车送输浓硫酸___________ 。
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
___ C1O2-+__NO+____=Cl-+____NO3-+______。
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:_____________________ 。
①硫酸可用作气体干燥剂
②往晶体硫酸铜中加液硫酸,晶体变白
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生
⑤浓硫酸与FeO反应
⑥运用铁制槽车和铝制槽车送输浓硫酸
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硫酸是三大工业用酸之一,在冶金、石油工业、制药、国防等方面都要用到硫酸。将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。试回答:
(1)加入少量水的原因是_________________________________________________ 。
(2)生成的黑色物质是______________ (写出化学式)。
(3)“体积膨胀,并放出有刺激性气味的气体(SO2)”,写出对应的化学方程式:_________________________________________________ 。
(4)上述现象体现了浓硫酸的_________________ (填序号)
①酸性 ②吸水性 ③脱水性 ④强氧化性
(5)向80mL浓硫酸中加入5.6g铜,加热一段时间后至不再反应为止,实验测得反应中共有1.12L(标准状况下)SO2气体生成,该反应的化学方程式为_____________________________________ ,反应中转移电子______ mol,铜剩余_______ g,该反应中浓硫酸体现了___________ 和__________ 。
(1)加入少量水的原因是
(2)生成的黑色物质是
(3)“体积膨胀,并放出有刺激性气味的气体(SO2)”,写出对应的化学方程式:
(4)上述现象体现了浓硫酸的
①酸性 ②吸水性 ③脱水性 ④强氧化性
(5)向80mL浓硫酸中加入5.6g铜,加热一段时间后至不再反应为止,实验测得反应中共有1.12L(标准状况下)SO2气体生成,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】写出下列反应的化学方程式
①浓硫酸与木炭反应的化学方程式_______ 。
②浓硝酸与铜粉反应的离子方程式_______ 。
③NH3与稀硝酸反应的离子方程式_______ 。
①浓硫酸与木炭反应的化学方程式
②浓硝酸与铜粉反应的离子方程式
③NH3与稀硝酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨基磺酸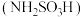 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
(1)由尿素 与发烟硫酸(用
与发烟硫酸(用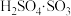 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为_______ 。
(2)氨基磺酸在高温时的分解反应为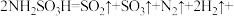
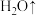 。
。
①检验该混合产物中含有 的试剂是
的试剂是_______ (填序号)。
A.品红溶液 B. 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液
②高温时,该反应中转移2mol电子时,生成气体的总物质的量是_______ mol。
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为_______ 。
②下列有关浓硫酸和浓硝酸的说法正确的是_______ (填序号)。
A.浓硫酸可用于干燥 、
、 、HI
、HI
B.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
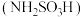 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。(1)由尿素
 与发烟硫酸(用
与发烟硫酸(用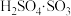 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为(2)氨基磺酸在高温时的分解反应为
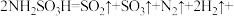
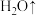 。
。①检验该混合产物中含有
 的试剂是
的试剂是A.品红溶液 B.
 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液②高温时,该反应中转移2mol电子时,生成气体的总物质的量是
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为
②下列有关浓硫酸和浓硝酸的说法正确的是
A.浓硫酸可用于干燥
 、
、 、HI
、HIB.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知铜和浓硫酸可以在加热条件下发生反应
(1)请写出该反应化学方程式___________ 。
(2)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为___________ 。
(3)一定量的铜片与含1.2mol的 的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为
的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为___________ L(假设气体全部逸出)。
(4)将(3)中反应后所得的溶液稀释后与足量的 溶液反应,所得沉淀的质量为
溶液反应,所得沉淀的质量为___________ g。
(1)请写出该反应化学方程式
(2)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为
(3)一定量的铜片与含1.2mol的
 的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为
的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为(4)将(3)中反应后所得的溶液稀释后与足量的
 溶液反应,所得沉淀的质量为
溶液反应,所得沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】磷酸亚铁锂 电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除
电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除 外,还含有
外,还含有 箔、少量其他不溶物)得到
箔、少量其他不溶物)得到 晶体等资源。
晶体等资源。
(1) 中铁元素的化合价为
中铁元素的化合价为_________ 。
(2) 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为________________________________________ 。
(3)能将 氧化为
氧化为 的试剂是
的试剂是_________ (填序号)。
A. B.稀硫酸 C.铜
B.稀硫酸 C.铜
(4)若溶液中含有 ,加入试剂
,加入试剂________________ (填化学式)时溶液变为红色。
 电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除
电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除 外,还含有
外,还含有 箔、少量其他不溶物)得到
箔、少量其他不溶物)得到 晶体等资源。
晶体等资源。(1)
 中铁元素的化合价为
中铁元素的化合价为(2)
 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为(3)能将
 氧化为
氧化为 的试剂是
的试剂是A.
 B.稀硫酸 C.铜
B.稀硫酸 C.铜(4)若溶液中含有
 ,加入试剂
,加入试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学工作者经常从不同的角度来预测某些物质的性质,然后进行实验验证,得出结论。某化学研究小组根据H2O2中氧元素的化合价,预测H2O2具有氧化性和还原性,并设计如下实验进行验证。请根据实验室提供的试剂以及相关实验内容选择合适的化学试剂进行实验验证,并对主要的实验现象进行描述,写出相关反应的离子方程式。
提供的试剂有:FeCl2溶液,酸性KMnO4溶液,KSCN溶液
(1)请完成表中①~⑤的相关内容
(2)请用一个化学方程式表示出H2O2既有氧化性又有还原性_______ 。
提供的试剂有:FeCl2溶液,酸性KMnO4溶液,KSCN溶液
(1)请完成表中①~⑤的相关内容
| 验证H2O2的性质 | 选用的化学试剂 | 主要的实验现象 | 发生反应的离子方程式 |
| 还原性 | ① | ② | 略 |
| 氧化性 | ③ | ④ | ⑤ |
(2)请用一个化学方程式表示出H2O2既有氧化性又有还原性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某兴趣小组研究I2与FeCl2溶液的反应。
配制FeCl2溶液:向0.1 mol·L-1FeCl3溶液中加入足量铁粉,充分振荡,备用。
(1)FeCl3溶液与铁粉反应的离子方程式是________ 。
(2)检验FeCl3完全反应的实验方案是____________ 。
(3)设计如下实验,研究I2是否能够氧化FeCl2:
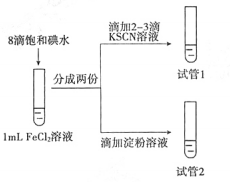
实验现象:试管1溶液变红,试管2溶液呈现较浅的蓝色。
实验结论:I2能够氧化FeCl2。
①有的同学认为上述实验现象不足以得出上述结论,原因是________ 。
②欲证实实验结论,再次设计对比实验。实验方案和相应的现象是________ 。
(4)继续进行实验:
①针对Ⅱ中现象,小组同学提出假设:在一定量KI的存在下,I-+I2 I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):
I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):____________

②应用化学平衡移动原理,结合离子方程式,解释实验I中溶液红色褪去的原因:_______________________ 。
配制FeCl2溶液:向0.1 mol·L-1FeCl3溶液中加入足量铁粉,充分振荡,备用。
(1)FeCl3溶液与铁粉反应的离子方程式是
(2)检验FeCl3完全反应的实验方案是
(3)设计如下实验,研究I2是否能够氧化FeCl2:

实验现象:试管1溶液变红,试管2溶液呈现较浅的蓝色。
实验结论:I2能够氧化FeCl2。
①有的同学认为上述实验现象不足以得出上述结论,原因是
②欲证实实验结论,再次设计对比实验。实验方案和相应的现象是
(4)继续进行实验:
| 实验 | 实验操作 | 实验现象 |
| I | 向试管1中加入KI固体,充分振荡 | 溶液红色完全褪去,变为黄色。 |
| Ⅱ | 向I中所得的黄色溶液中加入0.5mL CCl4,充分振荡、静置 | 水层仍为黄色,CCl4层几乎无色。 |
①针对Ⅱ中现象,小组同学提出假设:在一定量KI的存在下,I-+I2
 I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):
I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):
②应用化学平衡移动原理,结合离子方程式,解释实验I中溶液红色褪去的原因:
您最近一年使用:0次



