回答下列问题:
(1)地下钢管连接镁块是金属防腐措施中的_______ 法。
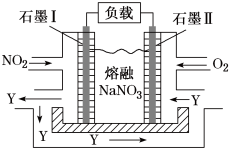
(2)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的_______ 极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为_______ 。
(3)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_______ 。
②铅蓄电池放电时的正极反应式为_______ ,当电路中有2mol电子转移时,理论上两电极质量变化的差值为_______ g。
(1)地下钢管连接镁块是金属防腐措施中的
(2)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的

(3)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
②铅蓄电池放电时的正极反应式为
更新时间:2022-06-10 16:01:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】根据电化学知识回答下列问题:
(1)如图所示,在不同的电解质溶液中可以组成不同的电池。

①当电解质溶液为稀硫酸时,Fe电极是________ (填“正”或“负”)极,其电极反应式为__________ 。
②当电解质溶液为NaOH溶液时,Al电极是________ (填“正”或“负”) 极,其电极反应式为_________ 。
③若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是______ (填“正”或“负”)极,其电极反应式为_______________________________ 。
(2)请你利用原电池原理,设计实验,比较铜和银的金属活动性。画出实验装置图,标出正负极、电子流动方向。________

(1)如图所示,在不同的电解质溶液中可以组成不同的电池。

①当电解质溶液为稀硫酸时,Fe电极是
②当电解质溶液为NaOH溶液时,Al电极是
③若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是
(2)请你利用原电池原理,设计实验,比较铜和银的金属活动性。画出实验装置图,标出正负极、电子流动方向。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铝作为一种应用广泛的金属,在电化学领域发挥着举足轻重的作用。回答下列问题:
(1)某同学根据氧化还原反应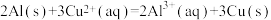 设计如图所示的原电池:
设计如图所示的原电池:

A溶液溶质的化学式为_______ ;电极Y材料的化学式为_______ ;盐桥中的阴离子向_______ (填化学式)溶液中移动。
(2)新型电池中的铝电池类型较多。
①Li-Al/FeS是一种二次电池,可用于车载电源,其电池总反应为 ,充电时锂电极连接电源的
,充电时锂电极连接电源的_______ 极,充电时阳极的电极反应式为_______ 。
②Al—空气燃料电池可用作电动汽车的电源,该电池多使用NaOH溶液为电解液。电池工作过程中,电路中通过3mol电子时,电解质溶液质量的变化为_______ 。
③A1-AgO(氧化高银)电池可用作水下动力电源。该电池反应的化学方程式为
 ,当电极上析出2.16gAg时,铝电极质量减少
,当电极上析出2.16gAg时,铝电极质量减少_______ g。
(1)某同学根据氧化还原反应
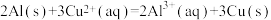 设计如图所示的原电池:
设计如图所示的原电池:
A溶液溶质的化学式为
(2)新型电池中的铝电池类型较多。
①Li-Al/FeS是一种二次电池,可用于车载电源,其电池总反应为
 ,充电时锂电极连接电源的
,充电时锂电极连接电源的②Al—空气燃料电池可用作电动汽车的电源,该电池多使用NaOH溶液为电解液。电池工作过程中,电路中通过3mol电子时,电解质溶液质量的变化为
③A1-AgO(氧化高银)电池可用作水下动力电源。该电池反应的化学方程式为

 ,当电极上析出2.16gAg时,铝电极质量减少
,当电极上析出2.16gAg时,铝电极质量减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】依据原电池原理,回答下列问题:
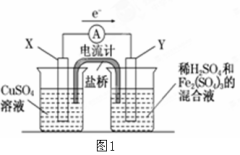

(1)图1是依据氧化还原反应:Cu(s)+2Fe3+(aq)=Cu2+(aq)+2Fe2+(aq)设计的原电池装置。
①电极X的材料是________ (填化学名称);电极Y的材料是__________ (填化学名称)。
②Y电极发生的电极反应式为:______________ 。
(2)图2是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2-离子(O2+4e―→2O2-)。
①c电极为______________ 极。(填“正”或“负”)
②d电极上的电极反应式为___________________________ 。
③如果消耗甲烷160g,假设化学能完全转化为电能,则转移电子的数目为______________ (用NA表示),需要消耗标准状况下氧气的体积为_______ L。


(1)图1是依据氧化还原反应:Cu(s)+2Fe3+(aq)=Cu2+(aq)+2Fe2+(aq)设计的原电池装置。
①电极X的材料是
②Y电极发生的电极反应式为:
(2)图2是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2-离子(O2+4e―→2O2-)。
①c电极为
②d电极上的电极反应式为
③如果消耗甲烷160g,假设化学能完全转化为电能,则转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯 铝电池是一种新型的燃料电池,电解质溶液是
铝电池是一种新型的燃料电池,电解质溶液是 。试完成下列问题:
。试完成下列问题:
 通入
通入 的电极是
的电极是___________ 极 填“正”或“负”
填“正”或“负” 。
。
 铝电极是
铝电极是___________ 极 填“正”或“负”
填“正”或“负” 。
。
 电子从
电子从___________  填“Al”或“
填“Al”或“ ”,下同
”,下同 极流向
极流向___________ 极。
 该装置将能
该装置将能___________ 转化为___________ 能。
 铝电池是一种新型的燃料电池,电解质溶液是
铝电池是一种新型的燃料电池,电解质溶液是 。试完成下列问题:
。试完成下列问题: 通入
通入 的电极是
的电极是 填“正”或“负”
填“正”或“负” 。
。 铝电极是
铝电极是 填“正”或“负”
填“正”或“负” 。
。 电子从
电子从 填“Al”或“
填“Al”或“ ”,下同
”,下同 极流向
极流向 该装置将能
该装置将能
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学能转化为电能的原理的发现和各式各样电池装置的发明,是贮能和功能技术的巨大进步。
回答下列问题:
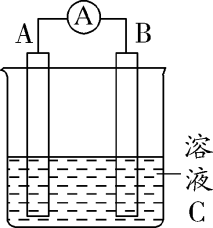
(1)上图中C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为__________________ ,反应进行一段时间后溶液C的pH将___________ (填“升高”“降低”或“基本不变”)。
(2)若将反应Cu +2Ag+=2Ag +Cu2+按图1所示设计一个原电池装置,则负极A的材料为___________ ,溶液C为___________ ,当导线上有2.5mole-流过时,正极生成银的质量为________________ 。
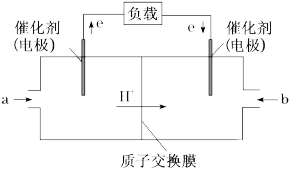
(3)下图为甲烷(CH4)燃料电池的构造示意图,d 电极是___________ (填“正极”或“负极”),C电极的反应方程式为___________________________ 。
回答下列问题:
(1)上图中C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若将反应Cu +2Ag+=2Ag +Cu2+按图1所示设计一个原电池装置,则负极A的材料为
(3)下图为甲烷(CH4)燃料电池的构造示意图,d 电极是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铅蓄电池在日常生活中应用广泛。回答下列问题:
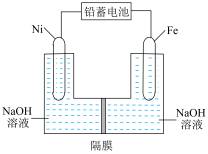
(1)现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移 电子时铁电极的质量减少
电子时铁电极的质量减少 ,则:
,则:
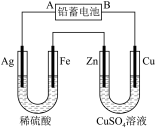
①A是铅蓄电池的___________ 极。
②Cu电极的电极反应式是___________ , 溶液的浓度
溶液的浓度___________ (填“减小”“增大”或“不变”)。
(2)铅蓄电池的 可以用石墨为电极,
可以用石墨为电极, 和
和 的混合溶液为电解液制取。阳极发生的电极反应式为
的混合溶液为电解液制取。阳极发生的电极反应式为___________ 。
(3)将 溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应:
溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应: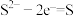 ,
, 。
。
电解时阴极的电极反应式:___________ ,电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成___________ 。
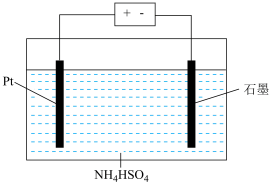
(4) 是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出
是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出 电极发生的电极反应为:
电极发生的电极反应为:___________ 。
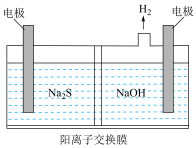
(5)工业上常采用催化还原法和碱吸收法处理 气体。当吸收液失去吸收能力后通入
气体。当吸收液失去吸收能力后通入 可得到
可得到 溶液,用如图所示装置电解所得
溶液,用如图所示装置电解所得 溶液可制得强氧化剂
溶液可制得强氧化剂 。
。
请写出电解 溶液的化学方程式
溶液的化学方程式___________ 。
(1)现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移
 电子时铁电极的质量减少
电子时铁电极的质量减少 ,则:
,则:
①A是铅蓄电池的
②Cu电极的电极反应式是
 溶液的浓度
溶液的浓度(2)铅蓄电池的
 可以用石墨为电极,
可以用石墨为电极, 和
和 的混合溶液为电解液制取。阳极发生的电极反应式为
的混合溶液为电解液制取。阳极发生的电极反应式为(3)将
 溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应:
溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应: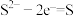 ,
, 。
。
电解时阴极的电极反应式:
(4)
 是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出
是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出 电极发生的电极反应为:
电极发生的电极反应为:
(5)工业上常采用催化还原法和碱吸收法处理
 气体。当吸收液失去吸收能力后通入
气体。当吸收液失去吸收能力后通入 可得到
可得到 溶液,用如图所示装置电解所得
溶液,用如图所示装置电解所得 溶液可制得强氧化剂
溶液可制得强氧化剂 。
。
请写出电解
 溶液的化学方程式
溶液的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】生物电池具有工作时不发热、不损坏电极等优点,不但可以节约大量金属,而且寿命比化学电源长的多,因此越来越受到人们的青睐。某生物电池以葡萄糖(C6H12O6)作原料,在酶的作用下被氧化为葡萄糖酸(C6H12O7),其工作原理如图所示。
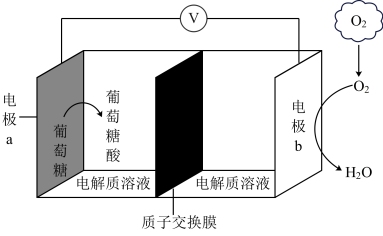
(1)电极b为___________ (填“正极”或“负极”),电极a的电极反应式为___________ 。
(2)该生物电池中发生反应的化学方程式为___________ ,当有2molH+通过质子交换膜时,理论上需要标准状况下氧气的体积为___________ L。
(3)该电池___________ (填“能”或“不能”)在高温条件下使用,原因是___________ 。

(1)电极b为
(2)该生物电池中发生反应的化学方程式为
(3)该电池
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列要求回答问题。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
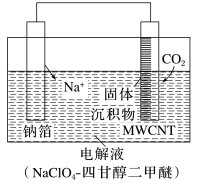
①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是___________ 。
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
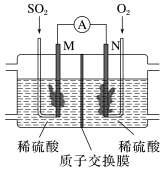
①M极发生的电极反应式为___________ 。
②质子交换膜右侧的溶液在反应后pH___________ (填“增大”“减小”或“不变”)。
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量___________ (填“增大”或“减小”)___________ g。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。

①M极发生的电极反应式为
②质子交换膜右侧的溶液在反应后pH
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电化学普遍应用于生活和生产中,前途广泛,是科研的重点方向。
(1)铅蓄电池为常见的二次电池,其原理为 ,放电时铅蓄电池的正极反应式为
,放电时铅蓄电池的正极反应式为___________ ,该电池充电时原负极应接外接电源的___________ 极。
(2)工业上采用Fe、C为电极电解 溶液制
溶液制 。电解时,应以
。电解时,应以___________ 作阴极,电解过程中阴极附近溶液pH将会___________ (填“增大”、“减小”或“不变”),电解时阳极反应式为___________ ,总反应的化学方程式为___________ 。
(3)根据下图装置信息填空:

①乙池中电极反应式为___________ 。
②当电池反应转移0.2mol电子时,甲池溶液质量增加___________ 。
(1)铅蓄电池为常见的二次电池,其原理为
 ,放电时铅蓄电池的正极反应式为
,放电时铅蓄电池的正极反应式为(2)工业上采用Fe、C为电极电解
 溶液制
溶液制 。电解时,应以
。电解时,应以(3)根据下图装置信息填空:

①乙池中电极反应式为
②当电池反应转移0.2mol电子时,甲池溶液质量增加
您最近一年使用:0次



