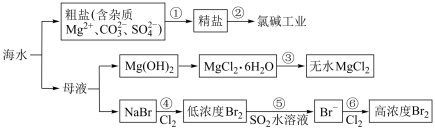
以海水等为原料,可以制备一系列物质,如图所示。下列说法错误的是
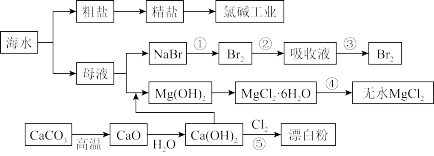

| A.Cl2、漂白粉和SO2均可以漂白有色物质,且其漂白原理不同 |
B.粗盐中含有Ca2+、Mg2+、 等杂质离子,精制时依次加入试剂为Na2CO3、NaOH、BaCl2溶液 等杂质离子,精制时依次加入试剂为Na2CO3、NaOH、BaCl2溶液 |
| C.电解海水提取的盐还可冶炼钠、钾、镁等金属 |
| D.步骤①中已经获得Br2,步骤②中又将获得的Br2还原为Br-,其目的是富集Br2,提高Br2的浓度 |
更新时间:2022-06-11 20:12:47
|
相似题推荐
【推荐1】下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A. | 检验新制氯水中含有HClO | 向新制氯水中加入少量CaCO3 |
| B. | 证明SO2具有还原性 | 向SO2水溶液中通入H2S气体 |
| C. | 检验钠与H2O反应产物NaOH | 将绿豆粒大小的钠投入盛有适量水的烧杯中,滴加稀盐酸 |
| D. | 证明SO2具有漂白性 | 将SO2通入品红溶液中,品红溶液褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】锥形瓶中装有部分变质的漂粉精粉末和红色纸花,向其中注射浓盐酸,观察到纸花褪色,并有黄绿色气体生成,该实验可以得到的结论是


| A.说明Ca(ClO)2具有漂白性 |
| B.实验中发生了氧化还原反应和化合反应 |
| C.浓盐酸被氧化 |
| D.反应中生成的气体只有Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验能达到相应实验目的的是
| 选项 | 试剂 | 实验目的 | 实验装置 | ||
| X | Y | Z | |||
| A | Na2SO3 | 稀HNO3 | 品红溶液 | 证明SO2具有漂白性 | 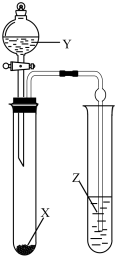 |
| B | MnO2 | 浓盐酸 | KI-淀粉溶液 | 比较Cl2与I2的氧化性强弱 | |
| C | NaCl | 浓硫酸 | AgNO3溶液 | 证明酸性:H2SO4>HCl | |
| D | 蔗糖 | 浓硫酸 | 溴水 | 证明浓硫酸具有脱水性、氧化性 | |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关物质的性质与用途对应关系错误的是
| A.浓硫酸具有吸水性,可用于干燥氨气 |
| B.Na2O2能与CO2反应,可用作供氧剂 |
| C.SO2具有漂白性,可用于漂白纸浆 |
| D.SiC熔点高,可用作耐高温材料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 海水提盐后的母液中含有 、Br-、
、Br-、 、
、 等离子,为获得Br2,可进行如下操作:制取Cl2,向母液中通入Cl2,向反应后的溶液中鼓入热空气并用Na2CO3溶液吸收(所得吸收液中含Br-、
等离子,为获得Br2,可进行如下操作:制取Cl2,向母液中通入Cl2,向反应后的溶液中鼓入热空气并用Na2CO3溶液吸收(所得吸收液中含Br-、 等离子),向溶液中滴加稀硫酸酸化,蒸馏后获得Br2。下列海水提溴过程中反应的离子方程式,书写
等离子),向溶液中滴加稀硫酸酸化,蒸馏后获得Br2。下列海水提溴过程中反应的离子方程式,书写不正确 的是
 、Br-、
、Br-、 、
、 等离子,为获得Br2,可进行如下操作:制取Cl2,向母液中通入Cl2,向反应后的溶液中鼓入热空气并用Na2CO3溶液吸收(所得吸收液中含Br-、
等离子,为获得Br2,可进行如下操作:制取Cl2,向母液中通入Cl2,向反应后的溶液中鼓入热空气并用Na2CO3溶液吸收(所得吸收液中含Br-、 等离子),向溶液中滴加稀硫酸酸化,蒸馏后获得Br2。下列海水提溴过程中反应的离子方程式,书写
等离子),向溶液中滴加稀硫酸酸化,蒸馏后获得Br2。下列海水提溴过程中反应的离子方程式,书写A.用MnO2和浓盐酸制氯气: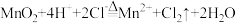 |
B.母液中通入Cl2: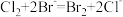 |
C.用Na2CO3溶液吸收Br2: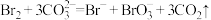 |
D.向吸收液中滴加稀硫酸: |
您最近一年使用:0次
【推荐2】海洋中有丰富的食品、矿产、能源、药物和水产资源等,某化学兴趣小组模拟从海水获取化学资源的方案设计如下。下列有关说法正确的是


A.第①步中除去粗盐中的 、 、 、 、 等杂质,加入药品的顺序可以为: 等杂质,加入药品的顺序可以为: 溶液→ 溶液→ 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
| B.工业上制取金属钠可以通过电解饱和食盐水实现 |
C.在第③步反应的离子方程式为: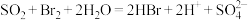 |
| D.第④步反应可以向吸收液中通入氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】制备相关物质,涉及的反应原理及部分流程不合理的是
A.制溴:浓缩海水 Br2 Br2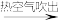 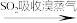 HBr溶液 HBr溶液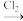 Br2 Br2 |
B.制取镁:海水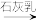    溶液 溶液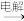 Mg Mg |
C.加热分解Ag2O冶炼Ag:2Ag2O 4Ag+O2↑ 4Ag+O2↑ |
D.制碘:干海带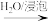 浸出液 浸出液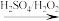 碘水 碘水 含I2苯溶液 含I2苯溶液 单质碘 单质碘 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下图海水综合利用的工业流程图,判断下列说法错误的是
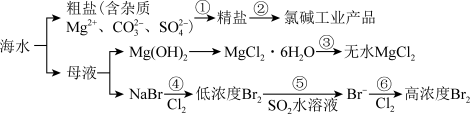
已知: 受热生成Mg(OH)Cl和HCl气体等。
受热生成Mg(OH)Cl和HCl气体等。

已知:
 受热生成Mg(OH)Cl和HCl气体等。
受热生成Mg(OH)Cl和HCl气体等。| A.过程①的提纯是物理变化 |
B.由母液得到无水 的过程中仅发生非氧化还原反应 的过程中仅发生非氧化还原反应 |
| C.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
D.在过程④、⑥反应中每氧化0.2mol  理论上需消耗7.1g 理论上需消耗7.1g  |
您最近一年使用:0次