影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
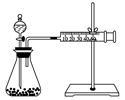
(1)该同学的实验目的是________________________ ;要得出正确的实验结论,还需控制的实验条件是________________________________________ 。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用上图装置进行定量实验。完成该实验应选用的实验药品是____________________________ ;应该测定的实验数据是________________________________________________________________________ 。
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在酸性高锰酸钾溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是________ 的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是________ 。
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol·L-1硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢:Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快 |

(1)该同学的实验目的是
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用上图装置进行定量实验。完成该实验应选用的实验药品是
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在酸性高锰酸钾溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
10-11高一下·辽宁·期中 查看更多[6]
(已下线)2010-2011学年辽宁省师大附中高一下学期期中考试化学试卷(已下线)2011-2012学年湖北省武汉市五校高二上学期期中统考化学试卷(已下线)2012-2013学年新疆乌鲁木齐市一中高一(平行班)下学期期中考试化学试卷(已下线)2012年鲁科版高中化学选修6 2反应条件对化学反应的影响练习卷(已下线)2013届新疆乌鲁木齐市一中高一下学期平行班期中考试化学试卷安徽省合肥市第十一中学2020-2021学年高二上学期第一次月考化学试题
更新时间:2016-12-09 04:24:29
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用 与稀硫酸反应来制取
与稀硫酸反应来制取 时,常加入少量
时,常加入少量 溶液来加快反应速率。为了研究
溶液来加快反应速率。为了研究 的量对
的量对 生成速率的影响,某同学设计了下表实验方案,将表中所给的试剂按一定体积混合后,将大小相同的
生成速率的影响,某同学设计了下表实验方案,将表中所给的试剂按一定体积混合后,将大小相同的 片(过量)分别放入三个反应容器(甲、乙、丙)中,收集产生的气体,并记录收集等体积气体所需的时间。
片(过量)分别放入三个反应容器(甲、乙、丙)中,收集产生的气体,并记录收集等体积气体所需的时间。
(已知:Zn和生成的Cu形成了原电池后可使反应速率加快)
回答下列问题:
(1)Zn和生成的Cu形成的原电池中,Cu为电池的_______ (填“正极”或“负极”),写出Zn极的电极反应式:_______ 。
(2)表中V1_______ (填“>”、“<”或“=”)20mL,V1=_______ mL。
(3)丙组实验中,反应结束后,溶液中c( )
)____  (不考虑混合溶液体积的变化)。
(不考虑混合溶液体积的变化)。
(4)t1_______ (填“>”、“<”或“=”)t3,原因是_______ 。
 与稀硫酸反应来制取
与稀硫酸反应来制取 时,常加入少量
时,常加入少量 溶液来加快反应速率。为了研究
溶液来加快反应速率。为了研究 的量对
的量对 生成速率的影响,某同学设计了下表实验方案,将表中所给的试剂按一定体积混合后,将大小相同的
生成速率的影响,某同学设计了下表实验方案,将表中所给的试剂按一定体积混合后,将大小相同的 片(过量)分别放入三个反应容器(甲、乙、丙)中,收集产生的气体,并记录收集等体积气体所需的时间。
片(过量)分别放入三个反应容器(甲、乙、丙)中,收集产生的气体,并记录收集等体积气体所需的时间。| 实验试剂 | 甲 | 乙 | 丙 |
 的硫酸/mL 的硫酸/mL | 20 | 20 | 20 |
 的 的 溶液/ 溶液/ | 0 | 2.5 | 10 |
 | V1 | V2 | 0 |
| 收集气体所需时间/s | t1 | t2 | t3 |
回答下列问题:
(1)Zn和生成的Cu形成的原电池中,Cu为电池的
(2)表中V1
(3)丙组实验中,反应结束后,溶液中c(
 )
) (不考虑混合溶液体积的变化)。
(不考虑混合溶液体积的变化)。(4)t1
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】I.用如图所示的装置进行制取NO实验(已知Cu与HNO3的反应是放热反应)。

(1)在检查装置的气密性后,向试管a中加入10mL6mol/L稀HNO3和lgCu片,然后立即用带导管的橡皮塞塞紧试管口。请写出Cu与稀HNO3反应的化学方程式:_________ 。
(2)实验过程中通常在开始反应时反应速率缓慢,随后逐渐加快,这是由于_________ ,进行一段时间后速率又逐渐减慢,原因是_________ 。
(3)欲较快地制得NO,可采取的措施是_________。
II.为了探究几种气态氧化物的性质,某同学设计了以下实验:
用三只集气瓶收集满二氧化硫、二氧化氮气体。倒置在水槽中,然后分别缓慢通入适量氧气或氯气,如图所示。一段时间后,A、B装置中集气瓶中充满溶液,C装置中集气瓶里还有气体。

(4)写出C水槽中反应的化学方程式:____________ 。
(5)写出B水槽里发生氧化还原反应的离子方程式:____________ 。
(6)如果装置A中通入的氧气恰好使液体充满集气瓶,假设瓶内液体不扩散,气体摩尔体积为aL/mol,集气瓶中溶液的物质的量浓度为________ 。

(1)在检查装置的气密性后,向试管a中加入10mL6mol/L稀HNO3和lgCu片,然后立即用带导管的橡皮塞塞紧试管口。请写出Cu与稀HNO3反应的化学方程式:
(2)实验过程中通常在开始反应时反应速率缓慢,随后逐渐加快,这是由于
(3)欲较快地制得NO,可采取的措施是_________。
| A.加热 | B.使用铜粉 | C.稀释HNO3 | D.改用浓HNO3 |
II.为了探究几种气态氧化物的性质,某同学设计了以下实验:
用三只集气瓶收集满二氧化硫、二氧化氮气体。倒置在水槽中,然后分别缓慢通入适量氧气或氯气,如图所示。一段时间后,A、B装置中集气瓶中充满溶液,C装置中集气瓶里还有气体。

(4)写出C水槽中反应的化学方程式:
(5)写出B水槽里发生氧化还原反应的离子方程式:
(6)如果装置A中通入的氧气恰好使液体充满集气瓶,假设瓶内液体不扩散,气体摩尔体积为aL/mol,集气瓶中溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HN03的用量为25.0mL、大理石用量为10.00g。
(1)请完成以下实验设计表,在实验目的一栏中填出对应的实验编号:
(2)实验①中CO2质量随时间变化的关系见图:
依据反应方程式CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,计算实验①在70~90s范围内HNO3的平均反应速率_______ 。(忽略溶液体积变化)
(3)请在上图中,画出实验②和③中CO2质量随时间变化关系的预期结果示意图,并标出线的序号_______ 。
(4)工业上已实现CO2和H2反应生成甲醇的转化。已知:在一恒温、恒容密闭容器中充入1mol CO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。测得CO2和CH3OH (g)的浓度随时间变化如下图所示。请回答:
①达到平衡时H2的转化率为_______ 。在前10min内,用CO2表示的反应速率:V(CO2)=______ mol/(L·min)
②能判断该反应达到化学平衡状态的依据是_______ 。
a.容器压强不变b.混合气体中c(CO2)不变
c. v(CH3OH)=v(H2O) d. c(CH3OH)=c(H2O)
(1)请完成以下实验设计表,在实验目的一栏中填出对应的实验编号:
| 试验编号 | T/K | 大理石规格 | HNO3浓度mol/L | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | 实验①和②探究HNO3浓度对该反应速率的影响; (II)实验①和 (III)实验①和 |
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |
(2)实验①中CO2质量随时间变化的关系见图:
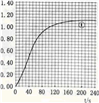
依据反应方程式CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,计算实验①在70~90s范围内HNO3的平均反应速率
(3)请在上图中,画出实验②和③中CO2质量随时间变化关系的预期结果示意图,并标出线的序号
(4)工业上已实现CO2和H2反应生成甲醇的转化。已知:在一恒温、恒容密闭容器中充入1mol CO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。测得CO2和CH3OH (g)的浓度随时间变化如下图所示。请回答:
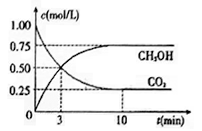
①达到平衡时H2的转化率为
②能判断该反应达到化学平衡状态的依据是
a.容器压强不变b.混合气体中c(CO2)不变
c. v(CH3OH)=v(H2O) d. c(CH3OH)=c(H2O)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入____ 极 (填a或b)。a极发生电极反应式为:____________
II.某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下( 累计值,体积已换算成标准状态) :
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大_______ ,原因是______________
(2)哪一时间段的反应速率最小________ ,原因是_________________________ 。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率( 设溶液体积不变)________
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:
A. 蒸馏水 B. NaCl溶液C. Na2CO3溶液D. CuSO4溶液
可行的是(填编号)________
II.某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下( 累计值,体积已换算成标准状态) :
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一时间段的反应速率最小
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率( 设溶液体积不变)
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:
A. 蒸馏水 B. NaCl溶液C. Na2CO3溶液D. CuSO4溶液
可行的是(填编号)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究小组为比较Al和Fe的金属性强弱,设计了图1所示的装置,甲中锥形瓶内盛放的是100ml稀盐酸(反应前后溶液体积变化可以忽略不计)。
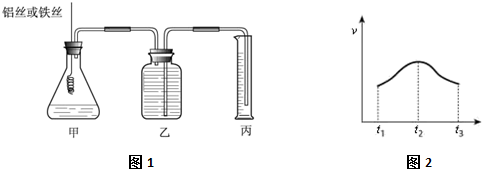
(1)若要比较产生气体的快慢有两种方法,一种是比较产生相同体积气体所需的时间,另一种是比较_____________ ;
(2)实验测得产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间内速率逐渐加快说明该反应是_____________________ (填放热或吸热)反应,t2~t3时间内速率逐渐减慢的主要原因是_________________ ;
(3)如果在相同条件下,把甲锥形瓶内盛放稀盐酸改成H+浓度相同的稀硫酸,发现反应会比原来慢许多,原因可能是______________________________________________________ ;(写出合理的一种即可)

(1)若要比较产生气体的快慢有两种方法,一种是比较产生相同体积气体所需的时间,另一种是比较
(2)实验测得产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间内速率逐渐加快说明该反应是
(3)如果在相同条件下,把甲锥形瓶内盛放稀盐酸改成H+浓度相同的稀硫酸,发现反应会比原来慢许多,原因可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
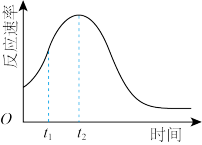
【推荐3】某小组利用H2C2O4溶液与用硫酸酸化的KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
(1)该实验是通过___ 来判断反应的快慢。
(2)已知H2C2O4被KMnO4(H+)氧化为CO2逸出,该反应的化学方程式为___ ,为了观察到实验现象从而判断反应的快慢,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4):n(KMnO4)≥___ 。
(3)探究温度对化学反应速率影响的实验编号是__ 和__ (填编号,下同),可探究H2C2O4浓度对化学反应速率影响的实验编号是__ 和__ 。
(4)实验①测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=__ 。
(5)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:___ ,若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是___ (填序号)
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.氯化锰
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 蒸馏水 体积/ml | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | |||
| ① | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 25 |
| ② | 0.50 | a | 0.010 | 4.0 | c | 25 |
| ③ | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 50 |
(2)已知H2C2O4被KMnO4(H+)氧化为CO2逸出,该反应的化学方程式为
(3)探究温度对化学反应速率影响的实验编号是
(4)实验①测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=
(5)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.氯化锰

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学课外兴趣小组探究过氧化钠与水的反应,探究过程如下:
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因_______ 。
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用_______ 检验该气体,则证明该反应过程中生成了_______ (填化学式)使溶液褪色。
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为_______ 。
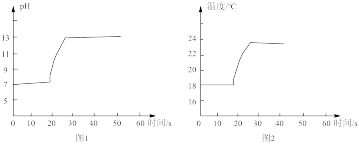
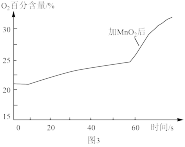
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。
根据图象,得出结论:过氧化钠与水反应过程的方程式为_______ 、_______ 。
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。


根据图象,得出结论:过氧化钠与水反应过程的方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】研发二氧化碳的碳捕集和碳利用技术及合成氨是科学研究热点问题,回答下列问题:
Ⅰ.CO2催化加氢制取甲醇,反应如下:
主反应: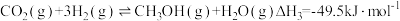
副反应: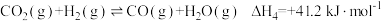
(1)则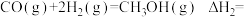
___________ kJ∙mol-1,该反应在___________ (填“高温”“低温”或“任意温度”)下能自发进行。
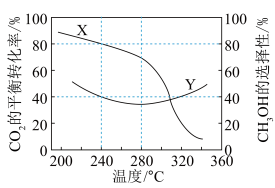
(2)在一定条件下,向某1L恒容密闭容器中充入1mol CO2和amol H2发生反应,起始总压强为21.2MPa.实验测得CO2的平衡转化率和平衡时CH3OH的选择性随温度变化如图所示: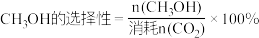 。
。
图中表示平衡时CH3OH的选择性的曲线为___________ (填“X”或“Y”),温度高于 280℃时,曲线 Y 随温度升高而升高的原因是___________ 。240℃时,反应20 min容器内达到平衡状态,副反应的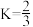 ,初始充入H2的物质的量a =
,初始充入H2的物质的量a = ___________ mol。
(3)工业利用N2 、H2催化合成氨实现了人类“向空气中要面包”的梦想。原料气(含N2 、H2 、CO)中的 CO 能被催化剂吸附,需经过铜氨液处理除去,反应为: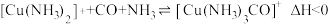 。
。
①除去原料气中 CO 的理由是___________ 。
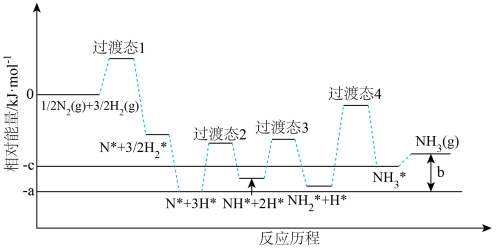
②研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。该反应历程中最大活化能对应步骤的化学方程式为___________ 。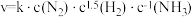 (k 为速率常数)。c (NH3 )的指数为负数的原因是
(k 为速率常数)。c (NH3 )的指数为负数的原因是___________ 。
Ⅰ.CO2催化加氢制取甲醇,反应如下:
主反应:
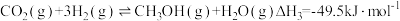
副反应:
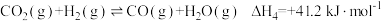
(1)则
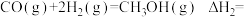
(2)在一定条件下,向某1L恒容密闭容器中充入1mol CO2和amol H2发生反应,起始总压强为21.2MPa.实验测得CO2的平衡转化率和平衡时CH3OH的选择性随温度变化如图所示:
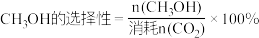 。
。图中表示平衡时CH3OH的选择性的曲线为
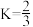 ,初始充入H2的物质的量a =
,初始充入H2的物质的量a = (3)工业利用N2 、H2催化合成氨实现了人类“向空气中要面包”的梦想。原料气(含N2 、H2 、CO)中的 CO 能被催化剂吸附,需经过铜氨液处理除去,反应为:
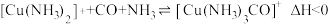 。
。①除去原料气中 CO 的理由是
②研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。该反应历程中最大活化能对应步骤的化学方程式为
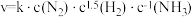 (k 为速率常数)。c (NH3 )的指数为负数的原因是
(k 为速率常数)。c (NH3 )的指数为负数的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在加热、加压条件下,利用金属锰的水热反应可将CO2转化为甲酸(HCOOH),转化关系示意图如下:
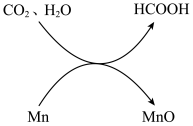
(1)HCOOH的官能团是羧基。HCOOH分子中与碳原子形成共价键的原子的数目是_______ 。
(2)转化过程可认为分两步反应进行:
反应I. Mn + H2O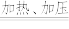 MnO + H2↑; 反应Ⅱ. ……
MnO + H2↑; 反应Ⅱ. ……
写出加热、加压条件下反应Ⅱ的化学方程式:_______ 。
(3)反应一段时间后,生成HCOOH的速率增大,可能的原因是_______ (填字母)。
A.反应放热使温度升高
B.反应I得到的MnO对HCOOH的生成有催化作用
C.H2能将MnO转化为MnO2

(1)HCOOH的官能团是羧基。HCOOH分子中与碳原子形成共价键的原子的数目是
(2)转化过程可认为分两步反应进行:
反应I. Mn + H2O
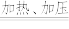 MnO + H2↑; 反应Ⅱ. ……
MnO + H2↑; 反应Ⅱ. ……写出加热、加压条件下反应Ⅱ的化学方程式:
(3)反应一段时间后,生成HCOOH的速率增大,可能的原因是
A.反应放热使温度升高
B.反应I得到的MnO对HCOOH的生成有催化作用
C.H2能将MnO转化为MnO2
您最近一年使用:0次



