人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产。某化学兴趣小组在实验室利用如图装置制备氨气并探究相关性质。
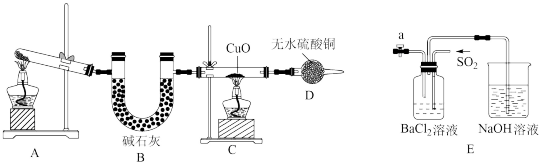
(1)该实验中A装置制备 的化学方程式是
的化学方程式是_______ 。
(2)D装置后接尾气吸收装置。下列能用来吸收尾气的装置是_______ (填装置序号)。
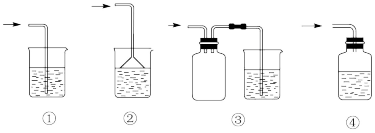
(3)若将D与a相连,在E中产生白色沉淀。其化学式为:_______ 。若向a处单独通入_______ (填下列气体字母编号),在E中也会产生白色沉淀。
A. B.
B. C.
C. D.
D.
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:_______ ;若充分反应后红色固体有剩余,再加入下列的_______ (填字母)试剂,固体又可以继续溶解。
A.稀 B.
B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
②已知 也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:
也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:_______ 。

(1)该实验中A装置制备
 的化学方程式是
的化学方程式是(2)D装置后接尾气吸收装置。下列能用来吸收尾气的装置是

(3)若将D与a相连,在E中产生白色沉淀。其化学式为:
A.
 B.
B. C.
C. D.
D.
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:
A.稀
 B.
B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液②已知
 也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:
也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:
更新时间:2022-07-13 07:28:33
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】依据图1中氮元素及其化合物的转化关系,回答问题:
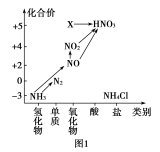
(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_________ 。
(2)下列试剂不能用于干燥NH3的是__________ 。
A.浓硫酸 B.碱石灰 C.NaOH固体
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO的化学方程式为______________ 。
②NO→NO2反应的实验现象是____________ 。
③NO2+H2O→HNO3中氧化剂与还原剂物质的量之比为______ 。
(4)图1中,实验室只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为_____ 。
(5)若要将NH3→N2,从原理上看,下列试剂可行的是______ 。
A.O2 B.Na C.NH4Cl D.NO2

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
(2)下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO的化学方程式为
②NO→NO2反应的实验现象是
③NO2+H2O→HNO3中氧化剂与还原剂物质的量之比为
(4)图1中,实验室只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为
(5)若要将NH3→N2,从原理上看,下列试剂可行的是
A.O2 B.Na C.NH4Cl D.NO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氨气具有广泛的用途。
(1)工业上合成氨反应的化学方程式是___________________________________ 。
(2)实验室常用如下图所示装置制取并收集氨气。

①实验室制取氨气反应的化学方程式是_______________________________ 。
②图中方框内收集氨气的装置可选用___________ (填字母序号)。
③尾气处理装置中使用倒扣漏斗的作用是_____________________________ 。
(3)工业上用NH3制取NO反应的化学方程式是____________________________ 。
(1)工业上合成氨反应的化学方程式是
(2)实验室常用如下图所示装置制取并收集氨气。

①实验室制取氨气反应的化学方程式是
②图中方框内收集氨气的装置可选用
③尾气处理装置中使用倒扣漏斗的作用是
(3)工业上用NH3制取NO反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮化钙(Ca3N2)是一种重要的化学试剂,具有耐高温、导热性好等优良性质,被广泛应用于新型陶瓷工业等领域。实验室拟用单质钙与氮气反应制备氮化钙,并测定产品纯度。已知氮化钙为棕色固体,在空气中会被氧化,遇水强烈水解,产生刺激性气味气体。
I.氮化钙的制备

(1)装置A中反应生成N2,离子方程式为___________ 。
(2)装置B中玻璃仪器为酒精灯、___________ 。
(3)选用上图中的装置制备氮化钙,其连接顺序为:A→___________ (注:焦性没食子酸有还原性、图中装置可重复选用)。
(4)装置A中生成N2的作用为:
①作为反应物与钙反应生成Ca3N2;
②___________ 。
II.产品纯度的测定
用如下装置测定产品纯度。实验时,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体,测得P装置反应后增重3.4g(已知Ca3N2摩尔质量为148g/mol,产品中所含的杂质不与NaOH浓溶液反应)。

(5)装置M中发生反应的化学方程式为___________ 。
(6)根据实验数据计算产品的纯度为___________ 。
(7)通过该实验方案测得的产品纯度偏低,请分析主要原因为___________ 。
I.氮化钙的制备

(1)装置A中反应生成N2,离子方程式为
(2)装置B中玻璃仪器为酒精灯、
(3)选用上图中的装置制备氮化钙,其连接顺序为:A→
(4)装置A中生成N2的作用为:
①作为反应物与钙反应生成Ca3N2;
②
II.产品纯度的测定
用如下装置测定产品纯度。实验时,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体,测得P装置反应后增重3.4g(已知Ca3N2摩尔质量为148g/mol,产品中所含的杂质不与NaOH浓溶液反应)。

(5)装置M中发生反应的化学方程式为
(6)根据实验数据计算产品的纯度为
(7)通过该实验方案测得的产品纯度偏低,请分析主要原因为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答:
(1)用氯化磷(PH4Cl)和NaOH反应制取PH3的化学方程式_______
(2)PH3在空气中会自然得到P2O5,0.2molPH3会消耗O2_______ mol。
(3)氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂。COS水解及部分应用流程如下(部分产物已略去)
COS H2S
H2S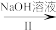 Na2S
Na2S M溶液+H2
M溶液+H2
①组成COS和PH3的各原子中,原子半径最大的元素为_______ ,在周期表中的位置是__ 。
②COS与CO2的结构相似,则COS的电子式为_______ 。
③已知M溶液中硫元素的主要存在形式为 ,则反应III中生成
,则反应III中生成 的离子方程式为
的离子方程式为_______
④如图是反应III中,在不同反应温度下,反应时间与H2产量的关系(初始含Na2S量为3mol)。由图象分析可知,a点时M溶液中除 外,还有
外,还有_______ (填含硫微粒的离子符号)

(1)用氯化磷(PH4Cl)和NaOH反应制取PH3的化学方程式
(2)PH3在空气中会自然得到P2O5,0.2molPH3会消耗O2
(3)氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂。COS水解及部分应用流程如下(部分产物已略去)
COS
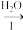 H2S
H2S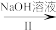 Na2S
Na2S M溶液+H2
M溶液+H2①组成COS和PH3的各原子中,原子半径最大的元素为
②COS与CO2的结构相似,则COS的电子式为
③已知M溶液中硫元素的主要存在形式为
 ,则反应III中生成
,则反应III中生成 的离子方程式为
的离子方程式为④如图是反应III中,在不同反应温度下,反应时间与H2产量的关系(初始含Na2S量为3mol)。由图象分析可知,a点时M溶液中除
 外,还有
外,还有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】研究氮的循环和转化对生产、生活有重要的价值。
I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下所示。

(1)设备1中发生反应的化学方程式是_______ ,实验室用消石灰和氯化铵固体制取NH3,该反应的化学方程式为_______ ;
(2)在工业上,可用浓氨水检验输送氯气的管道是否漏气,若漏气则有白烟生成,写出反应的化学方程式_______ 。设备2中通入的物质A是_______ 。
II.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

(3)过程①的目的是将NH 转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH
转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH 转化为NH3·H2O的离子方程式
转化为NH3·H2O的离子方程式_______ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素的物质化学式为_______ 。
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用以下哪种溶液以达到去除余氯的目的_______ (填序号)。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下所示。

(1)设备1中发生反应的化学方程式是
(2)在工业上,可用浓氨水检验输送氯气的管道是否漏气,若漏气则有白烟生成,写出反应的化学方程式
II.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH
 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
(3)过程①的目的是将NH
 转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH
转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH 转化为NH3·H2O的离子方程式
转化为NH3·H2O的离子方程式(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素的物质化学式为
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用以下哪种溶液以达到去除余氯的目的
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋是一个远未充分开发的巨大化学资源宝库。下列是海水的综合利用示意图,请回答:

(1)I是海水的淡化,主要方法有_______ 、_______ 等。
(2)II是海水提镁,流程如下:

参考下表中三种试剂的信息,步骤①最好选用的试剂是_______ 。
步骤②的化学方程式为_______ 。
(3)III可以通过侯氏制碱法实现,其中使用的原料有氨气,写出实验室制取氨气的化学方程式_______ 。

(1)I是海水的淡化,主要方法有
(2)II是海水提镁,流程如下:

参考下表中三种试剂的信息,步骤①最好选用的试剂是
| 试剂 | 氢氧化钾 | 氢氧化钠 | 氢氧化钙 |
| 价格(元/吨) | 6160 | 2300 | 580 |
(3)III可以通过侯氏制碱法实现,其中使用的原料有氨气,写出实验室制取氨气的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学利用实验室中几种等浓度(相同体积的溶液里含相同数目的溶质)溶液:
①NaOH溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液,进行以下实验。
溶液,进行以下实验。
(1)将表格补充完整。a___________ b___________
(2)该同学认为从理论上即可推测①与④不反应,依据是:___________
(3)写出②与④发生反应的离子反应方程式:___________
(4)该同学认为①与②可发生反应但无明显现象,因此选用以上给出的四种溶液设计了简单实验证明了反应确实发生。将该同学的实验方案补充完整:向盛有2mL①的试管中加入1mL②,___________ (从操作、现象、结论方面描述)。
①NaOH溶液 ②
 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液,进行以下实验。
溶液,进行以下实验。| 序号 | 操作 | 现象 | 离子方程式 |
| ⅰ | 向盛有2mL①的试管中加入1mL③ | 产生蓝色沉淀 | a |
| ⅱ | 向盛有2mL②的试管中加入1mL④ | b |
(2)该同学认为从理论上即可推测①与④不反应,依据是:
(3)写出②与④发生反应的离子反应方程式:
(4)该同学认为①与②可发生反应但无明显现象,因此选用以上给出的四种溶液设计了简单实验证明了反应确实发生。将该同学的实验方案补充完整:向盛有2mL①的试管中加入1mL②,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】孔雀石主要成分是Cu2(OH)2CO3,还含少量FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
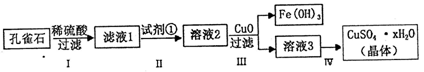
(1)步骤I中涉及的主要反应用离子方程式表示为___________ .
(2)步骤Ⅱ中试剂①是_______ (填代号).
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO 的目的是_________
(4)步骤Ⅳ获得硫酸铜晶体,需要经过_____________ 冷却结晶、过滤等操作.
(5)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.41g硫酸铜晶体,在____ (填实验仪器名称)中加热至质量不再改变时,称量粉末的质量为1.6g.则计算得x=______ (计算结果精确到0.1)

(1)步骤I中涉及的主要反应用离子方程式表示为
(2)步骤Ⅱ中试剂①是
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO 的目的是
(4)步骤Ⅳ获得硫酸铜晶体,需要经过
(5)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.41g硫酸铜晶体,在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】过氧化物在生活和生产中用途广泛,过氧化氢和过氧化钙是常见的过氧化物。
Ⅰ.过氧化钙( )微溶于水,可作医用防腐剂、消毒剂,以下是制备
)微溶于水,可作医用防腐剂、消毒剂,以下是制备 的一种方法
的一种方法

回答下列问题:
(1)步骤Ⅰ中反应的离子方程式是___________ 。
(2)步骤II中反应的化学方程式是:___________ ,反应在冰水浴中进行,是为了防止 挥发、
挥发、___________ (答1条即可)。
(3)待 结晶析出后通过
结晶析出后通过___________ (填操作)分离。
(4) 与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是
与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是___________ 。 还可用于长途运输鱼苗,这体现了
还可用于长途运输鱼苗,这体现了 的
的___________ (填字母)性质。
A.可缓慢供氧 B.能吸收鱼苗呼出的 C.能潮解 D.可抑菌
C.能潮解 D.可抑菌
Ⅱ.实验室利用废旧电池的铜帽制备 的部分实验步骤如下:
的部分实验步骤如下:

(5)“溶解Ⅰ”中反应的离子方程式为___________ ,其中 表现出的性质是
表现出的性质是___________ 。
Ⅰ.过氧化钙(
 )微溶于水,可作医用防腐剂、消毒剂,以下是制备
)微溶于水,可作医用防腐剂、消毒剂,以下是制备 的一种方法
的一种方法
回答下列问题:
(1)步骤Ⅰ中反应的离子方程式是
(2)步骤II中反应的化学方程式是:
 挥发、
挥发、(3)待
 结晶析出后通过
结晶析出后通过(4)
 与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是
与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是 还可用于长途运输鱼苗,这体现了
还可用于长途运输鱼苗,这体现了 的
的A.可缓慢供氧 B.能吸收鱼苗呼出的
 C.能潮解 D.可抑菌
C.能潮解 D.可抑菌Ⅱ.实验室利用废旧电池的铜帽制备
 的部分实验步骤如下:
的部分实验步骤如下:
(5)“溶解Ⅰ”中反应的离子方程式为
 表现出的性质是
表现出的性质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氯酸钾(KClO3)和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。
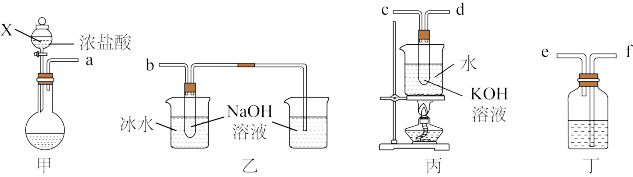
回答下列问题:
(1)仪器X名称是________ ,甲装置圆底烧瓶中的试剂为K2Cr2O7固体,写出发生反应的离子方程式________ 。
(2)为达成实验目的,上述仪器口连接顺序依次为:a-_________ 。
(3)丁装置中所盛试剂为_______ ;乙装置中采用冰水浴冷却的目的是_______ 。
(4)反应结束,取出b中试管,经冷却结晶,_____ ,______ ,干燥,得到KClO3晶体。
(5)为进一步测定所得KClO3晶体的纯度,设计了如下实验方案:
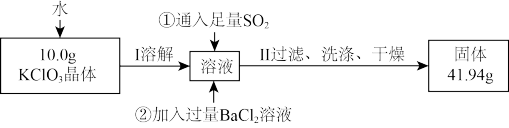
写出通入足量SO2时,溶液中发生反应的离子方程式_________ 。依据上述实验结果,测得该晶体的纯度为_________ 。

回答下列问题:
(1)仪器X名称是
(2)为达成实验目的,上述仪器口连接顺序依次为:a-
(3)丁装置中所盛试剂为
(4)反应结束,取出b中试管,经冷却结晶,
(5)为进一步测定所得KClO3晶体的纯度,设计了如下实验方案:

写出通入足量SO2时,溶液中发生反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】无水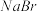 的制备流程如下:
的制备流程如下:

已知:①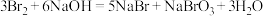 ;
;
② 溶于
溶于 溶液生成
溶液生成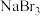 ,离子方程式可表示为
,离子方程式可表示为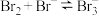 。
。
请回答:
(1) “反应I”所用 溶液最好是饱和溶液,理由是
溶液最好是饱和溶液,理由是____________
(2)已知“热还原”反应中,氧化剂和还原剂物质的量之比为 ,若该反应中消耗了
,若该反应中消耗了 碳粉,则理论上最终可制得
碳粉,则理论上最终可制得 的质量为
的质量为_____________ (不考虑制备过程中的损失)。
(3)“脱色”过程中生成了两种强酸,写出该过程的离子方程式:______________________
(4)用 与
与 溶液反应是制备
溶液反应是制备 的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:
的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:___________________
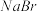 的制备流程如下:
的制备流程如下:
已知:①
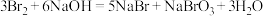 ;
;②
 溶于
溶于 溶液生成
溶液生成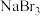 ,离子方程式可表示为
,离子方程式可表示为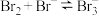 。
。请回答:
(1) “反应I”所用
 溶液最好是饱和溶液,理由是
溶液最好是饱和溶液,理由是(2)已知“热还原”反应中,氧化剂和还原剂物质的量之比为
 ,若该反应中消耗了
,若该反应中消耗了 碳粉,则理论上最终可制得
碳粉,则理论上最终可制得 的质量为
的质量为(3)“脱色”过程中生成了两种强酸,写出该过程的离子方程式:
(4)用
 与
与 溶液反应是制备
溶液反应是制备 的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:
的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:

(1)装置甲中发生反应的化学方程式为_______ ,盛装浓盐酸的仪器的名称为_______ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为_______ (填a或b);装置乙和丙盛装的试剂分别是_______ 。(填名称)
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的离子方程式为:_______ ,有同学认为装置己还有一个作用,该作用为_______ ,发挥该作用_______ (填“能”或“不能”)用澄清石灰水代替。
(4)装置戊中盛装石灰乳用来制备漂白粉,则
①装置戊中发生反应的化学方程式为:_______ 。
②装置戊中采用冰水浴的原因是_______ 。
③漂白粉长时间暴露在空气中容易发生变质的原因为_______ (结合化学方程式说明)。

(1)装置甲中发生反应的化学方程式为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的离子方程式为:
(4)装置戊中盛装石灰乳用来制备漂白粉,则
①装置戊中发生反应的化学方程式为:
②装置戊中采用冰水浴的原因是
③漂白粉长时间暴露在空气中容易发生变质的原因为
您最近一年使用:0次



