海洋资源的综合利用是21世纪海祥开发利用的重点发展领域之一、从海水中可以制取氯、溴、镁等多种化工产品。在元素周期表中,溴(Br)位于第四周期,与Cl同主族。氯气可用于海水提溴,其工艺流程如下:
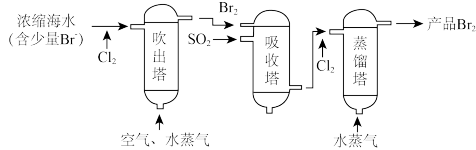
(1)进入吹出塔前海水中的 与
与 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2)已知: 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含____ (写离子符号)。
(3)两次通入 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得 ,理论上需消耗
,理论上需消耗_______ 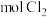 。
。
(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:
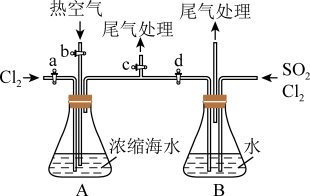
①进行吹出塔中实验时,应关闭活塞_______ ,打开活塞_______ 。
②可根据_______ (填现象),简单判断热空气的流速,通入热空气能吹出 的原因是
的原因是_______ 。
③装置B中要先通入 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 ,已反应完全的依据:
,已反应完全的依据:_______ 。

(1)进入吹出塔前海水中的
 与
与 发生反应的离子方程式为
发生反应的离子方程式为(2)已知:
 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含(3)两次通入
 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得 ,理论上需消耗
,理论上需消耗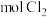 。
。(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:

①进行吹出塔中实验时,应关闭活塞
②可根据
 的原因是
的原因是③装置B中要先通入
 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 ,已反应完全的依据:
,已反应完全的依据:
更新时间:2022-07-15 18:22:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】18世纪下叶,科学家在实验室里把软锰矿和浓盐酸在一起加热,得到了氯气,就是我们现在实验室制备氯气的方法。某化学小组同学发现用这种方法制Cl2不易控制温度,他们现欲对该实验进行改进,进行了如下探究活动。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:2KMnO4+16HCl(浓)=___ +__ +5Cl2↑+8H2O。
(2)如图是实验室制备氯气并收集的装置(夹持设备已略)。
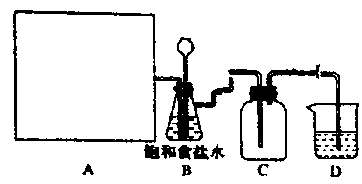
①该实验中A部分的装置是__ (填写装置的序号)。
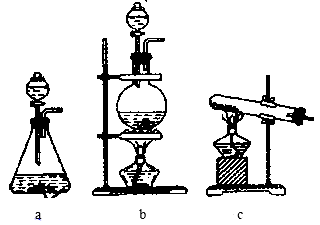
②装置B中的作用是__ 。
(3)①在制氯气前,必须进行的一项操作是__ 。
②D中装有NaOH溶液尾气吸收氯气,防止污染环境,同时我们也要防止液体倒吸对实验带来的安全隐患,选择合适装置来防止倒吸__ 。
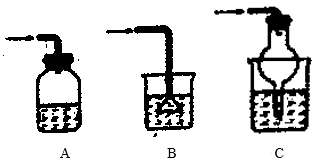
(4)实验室也可用氯酸钾与盐酸反应制备氯气,与出该反应的化学方程式,并用双线桥表示电子得失:___ ;当使用K37ClO3与H35Cl制备时,所得氯气的平均相对分子质量是__ 。
A.70 B.72 C.70.7 D.74
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:2KMnO4+16HCl(浓)=
(2)如图是实验室制备氯气并收集的装置(夹持设备已略)。

①该实验中A部分的装置是

②装置B中的作用是
(3)①在制氯气前,必须进行的一项操作是
②D中装有NaOH溶液尾气吸收氯气,防止污染环境,同时我们也要防止液体倒吸对实验带来的安全隐患,选择合适装置来防止倒吸

(4)实验室也可用氯酸钾与盐酸反应制备氯气,与出该反应的化学方程式,并用双线桥表示电子得失:
A.70 B.72 C.70.7 D.74
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
Ⅰ.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究 的性质,请补全实验现象b.
的性质,请补全实验现象b.___________ ,根据实验2现象写出该反应的离子方程式___________ 。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与 反应产生O2促进藻类快速生长。该反应说明氧化性:
反应产生O2促进藻类快速生长。该反应说明氧化性:
NaClO___________  (填“>”或“<”);当有1个
(填“>”或“<”);当有1个 生成时,转移电子的个数为
生成时,转移电子的个数为___________ 。
Ⅱ.亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
___________ ___________KI+___________=___________NO↑+___________I2+___________
___________KI+___________=___________NO↑+___________I2+___________ ___________
___________ ___________
___________
(3)请完成该化学方程式并配平。___________
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目___________ 。
Ⅰ.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究
 的性质,请补全实验现象b.
的性质,请补全实验现象b.| 序号 | 实验 | 实验现象 |
| 1 | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去; b.___________ |
| 2 | 向含5% 的酸性溶液中滴加淀粉碘化钾溶液 的酸性溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 反应产生O2促进藻类快速生长。该反应说明氧化性:
反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
 (填“>”或“<”);当有1个
(填“>”或“<”);当有1个 生成时,转移电子的个数为
生成时,转移电子的个数为Ⅱ.亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:___________
 ___________KI+___________=___________NO↑+___________I2+___________
___________KI+___________=___________NO↑+___________I2+___________ ___________
___________ ___________
___________
(3)请完成该化学方程式并配平。
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铁、钴在元素周期表中处于相邻位置,其单质及其化合物在工业生产中有重要用途:
(1)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
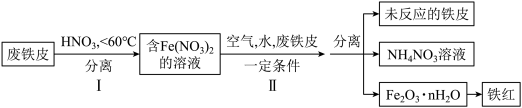
①步骤Ⅰ中的硝酸是三大强酸之一,其电离方程式为_______ ,曾出若温度过高,将导致硝酸分解,硝酸分解的化学方程式为_______ ;
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,硝酸的还原产物为硝酸铵,该反应的化学方程式为_______ ;
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
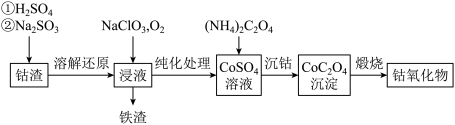
已知:Co(OH)3难溶于水,具有很强的氧化性。Co(OH)3溶解还原反应的离子方程式为_______ ,铁渣中铁元素的化合价为_______ ,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量2.41 g,CO2的体积为1.344 L(标准状况),则钴氧化物的化学式为_______ 。
(1)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ中的硝酸是三大强酸之一,其电离方程式为
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,硝酸的还原产物为硝酸铵,该反应的化学方程式为
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:

已知:Co(OH)3难溶于水,具有很强的氧化性。Co(OH)3溶解还原反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】已知海水中的溴含量约为 65 mg·L-1,从海水中提取溴的工业流程如下:
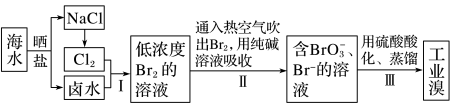
(1)步骤Ⅱ通入热空气吹出 Br2,利用了溴的_______ (填序号)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(2)步骤Ⅱ中涉及的离子反应如下,请在横线上填入正确的化学计量数:
___ Br2 +___  =
=___  +
+ ___ Br- +___ CO2↑
(3)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后 进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为________________________ 。
(4)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有________________ (填字母)。
A.乙醇 B.四氯化碳 C.醋酸 D.苯

(1)步骤Ⅱ通入热空气吹出 Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(2)步骤Ⅱ中涉及的离子反应如下,请在横线上填入正确的化学计量数:
 =
= +
+ (3)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后 进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为
(4)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有
A.乙醇 B.四氯化碳 C.醋酸 D.苯
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体系的简图,回答下列问题:

I.海水淡化:
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法可采用____ 操作。
II.海水制盐
(2)过程I采用的操作是溶解、___________ ;用到的玻璃仪器有___________ 。
(3)粗盐中可溶性的杂质离子有 、
、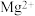 、
、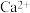 。要除去这些杂质离子得到精盐水,过程II依次加入了试剂顺序可选择
。要除去这些杂质离子得到精盐水,过程II依次加入了试剂顺序可选择___________ (填字母),其中 溶液的作用是
溶液的作用是___________ 。
a.NaOH溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸
b. 溶液、NaOH溶液、
溶液、NaOH溶液、 溶液、盐酸
溶液、盐酸
c.NaOH溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸
d. 溶液、
溶液、 溶液、NaOH溶液、盐酸
溶液、NaOH溶液、盐酸
(4)工业上从海水中提取溴单质的流程图中,步骤④中 作
作___________ 剂。
(5)工业上还可以利用海洋产品海带经过一系列反应制取单质 ,其中涉及到如下反应:
,其中涉及到如下反应: 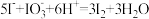 ,该反应中,氧化产物与还原产物之比为
,该反应中,氧化产物与还原产物之比为___________ 。

I.海水淡化:
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法可采用
II.海水制盐
(2)过程I采用的操作是溶解、
(3)粗盐中可溶性的杂质离子有
 、
、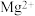 、
、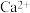 。要除去这些杂质离子得到精盐水,过程II依次加入了试剂顺序可选择
。要除去这些杂质离子得到精盐水,过程II依次加入了试剂顺序可选择 溶液的作用是
溶液的作用是a.NaOH溶液、
 溶液、
溶液、 溶液、盐酸
溶液、盐酸b.
 溶液、NaOH溶液、
溶液、NaOH溶液、 溶液、盐酸
溶液、盐酸c.NaOH溶液、
 溶液、
溶液、 溶液、盐酸
溶液、盐酸d.
 溶液、
溶液、 溶液、NaOH溶液、盐酸
溶液、NaOH溶液、盐酸(4)工业上从海水中提取溴单质的流程图中,步骤④中
 作
作(5)工业上还可以利用海洋产品海带经过一系列反应制取单质
 ,其中涉及到如下反应:
,其中涉及到如下反应: 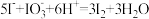 ,该反应中,氧化产物与还原产物之比为
,该反应中,氧化产物与还原产物之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】空气吹出法工艺,是目前“海水提溴”的最主要方法之。其工艺流程如下:

(1)步骤②发生主要反应的离子方程式是__________ 。
(2)步骤③通入热空气或水蒸气吹出Br2,利用了溴的__________ 性。
(3)写出步骤④中反应的离子方程式__________ 。
(4)步骤⑥中应控制温度在90℃以下,理由是__________ 。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。实验室中进行该操作用到的玻璃仪器主要有__________ 。
(6)根据上述反应可判断SO2、Cl-、Br-还原性由强到弱的顺序是:__________ 。

(1)步骤②发生主要反应的离子方程式是
(2)步骤③通入热空气或水蒸气吹出Br2,利用了溴的
(3)写出步骤④中反应的离子方程式
(4)步骤⑥中应控制温度在90℃以下,理由是
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。实验室中进行该操作用到的玻璃仪器主要有
(6)根据上述反应可判断SO2、Cl-、Br-还原性由强到弱的顺序是:
您最近一年使用:0次



