化学反应速率与生活、生产密切相关。
(1)为研究催化剂对H2O2分解反应速率的影响,某小组同学进行了如下实验:
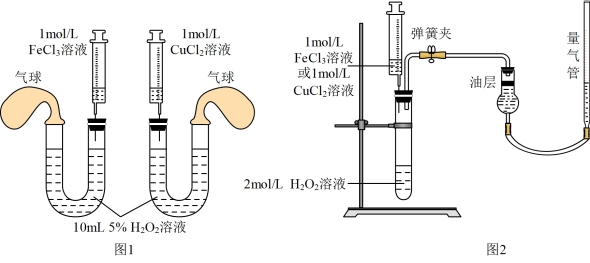
①定性研究:小组同学用图1装置进行实验,在注射器中分别加入相同体积的1mol/LFeCl3溶液和1mol/LCuCl2溶液,可通过观察___________ ,确定反应速率的大小。某同学提出用相同体积1mol/LCuSO4溶液代替1mol/LCuCl2溶液做实验,你认为是否合理及理由是___________ 。
②定量研究:为了更精确地研究催化剂对反应速率的影响,小组同学利用图2装置进行定量实验。向大试管中加入100mL2mol/L的H2O2溶液,向注射器中分别加入1mol/LCuCl2溶液和1mol/LFeCl3溶液,平行进行两次实验,测定的数据是___________ ,比较催化剂对反应速率的影响。若5min末得到标准状况下1.12L气体,忽略反应过程中溶液体积的变化,计算H2O2的分解反应速率为___________ 。
(2)一定条件下,在2L恒容容器中发生反应:2C(s)+2NO2(g) N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
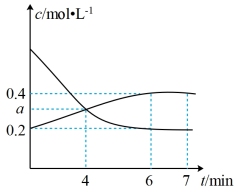
①在2min内,v(CO2)=___________ 。
②图3中,a=___________ (计算结果保留两位有效数字)。
③7min时,混合气体的平均相对分子质量为___________ (计算结果保留三位有效数字)。
(1)为研究催化剂对H2O2分解反应速率的影响,某小组同学进行了如下实验:

①定性研究:小组同学用图1装置进行实验,在注射器中分别加入相同体积的1mol/LFeCl3溶液和1mol/LCuCl2溶液,可通过观察
②定量研究:为了更精确地研究催化剂对反应速率的影响,小组同学利用图2装置进行定量实验。向大试管中加入100mL2mol/L的H2O2溶液,向注射器中分别加入1mol/LCuCl2溶液和1mol/LFeCl3溶液,平行进行两次实验,测定的数据是
(2)一定条件下,在2L恒容容器中发生反应:2C(s)+2NO2(g)
 N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
①在2min内,v(CO2)=
②图3中,a=
③7min时,混合气体的平均相对分子质量为
更新时间:2022-07-04 22:10:36
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为钠及其化合物的“价—类”二维图,请回答下列问题:

(1)②中Na、O的个数比为1:1,则其化学式是_______ ,其与水发生反应的化学方程式为_______ 。
(2)①与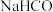 3溶液反应的离子方程式为
3溶液反应的离子方程式为_______ 。
(3)用 NaHSO4溶液鉴别 NaHCO3溶液和 Na2CO3;溶液的实验操作和现象为_______ 。
(4)NaH 中氢元素的化合价是_______ ,NaH 与水发生氧化还原反应,产物中既是氧化产物又是还原产物的是_______ (填化学式)。
(5)将2.3gNa投入97.8g水中充分反应,反应后溶液中溶质的质量分数是_______ 。

(1)②中Na、O的个数比为1:1,则其化学式是
(2)①与
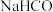 3溶液反应的离子方程式为
3溶液反应的离子方程式为(3)用 NaHSO4溶液鉴别 NaHCO3溶液和 Na2CO3;溶液的实验操作和现象为
(4)NaH 中氢元素的化合价是
(5)将2.3gNa投入97.8g水中充分反应,反应后溶液中溶质的质量分数是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】油画的白色颜料中曾含二价铅盐。二价铅盐经过长时间空气(含有微量H2S)的侵蚀,生成PbS而变黑,可用一定浓度的H2O2溶液擦洗修复。完成下列填空:
(1)H2O2与PbS反应生成PbSO4和H2O,写出该反应的化学方程式:___________ 。
(2)在PbSO4悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变澄清,有弱电解质生成,该弱电解质的化学式为___________ 。
(3)向200mL H2S溶液中缓慢通入SO2,发生反应2H2S+SO2=3S↓+2H2O,生成S的物质的量与通入SO2的物质的量关系如下图所示(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为___________ 。从开始通入SO2至饱和,再继续通一段时间,整个过程溶液中c(H+)的变化情况为___________ 。

(4)向含8.0g NaOH的溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物的质量为7.9g,则该无水物中一定含有的物质有___________ (填写化学式)。
(1)H2O2与PbS反应生成PbSO4和H2O,写出该反应的化学方程式:
(2)在PbSO4悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变澄清,有弱电解质生成,该弱电解质的化学式为
(3)向200mL H2S溶液中缓慢通入SO2,发生反应2H2S+SO2=3S↓+2H2O,生成S的物质的量与通入SO2的物质的量关系如下图所示(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为

(4)向含8.0g NaOH的溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物的质量为7.9g,则该无水物中一定含有的物质有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.700℃时,若向2L恒容的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g)⇌C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。___________ mol·L-1·min-1。
(2)图中A点v正___________ v逆(填“>”“<”或“=”)。
(3)第10min时,外界改变的条件可能是___________ (填字母)。
A.加催化剂 B.增大C的物质的量 C.减小 CO2的物质的量 D.升温 E.降温
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(1)该电池的正极反应式为___________ 。
(2)电池工作一段时间后电解质溶液的
___________ (填“增大”“减小”或“不变”)。

(2)图中A点v正
(3)第10min时,外界改变的条件可能是
A.加催化剂 B.增大C的物质的量 C.减小 CO2的物质的量 D.升温 E.降温
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(1)该电池的正极反应式为
(2)电池工作一段时间后电解质溶液的

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g)⇌2SO3(g)。
(1)向含有2molSO2的容器中通入过量氧气发生2SO2(g)+O2(g) 2SO3(g)ΔH=-QkJ·mol-1(Q>0),充分反应后生成SO3的物质的量
2SO3(g)ΔH=-QkJ·mol-1(Q>0),充分反应后生成SO3的物质的量___________ 2mol(填“<”“>”或“=”,下同),SO2的物质的量___________ 0mol,转化率___________ 100%,反应放出的热量___________ QkJ。
(2)降低温度,化学反应速率___________ (填“增大”“减小”或“不变”)。
(3)600℃时,在一容积为2L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10min和20min时,分别改变了影响反应速率的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,前10min正反应速率逐渐___________ (填“增大”“减小”或“不变”);前15min内用SO3表示平均反应速率为___________ 。
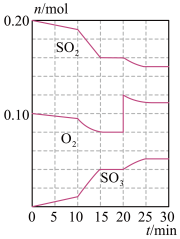
(4)图中反应进程,表示正反应速率与逆反应速率相等的时间段是___________ 。
(5)根据上图判断,10min时改变的反应条件可能是___________ (填编号,下同);20min时改变的反应条件可能是___________ 。
A.加入催化剂b.缩小容器容积c.降低温度d.增加O2的物质的量
(1)向含有2molSO2的容器中通入过量氧气发生2SO2(g)+O2(g)
 2SO3(g)ΔH=-QkJ·mol-1(Q>0),充分反应后生成SO3的物质的量
2SO3(g)ΔH=-QkJ·mol-1(Q>0),充分反应后生成SO3的物质的量(2)降低温度,化学反应速率
(3)600℃时,在一容积为2L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10min和20min时,分别改变了影响反应速率的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,前10min正反应速率逐渐

(4)图中反应进程,表示正反应速率与逆反应速率相等的时间段是
(5)根据上图判断,10min时改变的反应条件可能是
A.加入催化剂b.缩小容器容积c.降低温度d.增加O2的物质的量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在刚性密闭容器中充入一定量的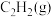 和
和 ,发生反应:
,发生反应: 。其他条件相同,在
。其他条件相同,在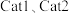 两种催化剂作用下,反应相同时间时
两种催化剂作用下,反应相同时间时 的转化率与温度的关系如图所示。
的转化率与温度的关系如图所示。

(1)催化效率较高的是_______ (填“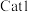 ”或“
”或“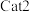 ”);b点
”);b点_______ (填“达到”或“未达到”)平衡。
(2)温度高于 ,升高温度,
,升高温度, 的原因可能是
的原因可能是_______ (答1条即可)。
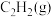 和
和 ,发生反应:
,发生反应: 。其他条件相同,在
。其他条件相同,在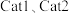 两种催化剂作用下,反应相同时间时
两种催化剂作用下,反应相同时间时 的转化率与温度的关系如图所示。
的转化率与温度的关系如图所示。
(1)催化效率较高的是
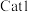 ”或“
”或“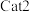 ”);b点
”);b点(2)温度高于
 ,升高温度,
,升高温度, 的原因可能是
的原因可能是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。碳中和是指CO2的排放总量和减少总量相当。
(1)科学家们经过探索实践,建立了如图所示的CO2新循环体系:

根据上图分析,下列相关说法错误的是
(2)在容积为2L的恒温密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
①下列说法正确的是_______ 。
a.反应达到平衡后,反应不再进行
b.使用催化剂是可以增大反应速率,提高生产效率
c.改变条件,CO2可以100%地转化为CH3OH
d.通过调控反应条件,可以提高该反应进行的程度
②a=_______ ;3~6min内,v(CO2)=_______ 。
③12min末时,混合气体中CH3OH的物质的量分数为_______ 。
④第3min时v正(CH3OH)_______ (填“>”、“<”或“=”)第9min时v逆(CH3OH)
(1)科学家们经过探索实践,建立了如图所示的CO2新循环体系:

根据上图分析,下列相关说法错误的是
| A.化学变化中质量和能量都是守恒的 |
| B.CO2和H2生成甲烷的反应中原子利用率为100% |
| C.将CO2还原为甲醇能有效促进“碳中和” |
| D.无机物和有机物可以相互转化 |
| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH)/mol | 0 | 0.50 | 0.65 | 0.75 | 0.75 |
| n(CO2)/mol | 1 | 0.50 | 0.35 | a | 0.25 |
①下列说法正确的是
a.反应达到平衡后,反应不再进行
b.使用催化剂是可以增大反应速率,提高生产效率
c.改变条件,CO2可以100%地转化为CH3OH
d.通过调控反应条件,可以提高该反应进行的程度
②a=
③12min末时,混合气体中CH3OH的物质的量分数为
④第3min时v正(CH3OH)
您最近一年使用:0次



