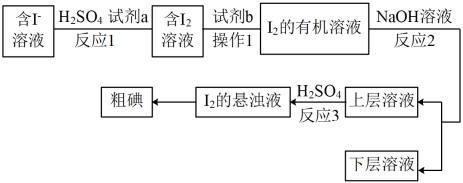
为完成下列实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器)
| 实验目的 | 玻璃仪器 | 试剂 | |
| A | 配制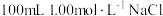 溶液 溶液 | 100mL容量瓶、胶头滴管、烧杯、量筒、玻璃棒 | NaCl固体、蒸馏水 |
| B | 从海带灰中获得含 的溶液 的溶液 | 烧杯、分液漏斗、玻璃棒 | 蒸馏水、海带灰 |
| C | 制备并收集氯气 | 圆底烧瓶、分液漏斗、导管、洗气瓶、集气瓶、烧杯 | 浓盐酸、二氧化锰、浓硫酸、饱和食盐水、氢氧化钠溶液 |
| D | 粗盐提纯 | 烧杯、量筒、玻璃棒、酒精灯、漏斗、胶头滴管 | 粗盐、蒸馏水、氯化钡溶液、氢氧化钠溶液、饱和碳酸钠溶液、稀盐酸 |
| A.A | B.B | C.C | D.D |
更新时间:2022-08-01 17:49:36
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:常温下可发生反应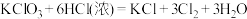 。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
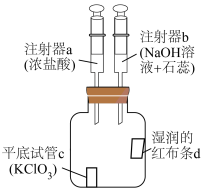
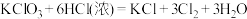 。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
A.c中产生 后,d褪色的原因是次氯酸具有漂白性 后,d褪色的原因是次氯酸具有漂白性 |
B.性质实验结束后,加入b中溶液除去多余的 溶液由蓝色变为紫色 溶液由蓝色变为紫色 |
| C.拉动a或b的活塞,可检查装置气密性 |
| D.c中反应的氧化剂与还原剂的物质的量比为1:6 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】设 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是A.在常温常压下,1.7 g  含有的原子数为 含有的原子数为 |
B.1 mol Na与足量 反应,生成 反应,生成 和 和 的混合物,钠失去 的混合物,钠失去 个电子 个电子 |
C.50 mL  盐酸与足量 盐酸与足量 共热,转移的电子数为 共热,转移的电子数为 |
D.20℃,101 kPa时,100 g由 和 和 组成的固体混合物中含有的金属阳离子数为 组成的固体混合物中含有的金属阳离子数为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】Cl2O 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。一种制取Cl2O 的装置如图所示。
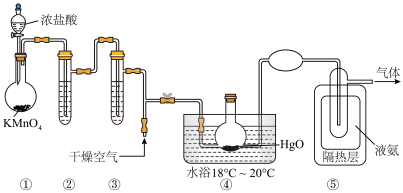
已知:Cl2O 的熔点为-116℃,沸点为 3.8℃;Cl2的沸点为-34.6℃;氨气的沸点:-33℃;HgO+2Cl2===HgCl2+Cl2O。
下列说法中不正确的是

已知:Cl2O 的熔点为-116℃,沸点为 3.8℃;Cl2的沸点为-34.6℃;氨气的沸点:-33℃;HgO+2Cl2===HgCl2+Cl2O。
下列说法中不正确的是
| A.Cl2O 与水的反应为氧化还原反应 |
| B.通入干燥空气的目的是将生成的Cl2O 稀释,减小爆炸危险 |
| C.从装置⑤中逸出气体的主要成分是 Cl2O |
| D.装置④与⑤之间不用橡胶管连接,是为了防止橡胶管燃烧和爆炸 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验中,不能达到实验目的的是
| 编号 | A | B | C | D |
| 实验方案 |  |  |  | 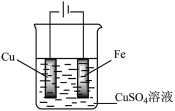 |
| 实验目的 | 证明混合溶液中有Fe2+ | 实验室制取乙烯的发生装置 | 稀释浓硫酸 | 在铁上镀铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是
| A.配制一定物质的量浓度的稀盐酸时,用量筒量取 9.82 mL 浓盐酸 |
| B.若配制 480 mL 1 mol/L NaOH 溶液,应称量 20.0 g NaOH 固体 |
| C.定容时,俯视刻度线会导致所得溶液浓度偏高 |
| D.定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】碘是人体不可缺少的微量元素,采用离子交换法从卤水(富含 )中提取碘的工艺流程如下。下列说法错误的是
)中提取碘的工艺流程如下。下列说法错误的是
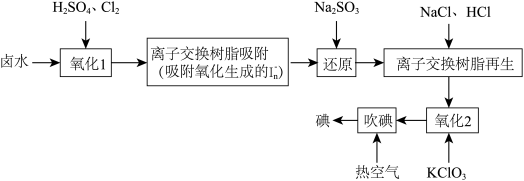
 )中提取碘的工艺流程如下。下列说法错误的是
)中提取碘的工艺流程如下。下列说法错误的是
A.“氧化1”的主要离子方程式为 |
| B.离子交换树脂的作用是富集碘元素 |
C.理论上参加反应的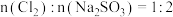 |
D.“吹碘”鼓入热空气是利用了 易升华的性质 易升华的性质 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】从海带中提取碘单质,成熟的工艺流程如下,下列说法不正确的是
干海带 海带灰
海带灰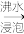 悬浊液
悬浊液 滤液
滤液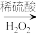 碘水
碘水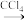
 的
的 溶液
溶液

干海带
 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液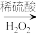 碘水
碘水
 的
的 溶液
溶液

| A.在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 |
B.向含 的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 |
| C.在碘水中加入几滴淀粉溶液,溶液变蓝色 |
D.向碘水中加入 得到I的 得到I的 溶液,该操作为“萃取” 溶液,该操作为“萃取” |
您最近一年使用:0次

 ,冷却,过滤,获得含I—的溶液,并设计如图所示实验方案从中提取I2。
,冷却,过滤,获得含I—的溶液,并设计如图所示实验方案从中提取I2。