某研究性学习小组制取氨气,并利用氨气和氧化铜反应来验证氨气分子中氮、氢原子的个数比,按如图所示装置进行实验。已知:氨气与灼热的氧化铜反应,生成铜、水和氮气。
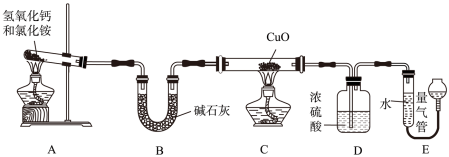
(1)装置A 中发生反应的化学方程式为_______ 。
(2)实验中,先断开C与D,加热装置_______ (填“A”或“C”)片刻,再连接C与D,加热另一个装置,其目的是_______ 。
(3)装置C 的玻璃管中发生反应的化学方程式为_______ ,若固体的质量减少3.2g,则该反应中转移电子的物质的量为_______ 。
(4)称量反应前后,玻璃管(含固体物质)的质量分别为m1g、m2g;生成的氮气在标准状况下的体积为VL。用所测数据计算出氨气分子中氮、氢原子个数之比为_______ 。
(5)小组同学还测定了反应前后装置D(含药品)的质量和生成的氮气体积(在标准状况下)。由此数据计算出的氨气分子中氮、氢原子个数比小于理论值,其原因是_______ 。

(1)装置A 中发生反应的化学方程式为
(2)实验中,先断开C与D,加热装置
(3)装置C 的玻璃管中发生反应的化学方程式为
(4)称量反应前后,玻璃管(含固体物质)的质量分别为m1g、m2g;生成的氮气在标准状况下的体积为VL。用所测数据计算出氨气分子中氮、氢原子个数之比为
(5)小组同学还测定了反应前后装置D(含药品)的质量和生成的氮气体积(在标准状况下)。由此数据计算出的氨气分子中氮、氢原子个数比小于理论值,其原因是
更新时间:2022-07-12 15:16:54
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
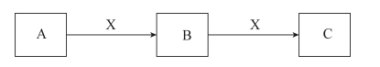
【推荐1】A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色,有关的转化关系如图所示(反应条件与部分反应的生成物略去)。

请回答下列问题:
(1)D的化学式为_____ ,检验Y的方法:____ 。F和Z生成E和G的化学方程式为_____ 。
(2)Y与氧化铜反应,每生成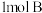 消耗
消耗 氧化铜,该反应的化学方程式为
氧化铜,该反应的化学方程式为_____ 。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为_______ 。
(4)气体F和气体 在通常条件下同时通入盛有
在通常条件下同时通入盛有 溶液的洗气瓶中(如图所示),洗气瓶中产生沉淀的理由是
溶液的洗气瓶中(如图所示),洗气瓶中产生沉淀的理由是_____ 。


请回答下列问题:
(1)D的化学式为
(2)Y与氧化铜反应,每生成
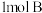 消耗
消耗 氧化铜,该反应的化学方程式为
氧化铜,该反应的化学方程式为(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)气体F和气体
 在通常条件下同时通入盛有
在通常条件下同时通入盛有 溶液的洗气瓶中(如图所示),洗气瓶中产生沉淀的理由是
溶液的洗气瓶中(如图所示),洗气瓶中产生沉淀的理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如图的反应关系:
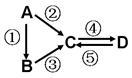
(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。写出其中D与水反应生成的酸名称_______ 。
(2)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式_______ 。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式_______ 。
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式_______ 。
(5)若A是应用最广泛的金属。④反应用到A,①⑤反应均用到同一种非金属单质。写出④反应的离子方程式_______ 。

(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。写出其中D与水反应生成的酸名称
(2)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式
(5)若A是应用最广泛的金属。④反应用到A,①⑤反应均用到同一种非金属单质。写出④反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氮化铝( )是一种性能优异的新型材料,在许多领域有广泛应用。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。查阅资料:
)是一种性能优异的新型材料,在许多领域有广泛应用。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。查阅资料:
①实验室用饱和 溶液与
溶液与 溶液共热制
溶液共热制 :
:
②工业制氮化铝: ,氮化铝在高温下能水解。
,氮化铝在高温下能水解。
③ 与
与 饱和溶液反应:
饱和溶液反应: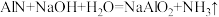
Ⅰ、氮化铝的制备
(1)实验中使用的装置如图所示,请按照氮气气流方向将各仪器接口连接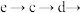
_______  。
。
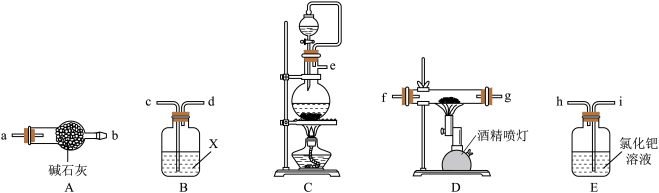
(2)B装置内的X液体可能是_______ ;E装置内氯化钯溶液的作用可能是_______
Ⅱ、氮化铝纯度的测定
(方案Ⅰ)甲同学用下图装置测定 的纯度(部分夹持装置已略去)。
的纯度(部分夹持装置已略去)。
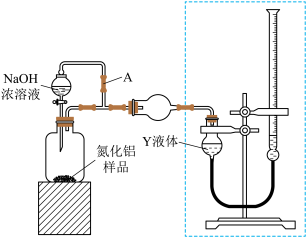
(3)为了准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是_______ 。
a.CCl4 b.H2O
c.NH4Cl饱和溶液 d.植物油
(方案Ⅱ)乙同学按以下步骤测定样品中 的纯度(流程如下图)
的纯度(流程如下图)

(4)步骤②的操作是通入过量_______ 气体。
 )是一种性能优异的新型材料,在许多领域有广泛应用。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。查阅资料:
)是一种性能优异的新型材料,在许多领域有广泛应用。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。查阅资料:①实验室用饱和
 溶液与
溶液与 溶液共热制
溶液共热制 :
:
②工业制氮化铝:
 ,氮化铝在高温下能水解。
,氮化铝在高温下能水解。③
 与
与 饱和溶液反应:
饱和溶液反应: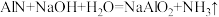
Ⅰ、氮化铝的制备
(1)实验中使用的装置如图所示,请按照氮气气流方向将各仪器接口连接
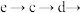
 。
。
(2)B装置内的X液体可能是
Ⅱ、氮化铝纯度的测定
(方案Ⅰ)甲同学用下图装置测定
 的纯度(部分夹持装置已略去)。
的纯度(部分夹持装置已略去)。
(3)为了准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是
a.CCl4 b.H2O
c.NH4Cl饱和溶液 d.植物油
(方案Ⅱ)乙同学按以下步骤测定样品中
 的纯度(流程如下图)
的纯度(流程如下图)
(4)步骤②的操作是通入过量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】六水氯化锶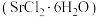 是实验室重要的分析试剂。工业上常以天青石(主要成分为
是实验室重要的分析试剂。工业上常以天青石(主要成分为 ,含少量
,含少量 )为原料制备,生产流程如图:
)为原料制备,生产流程如图:

已知:①25℃时, 的
的 为
为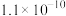 ,
, 的
的 为
为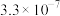 。
。
② (摩尔质量为
(摩尔质量为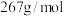 ),易溶于水,微溶于无水乙醇和丙酮。
),易溶于水,微溶于无水乙醇和丙酮。
(1)关于上述实验操作下列说法不正确的是_______。
(2)步骤I的化学方程式为_______ 。
(3)经盐酸浸取后的溶液中除含有 和
和 外,还有少量的
外,还有少量的 杂质。为了除去杂质
杂质。为了除去杂质 ,同时提高原料的利用率,滤液中
,同时提高原料的利用率,滤液中 的浓度应不高于
的浓度应不高于_______  。
。
(注:通常认为残留在溶液中的离子浓度小于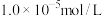 时,离子完全沉淀)
时,离子完全沉淀)
(4)产品纯度检测:称取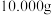 产品配成
产品配成 溶液,移取
溶液,移取 溶液于锥形瓶中,向其中加入含溶质为
溶液于锥形瓶中,向其中加入含溶质为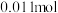 的
的 溶液。溶液中除
溶液。溶液中除 外,不含其它与
外,不含其它与 反应的离子,待
反应的离子,待 完全沉淀后,滴入1~2滴含
完全沉淀后,滴入1~2滴含 的溶液作指示剂,用
的溶液作指示剂,用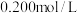 的NH4SCN标准溶液滴定剩余的
的NH4SCN标准溶液滴定剩余的 ,使剩余的
,使剩余的 以
以 白色沉淀的形式析出。
白色沉淀的形式析出。
①配制 样品溶液需要用到下列所有操作:
样品溶液需要用到下列所有操作:
a.打开容量瓶玻璃塞,加入适量水,塞紧塞子,倒立;
b.冷却至室温;
c.将溶液转移到容量瓶中;
d.轻轻振荡容量瓶;
e.将塞子反转180度,倒立;
f.称取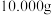 试样置于烧杯中,加入适量水充分溶解;
试样置于烧杯中,加入适量水充分溶解;
g.洗涤烧杯内壁和玻璃棒2~3次;
h.定容,摇匀。
请给出上述操作的正确顺序:_______ (操作可重复使用)。
a→e→f→______→______→______→______→______→h
②下列有关上述滴定操作的说法正确的是_______ 。
A.滴定管活塞涂凡士林:用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如下图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
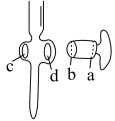
B.滴定开始时可将液体成线状快速流下,接近终点时减慢滴加速度,眼睛注视滴定管中液面变化
C.当加入最后半滴NH4SCN溶液时,溶液颜色从红色刚好变为无色,且半分钟内不变色
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.第一次滴定终点时,若测得消耗标准液体积小于 ,则第二次滴定时可稀释待测液后重新滴定来减小误差
,则第二次滴定时可稀释待测液后重新滴定来减小误差
③达到终点时,消耗NH4SCN溶液如下表:
则产品中 的质量百分含量为
的质量百分含量为_______ 。
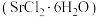 是实验室重要的分析试剂。工业上常以天青石(主要成分为
是实验室重要的分析试剂。工业上常以天青石(主要成分为 ,含少量
,含少量 )为原料制备,生产流程如图:
)为原料制备,生产流程如图:
已知:①25℃时,
 的
的 为
为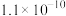 ,
, 的
的 为
为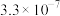 。
。②
 (摩尔质量为
(摩尔质量为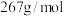 ),易溶于水,微溶于无水乙醇和丙酮。
),易溶于水,微溶于无水乙醇和丙酮。(1)关于上述实验操作下列说法不正确的是_______。
| A.工业上天青石焙烧前应先研磨粉碎,是为了提高化学反应速率 |
| B.步骤III,若要从滤液中得到大颗粒的高纯六水氯化锶晶体,需将滤液蒸发浓缩并快速降温结晶 |
C.过滤后为除去 晶体表面的杂质,应向过滤器中加冷水浸没,洗涤晶体2~3次 晶体表面的杂质,应向过滤器中加冷水浸没,洗涤晶体2~3次 |
D.为得到无水 ,可直接加热 ,可直接加热 脱去结晶水获得 脱去结晶水获得 |
(3)经盐酸浸取后的溶液中除含有
 和
和 外,还有少量的
外,还有少量的 杂质。为了除去杂质
杂质。为了除去杂质 ,同时提高原料的利用率,滤液中
,同时提高原料的利用率,滤液中 的浓度应不高于
的浓度应不高于 。
。(注:通常认为残留在溶液中的离子浓度小于
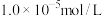 时,离子完全沉淀)
时,离子完全沉淀)(4)产品纯度检测:称取
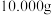 产品配成
产品配成 溶液,移取
溶液,移取 溶液于锥形瓶中,向其中加入含溶质为
溶液于锥形瓶中,向其中加入含溶质为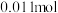 的
的 溶液。溶液中除
溶液。溶液中除 外,不含其它与
外,不含其它与 反应的离子,待
反应的离子,待 完全沉淀后,滴入1~2滴含
完全沉淀后,滴入1~2滴含 的溶液作指示剂,用
的溶液作指示剂,用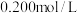 的NH4SCN标准溶液滴定剩余的
的NH4SCN标准溶液滴定剩余的 ,使剩余的
,使剩余的 以
以 白色沉淀的形式析出。
白色沉淀的形式析出。①配制
 样品溶液需要用到下列所有操作:
样品溶液需要用到下列所有操作:a.打开容量瓶玻璃塞,加入适量水,塞紧塞子,倒立;
b.冷却至室温;
c.将溶液转移到容量瓶中;
d.轻轻振荡容量瓶;
e.将塞子反转180度,倒立;
f.称取
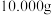 试样置于烧杯中,加入适量水充分溶解;
试样置于烧杯中,加入适量水充分溶解;g.洗涤烧杯内壁和玻璃棒2~3次;
h.定容,摇匀。
请给出上述操作的正确顺序:
a→e→f→______→______→______→______→______→h
②下列有关上述滴定操作的说法正确的是
A.滴定管活塞涂凡士林:用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如下图)处的四周,平行插入活塞槽中,然后朝同一个方向转动

B.滴定开始时可将液体成线状快速流下,接近终点时减慢滴加速度,眼睛注视滴定管中液面变化
C.当加入最后半滴NH4SCN溶液时,溶液颜色从红色刚好变为无色,且半分钟内不变色
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.第一次滴定终点时,若测得消耗标准液体积小于
 ,则第二次滴定时可稀释待测液后重新滴定来减小误差
,则第二次滴定时可稀释待测液后重新滴定来减小误差③达到终点时,消耗NH4SCN溶液如下表:
| 实验 | 消耗NH4SCN溶液体积 |
| 第一次 | 19.98 |
| 第二次 | 18.73 |
| 第三次 | 20.02 |
 的质量百分含量为
的质量百分含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组为确定一种从煤中提取的液态烃X的组成,对其进行探究。
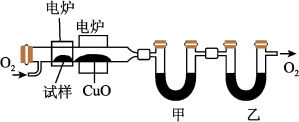
实验步骤如下:
 按上述装置图连接好各仪器,检验装置的气密性。
按上述装置图连接好各仪器,检验装置的气密性。
 向装置中通入氧气,一段时间后,启动电炉达到一定温度,有机物X经气化后缓慢通过灼热的氧化铜,与氧气充分反应。
向装置中通入氧气,一段时间后,启动电炉达到一定温度,有机物X经气化后缓慢通过灼热的氧化铜,与氧气充分反应。
 生成的气体依次通过甲、乙两个U形管被完全吸收。
生成的气体依次通过甲、乙两个U形管被完全吸收。
 关闭电炉,一段时间后停止通入氧气。测得甲、乙两个U形管增重分别为
关闭电炉,一段时间后停止通入氧气。测得甲、乙两个U形管增重分别为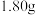 和
和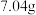 。
。
 通过仪器分析测得X的相对分子质量为106。
通过仪器分析测得X的相对分子质量为106。
回答下列问题:
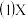 的分子式为
的分子式为______ 。
 甲中的试剂为
甲中的试剂为 写化学式
写化学式
______ ,某同学认为该套装置不合理,其理由是______ 。
 写出符合下列条件的所有X的结构简式
写出符合下列条件的所有X的结构简式______ 。
 芳香烃
芳香烃  苯环上的一氯代物有三种
苯环上的一氯代物有三种
 以醋酸为溶剂在催化剂作用下用氧气氧化X的某一同分异构体得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:
以醋酸为溶剂在催化剂作用下用氧气氧化X的某一同分异构体得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度: 时
时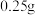 、
、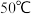 时
时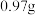 、
、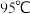 时
时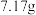 。得到的粗产品中有部分不溶性杂质,提纯PTA粗品的实验步骤为:将PTA粗品溶于适量热水、
。得到的粗产品中有部分不溶性杂质,提纯PTA粗品的实验步骤为:将PTA粗品溶于适量热水、______ 、______ 、过滤、洗涤、干燥。

实验步骤如下:
 按上述装置图连接好各仪器,检验装置的气密性。
按上述装置图连接好各仪器,检验装置的气密性。 向装置中通入氧气,一段时间后,启动电炉达到一定温度,有机物X经气化后缓慢通过灼热的氧化铜,与氧气充分反应。
向装置中通入氧气,一段时间后,启动电炉达到一定温度,有机物X经气化后缓慢通过灼热的氧化铜,与氧气充分反应。 生成的气体依次通过甲、乙两个U形管被完全吸收。
生成的气体依次通过甲、乙两个U形管被完全吸收。 关闭电炉,一段时间后停止通入氧气。测得甲、乙两个U形管增重分别为
关闭电炉,一段时间后停止通入氧气。测得甲、乙两个U形管增重分别为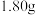 和
和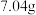 。
。 通过仪器分析测得X的相对分子质量为106。
通过仪器分析测得X的相对分子质量为106。回答下列问题:
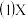 的分子式为
的分子式为 甲中的试剂为
甲中的试剂为 写化学式
写化学式
 写出符合下列条件的所有X的结构简式
写出符合下列条件的所有X的结构简式 芳香烃
芳香烃  苯环上的一氯代物有三种
苯环上的一氯代物有三种 以醋酸为溶剂在催化剂作用下用氧气氧化X的某一同分异构体得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:
以醋酸为溶剂在催化剂作用下用氧气氧化X的某一同分异构体得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度: 时
时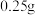 、
、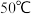 时
时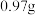 、
、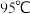 时
时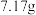 。得到的粗产品中有部分不溶性杂质,提纯PTA粗品的实验步骤为:将PTA粗品溶于适量热水、
。得到的粗产品中有部分不溶性杂质,提纯PTA粗品的实验步骤为:将PTA粗品溶于适量热水、
您最近一年使用:0次