部分物质的燃烧热如下表,下列关于CH4和水蒸气反应得到H2和CO的热化学方程式正确的是
已知1mol H2O(g)转化生成1mol H2O(l)时放出热量44.0 kJ。
| 物质 | H2(g) | CO(g) | CH4(g) |
| △H/(kJ·mol−1) | −285.8 | −283.0 | −890.3 |
| A.CH4(g)+ H2O(g)=CO(g)+ 3H2(g) △H1=+206.1 kJ·mol−1 |
| B.CH4(g)+ H2O(g)=CO(g)+ 3H2(g) △H2=−206.1 kJ·mol−1 |
| C.CH4(g)+ H2O(g)=CO(g)+ 3H2(g) △H3=+365.5 kJ·mol−1 |
| D.CH4(g)+ H2O(g)=CO(g)+ 3H2(g) △H4=−365.5 kJ·mol−1 |
2021高三·全国·专题练习 查看更多[6]
(已下线)第15讲 化学反应的热效应(练) — 2022年高考化学一轮复习讲练测(新教材新高考)黑龙江省鹤岗市第一中学2021-2022学年高二上学期开学考试化学试题(已下线)专题18 化学反应与能量(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练湖南省长沙市雅礼中学2021-2022学年高一下学期期末考试化学试题(已下线)第04讲 第一章《化学反应的热效应》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第1讲 化学能与热能
更新时间:2022-07-12 17:22:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列化学用语正确的是
A.电解液为稀硫酸的甲醇燃料电池中,负极的电极反应式为: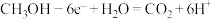 |
B.铅蓄电池充时阳极电极反应式为: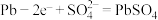 |
C.用惰性电极电解熔融氯化钠: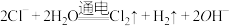 |
D. 燃烧热的热化学方程式为: 燃烧热的热化学方程式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:(1)H2O(g)=H2O(l) △H1=-Q1kJ/mol
(2)CH3OH(g)=CH3OH(l) △H2=-Q2kJ/mol
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=-Q3kJ/mol
Q1、Q2、Q3均大于0.若要使32g液态甲醇完全燃烧并恢复到室温,放出的热量为( )
(2)CH3OH(g)=CH3OH(l) △H2=-Q2kJ/mol
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=-Q3kJ/mol
Q1、Q2、Q3均大于0.若要使32g液态甲醇完全燃烧并恢复到室温,放出的热量为( )
| A.Q1+Q2+Q3 | B.5Q3+Q2-2Q1 |
| C.0.5Q3-Q2+2Q1 | D.0.5(Q1+Q2+Q3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】2CO(g)+4H2(g)═2CH4(g)+O2(g) △H=+71kJ⋅mol−1,CO(g)+2H2(g)═CH3OH(l)△H=−90.5kJ⋅mol−1已知CH4(g)的燃烧热为−890kJ⋅mol−1,则CH3OH(l)的燃烧热为( )
| A.−1528kJ⋅mol−1 | B.−764kJ⋅mol−1 | C.−382kJ⋅mol−1 | D.无法计算 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以CO和 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就是将
人工合成淀粉时,第一步就是将 转化为甲醇。
转化为甲醇。
已知:①
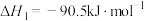
②
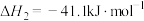
③
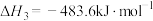
下列说法正确的是
 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就是将
人工合成淀粉时,第一步就是将 转化为甲醇。
转化为甲醇。已知:①

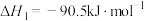
②

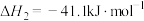
③

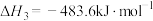
下列说法正确的是
A.若温度不变,反应①中生成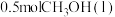 时,放出的热量小于45.25kJ 时,放出的热量小于45.25kJ |
| B.对于反应②③,选用高效催化剂,可分别降低反应的焓变 |
C. 与 与 合成甲醇的热化学方程式为 合成甲醇的热化学方程式为 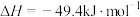 |
D.以 和 和 为原料合成甲醇,同时生成 为原料合成甲醇,同时生成 ,该反应放出能量 ,该反应放出能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】化学反应放出或吸收的能量称为反应热。反应热(ΔH)又因化学反应的分类给予不同的名称。如我们学过的燃烧热(ΔHc),又如由稳定单质化合生成1 mol纯物质的热效应称为生成热(ΔHf),断裂化学键时,所吸收的能量称为键能(ΔHb)。下面两个图中的数据分别表示水与二氧化碳各1 mol 分解时能量变化的示意图,图中的各数据均以kJ为单位,下列说法正确的是
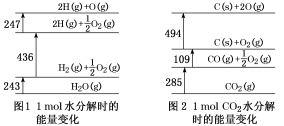

| A.H2O(g)的生成热:ΔHf=243 kJ·mol-1 |
| B.CO(g)的燃烧热:ΔHc=-570 kJ·mol-1 |
| C.O—H键的键能:ΔHb=436 kJ·mol-1 |
| D.CO(g)+H2O(g)=CO2(g)+H2(g) |
您最近一年使用:0次

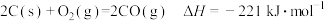 ;
;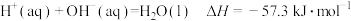 。
。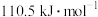
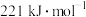
 时,放出
时,放出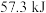 热量
热量

