化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图所示为 和
和 反应生成
反应生成 过程中的能量变化,下列说法正确的是
过程中的能量变化,下列说法正确的是

 和
和 反应生成
反应生成 过程中的能量变化,下列说法正确的是
过程中的能量变化,下列说法正确的是
A.1mol 和1mol 和1mol 反应吸收的能量为180kJ 反应吸收的能量为180kJ |
B.1mol 和1mol 和1mol 具有的总能量大于2mol 具有的总能量大于2mol 具有的总能量 具有的总能量 |
C.在1L的密闭容器中发生此反应,10min内 减少了1mol,因此10min内的平均反应速率为 减少了1mol,因此10min内的平均反应速率为 |
D.NO是一种酸性氧化物,且能与 直接反应生成 直接反应生成 |
更新时间:2022-07-15 16:27:40
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知2—丁烯的两种同分异构体可以相互转化:
 (g)
(g)
 (g)+4.6kJ
(g)+4.6kJ
下列关于2—丁烯的两种异构体的说法正确的是
 (g)
(g)
 (g)+4.6kJ
(g)+4.6kJ下列关于2—丁烯的两种异构体的说法正确的是
| A.两者的沸点相同 | B.低温有利于反式转化为顺式 |
| C.反式更稳定 | D.分别与等物质的量H2反应,反式放热多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列反应中属于吸热反应的是
| A.盐酸与氢氧化钠溶液的反应 | B.金属镁和盐酸的反应 |
| C.石灰石在高温下分解的反应 | D.乙醇在空气中燃烧的反应 |
您最近一年使用:0次
【推荐3】中国提出二氧化碳排放在2030年前达到峰值,2060年前实现碳中和。这体现了中国作为全球负责任大国的环境承诺和行动决心。二氧化碳选择性加氢制甲醇是解决温室效应、发展绿色能源和实现经济可持续发展的重要途径之一、常温常压下利用铜基催化剂实现二氧化碳选择性加氢制甲醇的反应机理和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注),下列说法错误的是
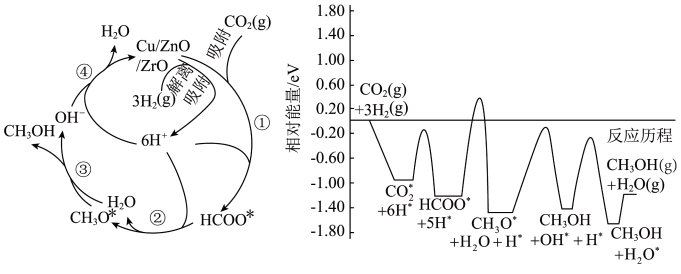
| A.二氧化碳选择性加氢制甲醇是放热反应 |
| B.催化剂能改变反应机理,加快反应速率,降低反应热 |
| C.总反应为CO2(g)+3H2(g)=CH3OH(g)+H2O(g) |
| D.该历程的决速步为HCOO*+4H*=CH3O*+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:2H2(g)+O2(g)=2H2O(g) ΔH=-akJ·mol-1

已知a、b、c均大于零,下列说法正确的是

已知a、b、c均大于零,下列说法正确的是
| A.1mol H2与O2反应生成水的反应热为a kJ |
| B.氢分子变为氢原子需要放出b kJ·mol-1的热量 |
| C.断开1mol H-O键需要的能量为(a+b+c)/4kJ |
| D.可通过a、b、c的具体数值判断H-H键与H-O键的相对牢固程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】理论研究表明,在101kPa和298K下,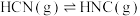 异构化反应过程的能量变化如图所示。下列说法正确的是
异构化反应过程的能量变化如图所示。下列说法正确的是
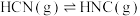 异构化反应过程的能量变化如图所示。下列说法正确的是
异构化反应过程的能量变化如图所示。下列说法正确的是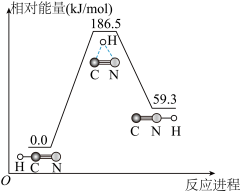
| A.HNC比HCN稳定 |
| B.反应物的总键能小于生成物的总键能 |
| C.该异构化反应只有在加热条件下才能进行 |
| D.1molHCN(s)转化为1molHNC(g)所吸收的能量要大于59.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】1.下列关于热化学反应的描述中正确的是
Ⅱ: 且a、b、c均大于零,则断开1摩尔H-Cl键所需的能量为(-a-b-c) kJ/mol
且a、b、c均大于零,则断开1摩尔H-Cl键所需的能量为(-a-b-c) kJ/mol
Ⅱ:
 且a、b、c均大于零,则断开1摩尔H-Cl键所需的能量为(-a-b-c) kJ/mol
且a、b、c均大于零,则断开1摩尔H-Cl键所需的能量为(-a-b-c) kJ/mol| A.氯化氢与氢氧化钠反应的中和热△H=-57.3kJ/mol,则硫酸和氢氧化钡反应的△H =-2×(-57.3) kJ/mol |
| B.CO(g)的燃烧热是283.0KJ/mol,则表示一氧化碳的燃烧热的热化学方程式为CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D.已知:Ⅰ:对于反应:H2(g)+Cl2(g)=2HCl(g)△H=-a kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下在2L的恒容密闭容器中,充入0.3 molA、0.1 molB和一定量C三种气体, 一定条件下发生反应,各物质的浓度随时间变化曲线如图所示。已知反应过程中混合气体的平均摩尔质量不变。下列说法错误的是
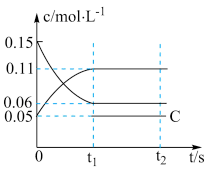
| A.起始C的物质的量是0.04 mol |
| B.该反应的化学方程式为3A( g)+C(g)═2B( g) |
| C.达到化学平衡时,混合气体中B的体积分数为50% |
| D.若t₁ = 1 5,0 ~ t₁ s内,A 的平均反应速率v(A)=0.006 mol/(L·s) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,下列说法正确的是
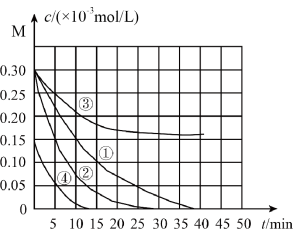
| 实验编号 | 温度/℃ | pH |
| ① | 25 | 1 |
| ② | 45 | 1 |
| ③ | 25 | 7 |
| ④ | 25 | 1 |

| A.实验①在15 min内M的降解速率为1.33×10-2 mol/(L·min) |
| B.若其他条件相同,实验①②说明降低温度,M降解速率增大 |
| C.若其他条件相同,实验①③证明pH越大,越不利于M的降解 |
| D.若其他条件相同,实验①④说明M的浓度越小,降解的速率越快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】Fenton法常用于处理含难降解有机物的工业废水,向调节好pH和 浓度的废水中加入
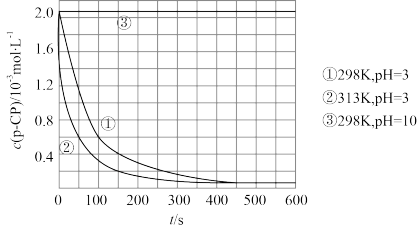
浓度的废水中加入 ,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,控制pCP的初始浓度相同,恒定实验温度在298K或313K进行实验。实验测得pCP的浓度随时间变化的关系如图所示,下列说法
,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,控制pCP的初始浓度相同,恒定实验温度在298K或313K进行实验。实验测得pCP的浓度随时间变化的关系如图所示,下列说法不正确 的是
 浓度的废水中加入
浓度的废水中加入 ,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,控制pCP的初始浓度相同,恒定实验温度在298K或313K进行实验。实验测得pCP的浓度随时间变化的关系如图所示,下列说法
,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,控制pCP的初始浓度相同,恒定实验温度在298K或313K进行实验。实验测得pCP的浓度随时间变化的关系如图所示,下列说法
A.由曲线①可得,降解反应在50~150s内的平均反应速率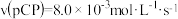 |
| B.实验③的目的为探究溶液的pH对降解反应速率的影响 |
| C.298K下,有机物pCP的降解速率在pH=10时比pH=3时慢 |
| D.升高温度,有利于加快降解反应速率,但温度过高反应速率又会变慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知v(A)、v(B)、v(C)之间有以下关系:2v(B)=3v(A),2v(B)=3v(C),则此反应可表示为
| A.2A+3B=2C | B.A+2B=C | C.3A+2B=2C | D.2A+2B=3C |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下,可逆反应X(g)+3Y(g) 2Z(g)△H <0,若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.2mol /L,0.6mol/ L,0.1 mol/L,则下列判断不合理的是
2Z(g)△H <0,若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.2mol /L,0.6mol/ L,0.1 mol/L,则下列判断不合理的是
 2Z(g)△H <0,若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.2mol /L,0.6mol/ L,0.1 mol/L,则下列判断不合理的是
2Z(g)△H <0,若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.2mol /L,0.6mol/ L,0.1 mol/L,则下列判断不合理的是| A.起始时c1:c2=1:3且 平衡时X、Y的转化率相等 |
| B.c1的取值范围为0< c1<0.25mo /L |
| C.反应开始后,Y和Z的生成速率之比为2:3 |
| D.对平衡体系加热,则混和气体的平均分子量减小 |
您最近一年使用:0次

 xC(g)+2D(g)。2min末测得此时容器中C和D的浓度为0.2mol/L和0.4mol/L。下列叙述正确的是
xC(g)+2D(g)。2min末测得此时容器中C和D的浓度为0.2mol/L和0.4mol/L。下列叙述正确的是

