研究人员发现,在一定的实验条件下,给水施加一个弱电场,在20℃、1个大气压下,水可以结成冰,称为“热冰”。
(1) 中半径较大的是
中半径较大的是_______ 原子,其原子结构示意图为_______ ;水分子中氢、氧原子间的化学键是_______ (填“共价键”或“离子键”)。
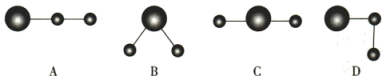
(2)用球棍模型表示的水分子结构正确的是_______ (填字母)。
(1)
 中半径较大的是
中半径较大的是(2)用球棍模型表示的水分子结构正确的是

更新时间:2022-08-22 11:14:48
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表为元素周期表的一部分,针对表中①~⑧元素,回答下列问题:_____ ,M层有___ 个电子。写出③的原子结构示意图_____ 。
(2)元素②在周期表中的位置是_____ ,③元素在周期表中的位置是第2周期_____ 族。
(3)写出②的最高价氧化物_______ ,写出⑥的最高价氧化物_____ 。
(4)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是______ (填化学式)。
(5)⑤的单质在③中燃烧,产物是______ 。

(2)元素②在周期表中的位置是
(3)写出②的最高价氧化物
(4)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是
(5)⑤的单质在③中燃烧,产物是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】用A+、B-、C2-、D、E、F分别表示含有10个电子的七种微粒(离子或分子),回答下列问题:
(提示:多核即由多个原子组合形成的微粒)
(1)如果A+、B-、C2-是单核离子,则A+是_______ 、C2-是_______ (用元素符号表示)。
(2)如果A是多核常见离子,请写出A+离子的电子式_______ 。
(3)已知D、E、F、G均是含有10个电子的分子。
①D是由两种元素组成的双原子分子,用电子式表示其形成过程是_______ ;
②E是所有10个电子微粒中最稳定的单原子分子,化学性质极不活泼,请写出该原子的结构示意图为_______ ;
③F是由两种元素组成的四原子分子,其结构式为_______ ;其分子的空间构型是_______ 。
(提示:多核即由多个原子组合形成的微粒)
(1)如果A+、B-、C2-是单核离子,则A+是
(2)如果A是多核常见离子,请写出A+离子的电子式
(3)已知D、E、F、G均是含有10个电子的分子。
①D是由两种元素组成的双原子分子,用电子式表示其形成过程是
②E是所有10个电子微粒中最稳定的单原子分子,化学性质极不活泼,请写出该原子的结构示意图为
③F是由两种元素组成的四原子分子,其结构式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同,A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)A元素单质的化学式为____ ,D元素的离子结构示意图为____ 。
(2)写出D、E最高价氧化物对应水化物的化学式____ 、____ (用化学式表示)。
(3)由E元素形成的单质的结构式可表示为____ 。
(4)由A、B、C三种元素形成的化合物的电子式为____ ,这种化合物中所含的化学键类型有____ 。
(5)H2D、HE的稳定性由强到弱的顺序为____ (用化学式表示)。
(1)A元素单质的化学式为
(2)写出D、E最高价氧化物对应水化物的化学式
(3)由E元素形成的单质的结构式可表示为
(4)由A、B、C三种元素形成的化合物的电子式为
(5)H2D、HE的稳定性由强到弱的顺序为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】已知乙烯能发生如图转化关系:
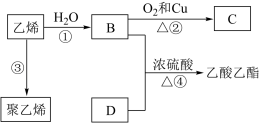
(1)A为乙烯的同系物,相对分子质量比乙烯大14,根据乙烯的性质推测A的性质,下列说法错误 的是_______。
(2)D的结构简式为:_______ 。
(3)写出反应①的反应类型:_______ 。
(4)写出反应②的化学方程式:_______ 。
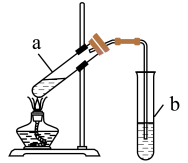
(5)实验室通过下图装置制备乙酸乙酯,浓硫酸的作用是_______ ,试管b中溶液是_______ ,请指出该装置的一处明显错误_______ 。
(6)E是乙酸乙酯的同分异构体,且E能与 溶液反应,则E的结构简式可能为(写出1种):
溶液反应,则E的结构简式可能为(写出1种):_______ 。

(1)A为乙烯的同系物,相对分子质量比乙烯大14,根据乙烯的性质推测A的性质,下列说法
A.A与 在一定条件下能发生取代反应 在一定条件下能发生取代反应 |
B.A与溴水反应产物为 |
C.A发生加成聚合产物为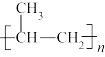 |
| D.A不能使酸性高锰酸钾溶液褪色 |
(2)D的结构简式为:
(3)写出反应①的反应类型:
(4)写出反应②的化学方程式:
(5)实验室通过下图装置制备乙酸乙酯,浓硫酸的作用是

(6)E是乙酸乙酯的同分异构体,且E能与
 溶液反应,则E的结构简式可能为(写出1种):
溶液反应,则E的结构简式可能为(写出1种):
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表是学习化学的重要工具。下表为某些元素在周期表中的位置。
(1)下图所示的模型表示的分子中,可由a、b形成的是___________ (填字母) 。写出C分子的空间构型为___________ ,D分子的结构简式是___________ 。
A.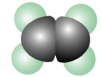 B.
B.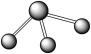 C.
C.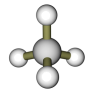 D.
D.
(2)b元素是形成有机物的主要元素,下列分子中同时含有sp和 两种杂化方式的是___________(填字母)。
两种杂化方式的是___________(填字母)。
(3)上述元素中最容易形成正离子的金属元素是___________ (填元素符号),写出该正离子的最外层电子的轨道表达式为___________ 。
(4)i、j元素与氢元素形成的化合物中,___________ (填化学式)的稳定性更强。
(5)f在d单质中燃烧产物的电子式是___________ 。
| a | |||||||||||||||||
| b | c | d | e | ||||||||||||||
| f | i | j | |||||||||||||||
| k | |||||||||||||||||
A.
 B.
B. C.
C. D.
D.
(2)b元素是形成有机物的主要元素,下列分子中同时含有sp和
 两种杂化方式的是___________(填字母)。
两种杂化方式的是___________(填字母)。A.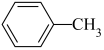 | B. | C. | D.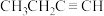 |
(4)i、j元素与氢元素形成的化合物中,
(5)f在d单质中燃烧产物的电子式是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐3】根据图中的反应路线及所给信息填空。

(1)A的结构简式是___________ ,名称是___________ 。
(2)①的反应类型是___________ 。
(3)反应③的化学方程式是___________ 。
(4)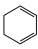 与Br2的CCl4溶液发生1,4-加成产物的结构简式是
与Br2的CCl4溶液发生1,4-加成产物的结构简式是___________ 。
(5)图为某药物中间体的结构示意图,试回答下列问题:
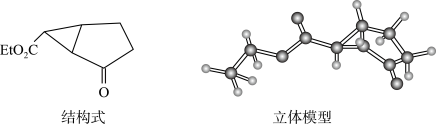
①观察结构式与立体模型,通过对比指出结构式中的“Et”表示___________ (用结构简式表示);该药物中间体分子的化学式为___________ 。
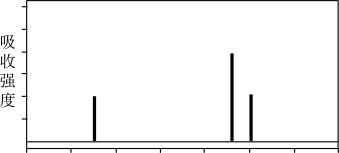
②现某种芳香族化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如图所示,试写出该化合物的结构简式:___________ 。

(1)A的结构简式是
(2)①的反应类型是
(3)反应③的化学方程式是
(4)
 与Br2的CCl4溶液发生1,4-加成产物的结构简式是
与Br2的CCl4溶液发生1,4-加成产物的结构简式是(5)图为某药物中间体的结构示意图,试回答下列问题:

①观察结构式与立体模型,通过对比指出结构式中的“Et”表示
②现某种芳香族化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如图所示,试写出该化合物的结构简式:

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4,请回答下列问题:
(1)用电子式表示 的形成过程
的形成过程_____________________ 。
(2)W在周期表中的位置是________________ 。
(3)X、Y、Z形成化合物的电子式为______ , 中含有的化学键类型为
中含有的化学键类型为________________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是__________ (用元素的离子符号表示)。
(5)下列说法能证明非金属性Q强于R的是______ (填字母)。
a.简单阴离子的还原性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性:
(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(1)用电子式表示
 的形成过程
的形成过程(2)W在周期表中的位置是
(3)X、Y、Z形成化合物的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:

b.简单氢化物热稳定性:

c.氧化物对应的水化物的酸性:

(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】我国科学家使用了新的铝铍埋藏测年法测量北京猿人的生存年代。这种方法的测量对象是石英(二氧化硅),它是砂石的主要成分。当宇宙射线打到地面时,会将石英中的硅原子和氧原子打破,生成铝和铍的同位素。只要测出一块石头中26Al和10Be的含量,就能推算出它被埋入地下的时间。完成下列填空:
(1)写出Be的核外电子排布式_______ 。Be所在的周期中,最外层有2个未成对电子的元素的符号是_______ 、_______ 。
(2)写出Al的最外层电子轨道表示式_______ 。铝原子核外有_______ 种运动状态不同的电子;铝原子核外有_______ 种能量不同的电子。有一种与26Al中子数相同的硅的核素,写出该核素符号_______ ,该硅电负性_______ (填“大于”或“小于”)Al 。
(3)比较Al3+、S2-和Cl-半径由大到小的顺序_______ ;这3种元素最高价氧化物对应的水化物中酸性最强的是_______ (写化学式)。
(4)铝单质在氧气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_______ 。铝元素最高价氧化物与氢氧化钠溶液反应的化学方程式_______ 。
(1)写出Be的核外电子排布式
(2)写出Al的最外层电子轨道表示式
(3)比较Al3+、S2-和Cl-半径由大到小的顺序
(4)铝单质在氧气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】短周期A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的化合物DF是常用的调味品。试根据以上叙述回答:
(1)写出下列元素名称:A_______ ,B_______ ,C_______ ,D_______ 。
(2)E在元素周期表中的位置:_______ 。
(3)F的离子结构示意图:_______ 。
(4)B、C、D的原子半径由大到小的顺序是_______ 。(用元素符号表示)
(5)C、D按原子个数比1∶1组成的一种化合物与水发生反应的化学方程式为_______ 。
(6)D单质制备漂白液的化学反应方程式_______ 。
(1)写出下列元素名称:A
(2)E在元素周期表中的位置:
(3)F的离子结构示意图:
(4)B、C、D的原子半径由大到小的顺序是
(5)C、D按原子个数比1∶1组成的一种化合物与水发生反应的化学方程式为
(6)D单质制备漂白液的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】2022年是门捷列夫发现元素周期律 153 周年,下图为元素周期表的一部分。门捷列夫预言了多种当时未知的元素,T 为其中之一、L在地壳中含量排第二位,广泛应用于信息技术等领域。
(1)写出J的原子结构示意图___________ 。
(2)下列说法不正确的是___________。
(3)已知JQ2结构中只含有极性共价键,试画出其结构式:___________ (用元素符号表示)。
(4)非金属性Q___________ M(用<、=、>来表示),判断依据是(试用一个化学方程式来表示)___________ 。
| X | Y | Z | ||
| L | J | Q | ||
| T | M |
(2)下列说法不正确的是___________。
| A.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ2 |
| B.Q、J的氧化物的水化物酸性:J<Q |
| C.用pH试纸测得Q单质的水溶液pH=3 |
| D.原子半径大小:L>J>Z |
(4)非金属性Q
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】 在光照条件下与
在光照条件下与 反应,可得到各种氯代甲烷。
反应,可得到各种氯代甲烷。
(1)在甲烷分子中,碳原子以最外层的4个电子分别与氢原子形成4个_______ 键。
(2)生成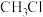 的化学方程式是
的化学方程式是_______ 。
(3)① 氯代的反应机理为自由基(带有单电子的原子或原子团,如
氯代的反应机理为自由基(带有单电子的原子或原子团,如 、
、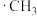 )反应,包括以下几步:
)反应,包括以下几步:
由 生成
生成 过程中,链传递其中一个方程式是
过程中,链传递其中一个方程式是 ,写出另一个方程式:
,写出另一个方程式:_______ 。
②探究光照对 与
与 反应的影响,实验如下:
反应的影响,实验如下:
a.由B和D得出的结论是_______ 。
b.依据上述反应机理,解释C中没有氯代甲烷的原因:_______ 。
 在光照条件下与
在光照条件下与 反应,可得到各种氯代甲烷。
反应,可得到各种氯代甲烷。(1)在甲烷分子中,碳原子以最外层的4个电子分别与氢原子形成4个
(2)生成
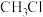 的化学方程式是
的化学方程式是(3)①
 氯代的反应机理为自由基(带有单电子的原子或原子团,如
氯代的反应机理为自由基(带有单电子的原子或原子团,如 、
、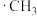 )反应,包括以下几步:
)反应,包括以下几步:| Ⅰ链引发 | Ⅱ链传递 | Ⅲ链终止 |
 | 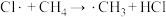 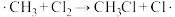 …… |   …… |
 生成
生成 过程中,链传递其中一个方程式是
过程中,链传递其中一个方程式是 ,写出另一个方程式:
,写出另一个方程式:②探究光照对
 与
与 反应的影响,实验如下:
反应的影响,实验如下:| 编号 | 操作 | 结果 |
| A | 将 与 与 混合后,光照 混合后,光照 | 得到氯代甲烷 |
| B | 将 先用光照,然后迅速在黑暗中与 先用光照,然后迅速在黑暗中与 混合 混合 | 得到氯代甲烷 |
| C | 将 先用光照,然后在黑暗中放置一段时间,再与 先用光照,然后在黑暗中放置一段时间,再与 混合 混合 | 几乎无氯代甲烷 |
| D | 将 先用光照,然后迅速在黑暗中与 先用光照,然后迅速在黑暗中与 混合 混合 | 几乎无氯代甲烷 |
b.依据上述反应机理,解释C中没有氯代甲烷的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】2022年央视春晚的舞蹈剧《只此青绿》灵感来自北宋卷轴画《千里江山图》,舞台的蓝色场景美轮美奂,气象磅礴,吞吐山河,该卷长11.91米,颜色绚丽,由石绿、雌、赭石、砗磲、朱砂等颜料绘制而成。回答以下问题:
(1)石绿,又名石青、蓝矿石,其主要成分为Cu3(CO3)2(OH)2。Cu2+在不同的溶剂中显示的颜色有差异,是因为形成了不同的配离子,某研究学习小组进行了如下实验探究:
①将白色硫酸铜粉末溶解于水中,溶液呈蓝色,是因为生成了一种蓝色的配位数为4的配离子,请写出生成此配离子的离子方程式:_____ 。并写出此配离子的结构简式(必须将配位键表示出来)_____ 。1mol该配离子中含有σ键的个数为______ 。
②向硫酸铜溶液中逐滴加入氨水,形成蓝色沉淀,请写出该反应的离子方程式:______ ;继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,请写出该反应的离子方程式:_____ ;再加入乙醇后,析出深蓝色的晶体_____ (写出化学式)。
(2)中国自古有“信口雌黄”、“雄黄入药”之说。雄黄As4S4和雌黄As2S3,都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图1所示。
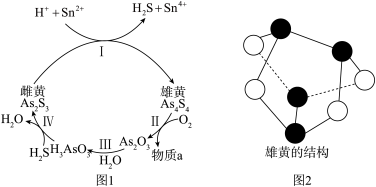
①如图2为雄黄(As4S4)结构图,分子中是否含有S-S键_____ (填“是”或“否”)。已知雌黄中没有π键且各原子最外层均达8电子稳定结构,试画出其结构图_____ 。
②转化的中间产物H3AsO3,是一种三元弱酸,且As原子上有一对孤电子对,其结构简式为_____ 。
(1)石绿,又名石青、蓝矿石,其主要成分为Cu3(CO3)2(OH)2。Cu2+在不同的溶剂中显示的颜色有差异,是因为形成了不同的配离子,某研究学习小组进行了如下实验探究:
①将白色硫酸铜粉末溶解于水中,溶液呈蓝色,是因为生成了一种蓝色的配位数为4的配离子,请写出生成此配离子的离子方程式:
②向硫酸铜溶液中逐滴加入氨水,形成蓝色沉淀,请写出该反应的离子方程式:
(2)中国自古有“信口雌黄”、“雄黄入药”之说。雄黄As4S4和雌黄As2S3,都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图1所示。

①如图2为雄黄(As4S4)结构图,分子中是否含有S-S键
②转化的中间产物H3AsO3,是一种三元弱酸,且As原子上有一对孤电子对,其结构简式为
您最近一年使用:0次



