铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是____ (填字母代号)。
(2)向沸水中逐滴滴加lmol/LFeCl3溶液,至____ ,该分散系中粒子直径的范围是____ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:____ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:首先取少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是____ ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,____ (填实验操作,下同)、洗涤、干燥,称量沉淀质量为43.05g。则待测溶液中,FeCl3的物质的量浓度为____ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是____ (填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①____ ;②____ ;③____ ;④____ 。
B.请写出通入⑥的化学方程式:_____ 。
(1)所含铁元素既有氧化性又有还原性的物质是
| A.Fe | B.FeCl2 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①
B.请写出通入⑥的化学方程式:
更新时间:2022-08-23 16:46:31
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)现有下列物质:①小苏打② 晶体③
晶体③ ④
④ 溶液⑤液态的
溶液⑤液态的 ⑥酒精(
⑥酒精( )⑦铜。上述物质中:能导电的是
)⑦铜。上述物质中:能导电的是_______ (填序号,下同);属于酸性氧化物的是_______ 。属于电解质的是_______ 。溶于水后形成的水溶液不能导电的是_______ 。
(2)同学们吃的食品包装袋中经常有一个小纸袋,上面写着“干燥剂”, 其主要成分是生石灰( )。
)。
①生石灰属于哪类氧化物:_______ 。
②生石灰可作干燥剂的理由是(用化学方程式表示)_______ 。
(3)某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。①现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,其中正确的是_______ (填序号)。
a.甲同学的操作:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙直接加热饱和氯化铁溶液;
c.丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
②制备氢氧化铁胶体的化学方程式是_______ 。
③证明有氢氧化铁胶体生成的实验操作是_______ 。
(1)现有下列物质:①小苏打②
 晶体③
晶体③ ④
④ 溶液⑤液态的
溶液⑤液态的 ⑥酒精(
⑥酒精( )⑦铜。上述物质中:能导电的是
)⑦铜。上述物质中:能导电的是(2)同学们吃的食品包装袋中经常有一个小纸袋,上面写着“干燥剂”, 其主要成分是生石灰(
 )。
)。①生石灰属于哪类氧化物:
②生石灰可作干燥剂的理由是(用化学方程式表示)
(3)某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。①现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,其中正确的是
a.甲同学的操作:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙直接加热饱和氯化铁溶液;
c.丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
②制备氢氧化铁胶体的化学方程式是
③证明有氢氧化铁胶体生成的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定条件下,Co2+与肼在碱性环境中反应制得高纯度纳米钴。请完成相应的离子方程式_______ :
N2H4+Co2++ Co+N2↑+
Co+N2↑+
检验产品的颗粒尺寸是否为纳米级的简易方案是:_____________ 。
N2H4+Co2++
 Co+N2↑+
Co+N2↑+ 检验产品的颗粒尺寸是否为纳米级的简易方案是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】从不同的角度对物质进行分类有利于研究物质的组成与性质。现有以下5种物质:
①Cu②NaCl③饱和硫酸铁溶液④ ⑤干冰
⑤干冰
回答下列问题:
(1)以上物质能导电的有___________ (填序号)。
(2)以上物质属于电解质的有___________ (填序号)。
(3)分别写出②、④在水中的电离方程式___________ 、___________ 。
(4)①可溶解在③中,产物中金属元素均为+2价,该反应的离子方程式为___________ 。
(5)将少量③分别滴加到下列物质中,得到三种分散系a、b、c。

试将a、b、c符号以及对应的分散质具体的化学式填入下列方框中:___________ 。

①Cu②NaCl③饱和硫酸铁溶液④
 ⑤干冰
⑤干冰回答下列问题:
(1)以上物质能导电的有
(2)以上物质属于电解质的有
(3)分别写出②、④在水中的电离方程式
(4)①可溶解在③中,产物中金属元素均为+2价,该反应的离子方程式为
(5)将少量③分别滴加到下列物质中,得到三种分散系a、b、c。

试将a、b、c符号以及对应的分散质具体的化学式填入下列方框中:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题:
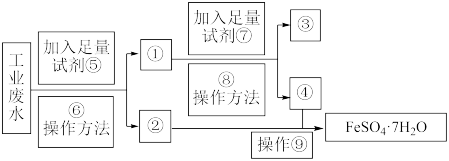
(1)⑥操作方法的名称是_______ ;操作⑨包括:蒸发浓缩、_______ 、过滤、洗涤、低温干燥。
(2)加入试剂⑤发生反应的离子方程式为_______ 。
(3)试剂⑦的化学式为_______ 。
(4)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0 mL ④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,其中涉及氧化还原反应的化学方程式为_______ 。
乙同学取2.0 mL ④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉及氧化还原反应的离子方程式为_______ 。

(1)⑥操作方法的名称是
(2)加入试剂⑤发生反应的离子方程式为
(3)试剂⑦的化学式为
(4)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0 mL ④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,其中涉及氧化还原反应的化学方程式为
乙同学取2.0 mL ④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉及氧化还原反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:

试回答:在“浸出”步骤中,为提高镁的浸出率,可采取的措施有_______ (两条即可)。

试回答:在“浸出”步骤中,为提高镁的浸出率,可采取的措施有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】稀土(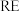 )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下: 熔点为
熔点为 ;月桂酸和
;月桂酸和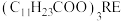 均难溶于水。该工艺条件下,稀土离子保持
均难溶于水。该工艺条件下,稀土离子保持 价不变;
价不变;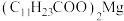 的
的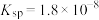 ,
, 开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
(1)“氧化调pH”中,化合价有变化的金属离子是_______ 。
(2)“过滤1”前,用 溶液调pH至
溶液调pH至_______ 的范围内,该过程中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)①“加热搅拌”有利于加快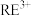 溶出、提高产率,其原因是
溶出、提高产率,其原因是_______ 。
②“操作X”的过程为:先_______ ,再固液分离。
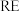 )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下: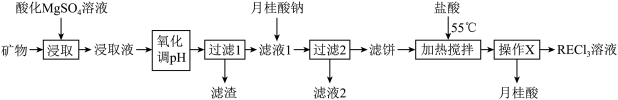
 熔点为
熔点为 ;月桂酸和
;月桂酸和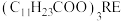 均难溶于水。该工艺条件下,稀土离子保持
均难溶于水。该工艺条件下,稀土离子保持 价不变;
价不变;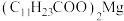 的
的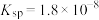 ,
, 开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。| 离子 |  |  |  | 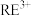 |
| 开始沉淀时的pH | 8.8 | 1.5 | 3.6 | 6.2~7.4 |
| 沉淀完全时的pH | / | 3.2 | 4.7 | / |
(1)“氧化调pH”中,化合价有变化的金属离子是
(2)“过滤1”前,用
 溶液调pH至
溶液调pH至 发生反应的离子方程式为
发生反应的离子方程式为(3)①“加热搅拌”有利于加快
 溶出、提高产率,其原因是
溶出、提高产率,其原因是②“操作X”的过程为:先
您最近一年使用:0次
填空题
|
适中
(0.65)
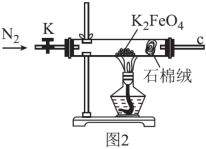
【推荐1】高铁酸钾(K2FeO4)是一种强氧化剂和环境友好型水处理剂,易分解,遇水和酸易变质。某学习小组在实验室对高铁酸钾的制备和一些性质进行探究。用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,_______ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】看实验操作(如下图)完成下列各题。
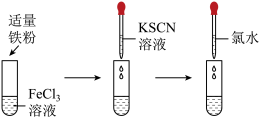
(1)实验现象:加适量铁粉振荡后,溶液变成_______ ,再加KSCN溶液,再滴加氯水后,溶液变成_______ 。
(2)结论:Fe3+遇到较强的还原剂时,会被还原成_______ ,Fe2+在较强的氧化剂的作用下会被氧化成_______ 。

(1)实验现象:加适量铁粉振荡后,溶液变成
(2)结论:Fe3+遇到较强的还原剂时,会被还原成
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某同学设计下图所示装置,用粗铁粒与189g·L-1硝酸反应制取NO气体。

完全反应后,A装置烧杯里含铁的价态可能是________________ 。
现有仪器和药品:试管和胶头滴管,0.1mol·L-1KSCN溶液、0.1mol·L-1KI溶液、0.2mol·L-1酸性KMnO4溶液、氯水等。
请你设计一个简单实验,探究上述判断,填写下列实验报告:

完全反应后,A装置烧杯里含铁的价态可能是
现有仪器和药品:试管和胶头滴管,0.1mol·L-1KSCN溶液、0.1mol·L-1KI溶液、0.2mol·L-1酸性KMnO4溶液、氯水等。
请你设计一个简单实验,探究上述判断,填写下列实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量溶液装于试管,向试管中滴入几滴KSCN溶液 | |
| 第二步 | 若溶液紫色退去,则说明含有Fe2+,若无明显变化,则说明不含Fe2+ |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】高铁酸盐具有极强的氧化性,可作水处理剂。低温下,在Na2FeO4溶液中加入KOH浓溶液可析出K2FeO4。完成下列填空:
(1)写出上述得到K2FeO4的化学方程式_____ 。
(2)Na2FeO4和稀H2SO4发生如下反应:Na2FeO4+H2SO4→Fe2(SO4)3+O2↑+Na2SO4+H2O。配平上述化学方程式_____ 。若反应中产生3.36L(标准状况)的氧气,则转移电子数为_____ 。
(3)实验室配制Fe2(SO4)3溶液时,需加入少量稀硫酸,结合离子方程式用化学平衡移动原理解释其原因______ 。
(4)在Fe2(SO4)3溶液中滴加NaHSO3溶液,n(SO42-)增大,则还原产物是____ 。写出检验上述反应中Fe2(SO4)3是否消耗完全的方法______ 。
(5)已知HSO3-在水中既能水解也能电离。NaHSO3溶液呈酸性,溶液中c(H2SO3)_____ c(SO32-)(选填“>”、“<”或“=”)。
(1)写出上述得到K2FeO4的化学方程式
(2)Na2FeO4和稀H2SO4发生如下反应:Na2FeO4+H2SO4→Fe2(SO4)3+O2↑+Na2SO4+H2O。配平上述化学方程式
(3)实验室配制Fe2(SO4)3溶液时,需加入少量稀硫酸,结合离子方程式用化学平衡移动原理解释其原因
(4)在Fe2(SO4)3溶液中滴加NaHSO3溶液,n(SO42-)增大,则还原产物是
(5)已知HSO3-在水中既能水解也能电离。NaHSO3溶液呈酸性,溶液中c(H2SO3)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图是某儿童在浏阳市医疗机构临床检验结果报告单的部分数据:
根据上表的数据,回答下列问题。
(1)该儿童_______ 元素含量偏低。
(2)缺铁性贫血患者补充的铁元素应为 。一些补铁剂以
。一些补铁剂以 为主要成分,某化学兴趣小组对市售的补铁药片是否变质进行检测,请帮助完成实验报告。
为主要成分,某化学兴趣小组对市售的补铁药片是否变质进行检测,请帮助完成实验报告。
(3)用 制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是_______ 。含有 的补铁药片与维生素C同服,可以达到更好的补铁效果,这个过程中体现维生素C的
的补铁药片与维生素C同服,可以达到更好的补铁效果,这个过程中体现维生素C的_______ (填“氧化性”或“还原性”)。
(4)不仅溶液中 易被氧化,
易被氧化, 更易被氧化,请写出溶液中的
更易被氧化,请写出溶液中的 被溶解在溶液中的
被溶解在溶液中的 氧化的化学方程式
氧化的化学方程式_______ 。请简要描述 被氧化的现象
被氧化的现象_______ 。
| 序号 | 分析项目 | 检测结果 | 单位 | 参考范围 |
| 1 | 锌(Zn) | 115.92 | μmol/L | 66-120 |
| 2 | 铁(Fe) | 8.95 | μmol/L | 7.52-11.82 |
| 3 | 钙(Ca) | 1.48 | μmol/L | 1.55-2.10 |
根据上表的数据,回答下列问题。
(1)该儿童
(2)缺铁性贫血患者补充的铁元素应为
 。一些补铁剂以
。一些补铁剂以 为主要成分,某化学兴趣小组对市售的补铁药片是否变质进行检测,请帮助完成实验报告。
为主要成分,某化学兴趣小组对市售的补铁药片是否变质进行检测,请帮助完成实验报告。| 实验步骤 | 实验现象 | 实验结论 |
步骤1:取市售 药片加入适量蒸馏水溶解 药片加入适量蒸馏水溶解 | 药片部分溶解 | |
| 步骤2:取少量步骤1所得溶液于试管,滴加几滴 | 补铁药片已变质。 |
(3)用
 制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是 的补铁药片与维生素C同服,可以达到更好的补铁效果,这个过程中体现维生素C的
的补铁药片与维生素C同服,可以达到更好的补铁效果,这个过程中体现维生素C的(4)不仅溶液中
 易被氧化,
易被氧化, 更易被氧化,请写出溶液中的
更易被氧化,请写出溶液中的 被溶解在溶液中的
被溶解在溶液中的 氧化的化学方程式
氧化的化学方程式 被氧化的现象
被氧化的现象
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知硫氰(SCN)2为拟卤素,其分子及阴离子的性质与卤素性质相似。完成下列填空:将硫氰化钾溶液与氯化铁溶液混合,溶液变为红色。
(1)写出该反应的化学方程式:________________________________ 。
(2)将生成的红色溶液分为三等份,进行如下实验(第三份是对照):
①第一份中滴加碘化钾溶液至过量,再加入四氯化碳,充分振荡,最终水层接近无色,四氯化碳层呈__________ 色,写出该过程的离子方程式:________________________ 。向该溶液中滴加少量溴水,水溶液又变为红色,则氧化性Br2________ (填“大于”“小于”或“无法确定”) (SCN)2。
②第二份中加入少量酸性高锰酸钾溶液,血红色褪去。完成并配平该反应的离子方程式_________________ 。若含________ mol高锰酸钾的溶液完全反应,转移电子2 mol。

(1)写出该反应的化学方程式:
(2)将生成的红色溶液分为三等份,进行如下实验(第三份是对照):
①第一份中滴加碘化钾溶液至过量,再加入四氯化碳,充分振荡,最终水层接近无色,四氯化碳层呈
②第二份中加入少量酸性高锰酸钾溶液,血红色褪去。完成并配平该反应的离子方程式

您最近一年使用:0次



