二氧化碳的“捕捉”与“封存”是实现温室气体减排的重要途径之一、实际生产中,经常利用足量NaOH溶液来“捕捉”CO2,流程图如图(部分条件及物质未标出)。

(1)用NaOH溶液喷淋“捕捉”空气中的CO2的优点是____ 。
(2)操作①中_____ (填“一定”“不一定”)含有过滤。
(3)上述工业流程中____ (选填A、B、C)内发生了分解反应。
A.吸收塔 B.分离池 C.煅烧炉
(4)上述流程中可以循环使用的物质是____ 。(写出其中一种即可)
(5)吸收塔中发生反应的化学方程式为____ 。

(1)用NaOH溶液喷淋“捕捉”空气中的CO2的优点是
(2)操作①中
(3)上述工业流程中
A.吸收塔 B.分离池 C.煅烧炉
(4)上述流程中可以循环使用的物质是
(5)吸收塔中发生反应的化学方程式为
更新时间:2022-08-22 10:17:55
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究性学习小组为了验证臭氧的氧化性强于氧气,进行了下述实验,请参与探究并回答相关问题.
[实验目的]验证臭氧的氧化性强于氧气
[实验原理]2KI+O3+H2O===2KOH+I2+O2,淀粉溶液遇单质碘变蓝色.
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计.
[实验步骤]①取a溶液与碘化钾溶液混合;
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上;
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧.将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等;
④观察现象并进行记录:
请根据上述实验原理、步骤及你所学的知识,回答下列问题:
(1)实验原理的化学反应的反应类型是________ (填序号).
A.离子反应 B.氧化还原反应
C.复分解反应 D.置换反应
E.分解反应 F.化合反应
(2)实验药品中的a溶液是________ 溶液.
(3)写出在臭氧消毒柜中产生O3的化学方程式:__________________________________ .
(4)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是:________________ .
(5)从实验数据记录不能得出的结论是________ (填序号).
A.O3的氧化性比O2强
B.氧气也能氧化碘化钾中的碘离子
C.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(6)在O3氧化KI的反应中,若有9.6 g O3发生反应,则转移电子的物质的量为________ .
[实验目的]验证臭氧的氧化性强于氧气
[实验原理]2KI+O3+H2O===2KOH+I2+O2,淀粉溶液遇单质碘变蓝色.
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计.
[实验步骤]①取a溶液与碘化钾溶液混合;
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上;
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧.将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等;
④观察现象并进行记录:
| 时间(min) | 0 | 15 | 30 | 45 | 60 | 90 | 120 | |
| 滤纸的颜色变化 | 玻璃(Ⅰ) 上的滤纸 | 白色 | 白色 | 灰色 | 浅蓝色 | 蓝色 | 蓝色 | 浅蓝色 |
| 玻璃 (Ⅱ) 上的滤纸 | 白色 | 白色 | 白色 | 白色 | 灰色 | 灰色 | 浅蓝色 | |
(1)实验原理的化学反应的反应类型是
A.离子反应 B.氧化还原反应
C.复分解反应 D.置换反应
E.分解反应 F.化合反应
(2)实验药品中的a溶液是
(3)写出在臭氧消毒柜中产生O3的化学方程式:
(4)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是:
(5)从实验数据记录不能得出的结论是
A.O3的氧化性比O2强
B.氧气也能氧化碘化钾中的碘离子
C.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(6)在O3氧化KI的反应中,若有9.6 g O3发生反应,则转移电子的物质的量为
您最近半年使用:0次
【推荐2】如图五角星上排列的A、B、C、D、E五种物质均为中学化学中常见的化合物,相互之间的连线表示两种物质能发生化学反应。
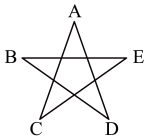
A、C、E均为氧化物,A是人体呼出的气体之一;在实验室中B可以用来制取A,而D可以用来检验A;C和E反应能生成D。
(1)写出下列物质的化学式:
A________ ,D________ ;
(2)B除了制取A之外的另一种用途是____________________________________ ;
(3)C和E反应的化学方程式为________________________________________
(4)这五种物质之间两两发生反应,其中没有涉及的基本反应类型是________ 。

A、C、E均为氧化物,A是人体呼出的气体之一;在实验室中B可以用来制取A,而D可以用来检验A;C和E反应能生成D。
(1)写出下列物质的化学式:
A
(2)B除了制取A之外的另一种用途是
(3)C和E反应的化学方程式为
(4)这五种物质之间两两发生反应,其中没有涉及的基本反应类型是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】已知无水AlCl3遇潮湿空气即产生大量白雾,实验室可用如图所示装置制备无水AlCl3。请回答:

(1)仪器a的名称是_______ 。
(2)装置A中发生反应的化学方程式_______ 。
(3)装置B盛放的试剂是_______ ,它的作用除降低氯气在水中的溶解量外还包括_______ 。
(4)装置G的作用是_______ (用离子方程式表示)。
(5)已知无水AlCl3遇潮湿空气,能发生复分解反应,产生大量的白雾,请写出该反应的化学方程式_______ 。

(1)仪器a的名称是
(2)装置A中发生反应的化学方程式
(3)装置B盛放的试剂是
(4)装置G的作用是
(5)已知无水AlCl3遇潮湿空气,能发生复分解反应,产生大量的白雾,请写出该反应的化学方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】最近小明对水产生了浓厚的兴趣。

(1)在化学课堂上,老师进行了电解水的实验,揭示了水的组成。右图实验中试管1中得到的气体在点燃之前要先进行验纯的原因是_____ 。
(2)小明放学回家后,主动帮妈妈刷碗,发现自来水洗不掉碗碟上的油污,发现加入少许洗涤剂就可以洗干净,是因为洗涤剂有_____ 作用。
(3)周末他取村子里的河水于玻璃杯中,倒入少量肥皂水,用筷子搅拌后发现有大量浮渣漂浮在水面上,无泡沫产生,说明河水是_____ (选填“硬水”或“软水”)。硬水的危害很大,生活中将硬水软化的方法是_____ 。
(4)晚上,小明在电视上看到保护水资源的呼吁。下列做法中,你认为有利于防治水体污染的是_____。
(5)小明从课本学习到水常用作溶剂,实验室配制质量分数为0.9%的氯化钠溶液,小明用量筒量取蒸馏水读数时,仰视凹液面的最低处,会引起所配溶液的溶质质量分数_____ (选填“大于”、“小于”或“等于”)0.9%。

(1)在化学课堂上,老师进行了电解水的实验,揭示了水的组成。右图实验中试管1中得到的气体在点燃之前要先进行验纯的原因是
(2)小明放学回家后,主动帮妈妈刷碗,发现自来水洗不掉碗碟上的油污,发现加入少许洗涤剂就可以洗干净,是因为洗涤剂有
(3)周末他取村子里的河水于玻璃杯中,倒入少量肥皂水,用筷子搅拌后发现有大量浮渣漂浮在水面上,无泡沫产生,说明河水是
(4)晚上,小明在电视上看到保护水资源的呼吁。下列做法中,你认为有利于防治水体污染的是_____。
| A.使用节水型马桶 | B.生活污水任意排放 |
| C.合理施用农药和化肥 | D.工业废水处理达标后排放 |
(5)小明从课本学习到水常用作溶剂,实验室配制质量分数为0.9%的氯化钠溶液,小明用量筒量取蒸馏水读数时,仰视凹液面的最低处,会引起所配溶液的溶质质量分数
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(1)玻璃棒是化学实验中常用的仪器之一,其主要用于搅拌、过滤或转移液体时的引流。下列实验过程中,通常不需要使用玻璃棒的是___________ (填序号,下同)
①用pH试纸测定Na2CO3溶液的pH
②用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
③实验室中用FeCl3溶液和沸水制取Fe(OH)3胶体
④用已知浓度的稀盐酸滴定未知浓度的氢氧化钠溶液
⑤取某溶液做焰色反应实验,检验该溶液中是否含有钠元素
(2)①下列仪器在使用前一定要检查是否漏液的是______________________ 。
a.容量瓶 b.冷凝管 c.碱式滴定管 d.长颈漏斗 e.分液漏斗
②检查装置气密性是化学实验中的重要操作之一。不进行气密性检查可能导致的后果是____________ 。
a.收集不到气体 b.造成环境污染
c.观察到的实验现象有误 d.引发爆炸事故
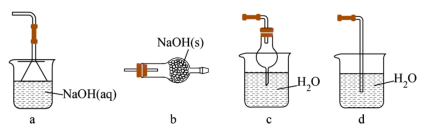
(3)下图所示装置可用于制备某种干燥的纯净气体。该装置中所盛装的药品正确的是_____________ 。
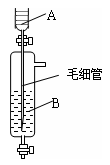
a.A中装浓硫酸,B中装浓盐酸
b.A中装浓盐酸,B中装浓硫酸
c.A中装氢氧化钠浓溶液,B中装浓氨水
d.A中装浓氨水,B中装氢氧化钠浓溶液
①用pH试纸测定Na2CO3溶液的pH
②用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
③实验室中用FeCl3溶液和沸水制取Fe(OH)3胶体
④用已知浓度的稀盐酸滴定未知浓度的氢氧化钠溶液
⑤取某溶液做焰色反应实验,检验该溶液中是否含有钠元素
(2)①下列仪器在使用前一定要检查是否漏液的是
a.容量瓶 b.冷凝管 c.碱式滴定管 d.长颈漏斗 e.分液漏斗
②检查装置气密性是化学实验中的重要操作之一。不进行气密性检查可能导致的后果是
a.收集不到气体 b.造成环境污染
c.观察到的实验现象有误 d.引发爆炸事故
(3)下图所示装置可用于制备某种干燥的纯净气体。该装置中所盛装的药品正确的是

a.A中装浓硫酸,B中装浓盐酸
b.A中装浓盐酸,B中装浓硫酸
c.A中装氢氧化钠浓溶液,B中装浓氨水
d.A中装浓氨水,B中装氢氧化钠浓溶液
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
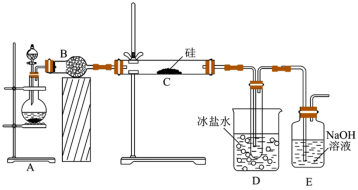
【推荐3】三氯硅烷(SiHCl3)可用于生产有机硅化合物、多晶硅。实验室先用NaCl固体与浓硫酸混合加热制取HCl,再利用HCl和硅粉制备三氯硅烷,实验装置如下图(加热仪器已略去)。回答下列问题: SiHCl3+H2
SiHCl3+H2
②三氯硅烷的熔点 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。
(1)装置B的名称_______ ,装置B中所装药品是_______ (填“碱石灰”或“无水氯化钙”)。
(2)加热前要先通一段时间HCl气体,原因是_______ 。
(3)装置D中冰盐水的作用是_______ 。
(4)该实验装置存在明显不足,请指出:_______ 。
(5)已知 在高温条件下易分解生成
在高温条件下易分解生成 和HCl。利用
和HCl。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图所示,写出该反应的化学方程式:
)的装置如图所示,写出该反应的化学方程式:_______ 。_______ (填序号)。
 SiHCl3+H2
SiHCl3+H2 ②三氯硅烷的熔点
 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。(1)装置B的名称
(2)加热前要先通一段时间HCl气体,原因是
(3)装置D中冰盐水的作用是
(4)该实验装置存在明显不足,请指出:
(5)已知
 在高温条件下易分解生成
在高温条件下易分解生成 和HCl。利用
和HCl。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图所示,写出该反应的化学方程式:
)的装置如图所示,写出该反应的化学方程式: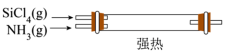
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某实验小组设计如下实验装置(夹持仪器已省略)制备干燥的 ,并在碱性条件下制备
,并在碱性条件下制备 (反应原理:
(反应原理: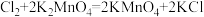 ,
, 溶液为绿色)。回答下列问题:
溶液为绿色)。回答下列问题:
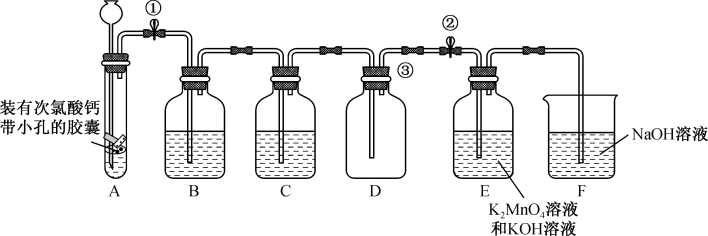
(1)设计次氯酸钙装入带有小孔的胶囊的目的是_______ 。
(2)B、C中盛放的试剂分别为_______ 、_______ (填名称)。
(3)实验时,首先组装装置,然后_______ ,再将各装置中加入相应的试剂后,将浓盐酸从_______ (填仪器名称)加入试管中,写出试管中反应的化学方程式:_______ 。
(4)装置E中反应已完成的现象是_______ 。
(5)装置F的作用是_______ (用离子方程式表示)。
(6)从装置E的溶液中获取 固体的方法是蒸发浓缩、
固体的方法是蒸发浓缩、_______ 、过滤、洗涤干燥。
(7)采用紫外一可见分光光度法测试高锰酸钾样品的纯度。准确称取0.70g高锰酸钾样品配制1000mL 溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为
溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为 (式中A为吸光度,C为高锰酸钾浓度,单位为
(式中A为吸光度,C为高锰酸钾浓度,单位为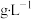 ,a、b为常数)。
,a、b为常数)。
根据上表相关数据可计算出高锰酸钾样品的纯度为_______ %(保留三位有效数字)。
 ,并在碱性条件下制备
,并在碱性条件下制备 (反应原理:
(反应原理: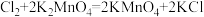 ,
, 溶液为绿色)。回答下列问题:
溶液为绿色)。回答下列问题:
(1)设计次氯酸钙装入带有小孔的胶囊的目的是
(2)B、C中盛放的试剂分别为
(3)实验时,首先组装装置,然后
(4)装置E中反应已完成的现象是
(5)装置F的作用是
(6)从装置E的溶液中获取
 固体的方法是蒸发浓缩、
固体的方法是蒸发浓缩、(7)采用紫外一可见分光光度法测试高锰酸钾样品的纯度。准确称取0.70g高锰酸钾样品配制1000mL
 溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为
溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为 (式中A为吸光度,C为高锰酸钾浓度,单位为
(式中A为吸光度,C为高锰酸钾浓度,单位为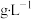 ,a、b为常数)。
,a、b为常数)。 | 0.50 | 0.70 | 待测溶液 |
| A(吸光度) | 0.30 | 0.40 | 0.39 |
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某工厂的工业废水中含有大量的 FeSO4、较多的 CuSO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图完成回收硫酸亚铁和铜的简单实验方案,回答下列问题:(图中所加试剂均为过量,流程图中无需填写)

(1)操作f的名称为____________ ,物质c的成分_________________
(2)试剂a的化学式为_____ ,加入该试剂所发生的化学方程式为______________ 。
(3) 请写出c→h+k的化学方程式______________

(1)操作f的名称为
(2)试剂a的化学式为
(3) 请写出c→h+k的化学方程式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】铁及其化合物有着广泛的用途。
(1)纳米铁制备:用草酸亚铁晶体在700℃下焙烧反应制备纳米零价铁,其化学反应方程式: 。当生成
。当生成 时,转移电子的物质的量为
时,转移电子的物质的量为____ 。
(2)纳米铁粉可以高效地去除被污染水体中的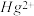 等重金属离子,其本质是
等重金属离子,其本质是____ (用离子方程式表示)。
(3)纳米铁除水体中 :将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中
:将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中 ,其都分反应原理如图所示,与不添加铜粉相比,添加少量铜粉时去除
,其都分反应原理如图所示,与不添加铜粉相比,添加少量铜粉时去除 效率更高,其主要原因是
效率更高,其主要原因是____ 。

(4)铁红(主要成分为 )是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
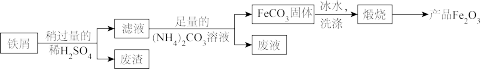
①写出加入 溶液的反应生成
溶液的反应生成 沉淀的离子方程式
沉淀的离子方程式_______ 。
②若煅烧不充分,产品 中会含有
中会含有 ,为了避免产品中有FeO,可采取的措施是
,为了避免产品中有FeO,可采取的措施是_______ (答一种即可)。
③称取3.0g产品,用足量稀硫酸溶解,逐滴加入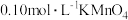 溶液20mL,二者恰好反应完全。若此产品中只含有
溶液20mL,二者恰好反应完全。若此产品中只含有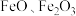 ,求产品中
,求产品中 的质量分数
的质量分数_______ 。
(1)纳米铁制备:用草酸亚铁晶体在700℃下焙烧反应制备纳米零价铁,其化学反应方程式:
 。当生成
。当生成 时,转移电子的物质的量为
时,转移电子的物质的量为(2)纳米铁粉可以高效地去除被污染水体中的
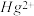 等重金属离子,其本质是
等重金属离子,其本质是(3)纳米铁除水体中
 :将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中
:将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中 ,其都分反应原理如图所示,与不添加铜粉相比,添加少量铜粉时去除
,其都分反应原理如图所示,与不添加铜粉相比,添加少量铜粉时去除 效率更高,其主要原因是
效率更高,其主要原因是
(4)铁红(主要成分为
 )是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
①写出加入
 溶液的反应生成
溶液的反应生成 沉淀的离子方程式
沉淀的离子方程式②若煅烧不充分,产品
 中会含有
中会含有 ,为了避免产品中有FeO,可采取的措施是
,为了避免产品中有FeO,可采取的措施是③称取3.0g产品,用足量稀硫酸溶解,逐滴加入
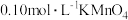 溶液20mL,二者恰好反应完全。若此产品中只含有
溶液20mL,二者恰好反应完全。若此产品中只含有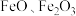 ,求产品中
,求产品中 的质量分数
的质量分数
您最近半年使用:0次



