化学反应中一定伴随着能量的变化,下列有关能量的说法正确的是
| A.相同条件下,等物质的量的硫蒸气和硫粉分别完全燃烧,前者放出热量多 |
B.已知 、 、 条件下: 条件下: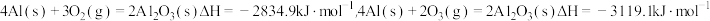 ,则 ,则 比 比 稳定 稳定 |
C.根据热化学方程式: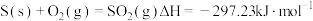 ,可推知 ,可推知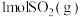 的能量总和大于 的能量总和大于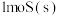 和 和 的能量总和 的能量总和 |
D.在稀水溶液中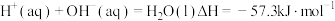 ,将含 ,将含 的浓硫酸与含 的浓硫酸与含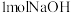 的溶液混合时,放出的热量小于 的溶液混合时,放出的热量小于 |
更新时间:2022-09-02 10:07:56
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列与化学反应能量变化相关的叙述正确的是
| A.能量变化的同时一定发生了化学变化 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知下列反应的平衡常数:
S(s)+ O2(g)⇌SO2(g),K1;
H2(g) +S(s)⇌H2S(g), K2;
则反应H2(g) +SO2(g)⇌O2(g) +H2S(g)的平衡常数是
S(s)+ O2(g)⇌SO2(g),K1;
H2(g) +S(s)⇌H2S(g), K2;
则反应H2(g) +SO2(g)⇌O2(g) +H2S(g)的平衡常数是
| A.K1+K2 | B.K2−K1 | C.K1 ×K2 | D.K2/K1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知H+(aq)+OH-(aq) ═ H2O(l) ΔH=-57.3 kJ/mol,下列说法正确的是
| A.当用稀CH3COOH(aq)和稀NaOH(aq)生成1 mol H2O(l)时,反应热为ΔH1,ΔH1>ΔH |
| B.用含1 mol HCl的稀HCl(aq)和40 g NaOH固体反应生成1 mol H2O(l)时,反应热为ΔH1,ΔH1>ΔH |
| C.含1 mol H2SO4的稀溶液和含1 mol Ba(OH)2的稀溶液完全反应,放出57.3 kJ的热量 |
| D.中和反应中,反应物的总能量低于生成物的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关中和反应反应热测定实验的说法正确的是
| A.温度计能代替玻璃搅拌器,用于搅拌反应物 |
| B.强酸与强碱反应生成1molH2O(l)释放的热量都约为57.3kJ |
| C.该实验中,读取混合溶液不再变化的温度为终止温度 |
| D.内筒内若有水残留,会使测得的反应热数值绝对值偏小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】含有11.2g KOH的稀溶液与1L 0.1mol·L﹣1的H2SO4溶液反应,放出11.46kJ的热量,下列热化学方程式正确的是( )
A.KOH(aq)+ H2SO4(aq)═ H2SO4(aq)═ K2SO4(aq)+H2O(l) △H=﹣11.46 kJ·mol﹣1 K2SO4(aq)+H2O(l) △H=﹣11.46 kJ·mol﹣1 |
| B.2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l) △H=﹣11.46 kJ·mol﹣1 |
| C.2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l) △H=+114.6 kJ·mol﹣1 |
D.KOH(aq)+ H2SO4(aq)═ H2SO4(aq)═ K2SO4(aq)+H2O(l) △H=﹣57.3 kJ·mol﹣1 K2SO4(aq)+H2O(l) △H=﹣57.3 kJ·mol﹣1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】利用含碳化合物合成燃料,已知 反应过程中的能量变化如下图,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的情况。下列判断正确的是
反应过程中的能量变化如下图,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的情况。下列判断正确的是

 反应过程中的能量变化如下图,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的情况。下列判断正确的是
反应过程中的能量变化如下图,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的情况。下列判断正确的是
A.如果该反应生成液态 ,则ΔH增大 ,则ΔH增大 |
| B.加入催化剂,该反应的活化能和ΔH均变小 |
C.该反应的 |
| D.反应物的总能量大于生成物的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列说法正确的是( )
| A.燃烧热和中和热的数值都会随反应物的用量不同而改变,故1molS(s)和2molS(s)的燃烧热不相等 |
| B.已知:2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+O2(g)=2CO(g)ΔH=bkJ/mol,则a>b |
| C.H2(g)的燃烧热为285.8kJ/mol,则表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ/mol |
| D.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ/mol,在低温条件下不能自发进行,但在高温条件下能自发进行 |
您最近一年使用:0次



