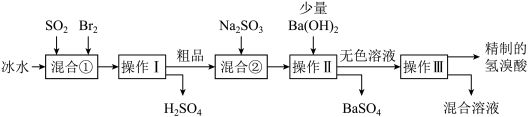
劳动创造价值。下列有关物质的性质与劳动具有对应关系的是
| A.NH4NO3分解产生大量气体,可用作汽车安全气囊产气药 |
| B.SO2具有漂白性,可用于制溴工业中吸收Br2 |
| C.FeCl3溶液显酸性,可用于蚀刻铜制的电路板 |
| D.MnO2不溶于水,可用作H2O2分解的催化剂 |
更新时间:2022-04-11 08:15:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列变化不属于化学变化的有几项
①用铁质容器盛放浓硝酸 ②给装有氯化铵的试管加热,在管口又有白色晶体产生 ③液氮用作制冷剂 ④ 明矾用作净水剂 ⑤碳酸钠晶体的风化 ⑥用氢氟酸刻蚀石英制艺术品 ⑦二氧化氮气体遇冷颜色变浅
①用铁质容器盛放浓硝酸 ②给装有氯化铵的试管加热,在管口又有白色晶体产生 ③液氮用作制冷剂 ④ 明矾用作净水剂 ⑤碳酸钠晶体的风化 ⑥用氢氟酸刻蚀石英制艺术品 ⑦二氧化氮气体遇冷颜色变浅
| A.0 | B.1 | C.2 | D.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】“增蓝天,保碧水,护净土”,江苏省正加快推进生态环境治理现代化建设。下列叙述正确的是
| A.推广使用煤气化和液化技术,获得清洁燃料和化工原料 |
| B.在一定条件下,选择合适的催化剂将CO2氧化为甲酸 |
| C.铵态氮肥使用时要深施覆土,是因为铵态氮肥易氧化变质 |
| D.纳米铁粉可以通过吸附作用高效地除去被污染水体中的Cu2+、Ag+等重金属离子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式正确且能用来解释相应实验现象的是
| 实验现象 | 离子方程式 | |
| A | 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 | Mg(OH)2+2NH =Mg2++2NH3•H2O =Mg2++2NH3•H2O |
| B | 向沸水中滴加饱和氯化铁溶液得到透明的红褐色液体 | Fe3++3H2O=Fe(OH)3↓+3H+ |
| C | 二氧化硫使酸性高锰酸钾溶液褪色 | 3SO2+2MnO +4H+=3SO +4H+=3SO +2Mn2++2H2O +2Mn2++2H2O |
| D | 向NaHSO4溶液中滴加Ba(OH)2溶液至SO 离子恰好沉淀完全 离子恰好沉淀完全 | Ba2++2OH-+2H++SO =BaSO4↓+2H2O =BaSO4↓+2H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作对应的现象和根据现象得出的结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A. | 在酸性高酸钾溶液中通入过量的SO2 | 溶液褪色 | 二氧化硫具有还原性 |
| B. | 碳和浓硫酸加热所得气体产物依次通过品红溶液和澄清石灰水 | 溶液褪色 | 气体产物中含有CO2和SO2 |
| C. | 常温下将铜加入浓硫酸中 | 溶液褪色 | 铜衣面生成致密的氧化膜 |
| D. | 足量的铜和浓硝酸反应,反应停止后,往溶液中加入稀硫酸 | 溶液褪色 | 铜和稀硫酸发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】取 1LFeCl3溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法错误的是
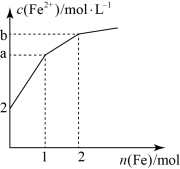
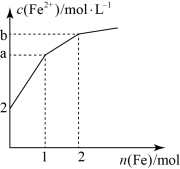
| A.当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+ |
| B.当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu |
| C.当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1 |
| D.腐蚀之前原溶液中n(Fe3+)=4 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组澄清溶液中离子能大量共存,且加(或滴入)X试剂后发生反应的离子方程式书写正确的是
| 选项 | 离子组 | 试剂X | 离子方程式 |
| A |  、 、 、 、 、 、 | 过量H2S | 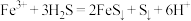 |
| B |  、 、 、 、 、 、 | 过量SO2 | 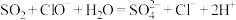 |
| C |  、 、 、 、 、 、 | 过量铜粉 | 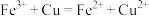 |
| D |  、 、 、 、 、 、 | 少量HCl | 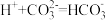 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】废旧铅蓄电池的铅膏主要含有 、
、 和Pb.从铅膏中回收
和Pb.从铅膏中回收 流程如下。
流程如下。
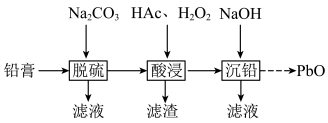
【已知: 性质类似
性质类似 】
】
下列说法错误的是
 、
、 和Pb.从铅膏中回收
和Pb.从铅膏中回收 流程如下。
流程如下。
【已知:
 性质类似
性质类似 】
】下列说法错误的是
A.“脱硫”是把 转化为 转化为 将硫除去 将硫除去 |
B.“酸浸”发生的反应有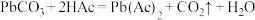 |
C.“酸浸”中 会分解,应适当过量 会分解,应适当过量 |
| D.“沉铅”时为保证铅的完全沉淀,应该加入过量氢氧化钠 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
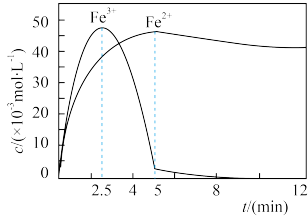
【推荐2】铁粉活化可用于污水处理。活化方法如下:向一定量表面被部分氧化的铁粉中加入少量稀盐酸和 (少量
(少量 有利于铁粉活化),搅拌。一段时间后,铁粉吸附
有利于铁粉活化),搅拌。一段时间后,铁粉吸附 形成胶体。活化过程中,溶液中
形成胶体。活化过程中,溶液中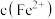 、
、 随时间变化如图所示。下列说法不合理的是
随时间变化如图所示。下列说法不合理的是
 (少量
(少量 有利于铁粉活化),搅拌。一段时间后,铁粉吸附
有利于铁粉活化),搅拌。一段时间后,铁粉吸附 形成胶体。活化过程中,溶液中
形成胶体。活化过程中,溶液中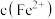 、
、 随时间变化如图所示。下列说法不合理的是
随时间变化如图所示。下列说法不合理的是
A.盐酸能与铁粉表面的 反应 反应 |
B. ,溶液的pH不断升高 ,溶液的pH不断升高 |
C. , , 减小, 减小,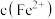 增加,可能发生反应: 增加,可能发生反应: |
D. 后, 后,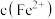 减小,可能是 减小,可能是 将 将 还原为 还原为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】氧泡泡是一种多功能新型漂白剂,其有效成分是过碳酸钠(xNa2CO3•yH2O2)。
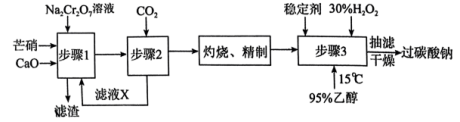
I.以芒硝(Na2SO4•10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如图:
Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使H2O2充分快速分解(催化剂不参与其它反应),然后加酚酞作指示剂,用0.0500mol•L-1H2SO4溶液滴定至终点,消耗硫酸V1mL。
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1H3PO4溶液,再加入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液V2mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
过碳酸钠制备的流程中,下列说法错误的是
I.以芒硝(Na2SO4•10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如图:

Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使H2O2充分快速分解(催化剂不参与其它反应),然后加酚酞作指示剂,用0.0500mol•L-1H2SO4溶液滴定至终点,消耗硫酸V1mL。
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1H3PO4溶液,再加入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液V2mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
过碳酸钠制备的流程中,下列说法错误的是
| A.步骤1中2mol芒硝参与反应时,消耗1molNa2Cr2O7 |
| B.滤渣的主要成分为CaSO4 |
C.步骤2的方程式为2Na2CrO4+2CO2+H2O Na2Cr2O7+2NaHCO3↓ Na2Cr2O7+2NaHCO3↓ |
| D.稳定剂的作用是阻止微量杂质金属离子的催化作用,减少双氧水的分解 |
您最近一年使用:0次

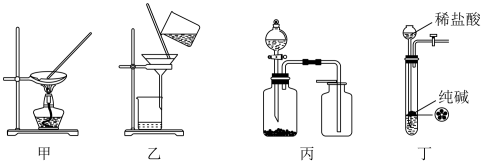
 的溶液
的溶液 气体
气体