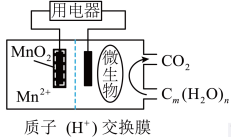
微生物燃料电池可用于净化含铬废水,其工作原理示意如图所示。该电池工作时,下列说法正确的是
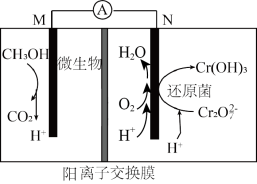

| A.M极是电池的正极 |
B.N极的电极反应为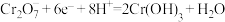 |
| C.电池工作时,电子由M极通过离子交换膜流向N极 |
D.电路中转移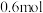 电子时,M极上有 电子时,M极上有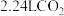 生成 生成 |
更新时间:2022-09-08 09:37:02
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是
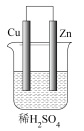
实验后的记录:
①Zn为正极,Cu为负极。
②H+向负极移动。
③电子流动方向:从Zn经外电路流向Cu。
④Cu极上有H2产生。
⑤若有1mol电子流过导线,则产生H2为0.5mol。
⑥正极的电极反应式为Zn-2e-===Zn2+。

实验后的记录:
①Zn为正极,Cu为负极。
②H+向负极移动。
③电子流动方向:从Zn经外电路流向Cu。
④Cu极上有H2产生。
⑤若有1mol电子流过导线,则产生H2为0.5mol。
⑥正极的电极反应式为Zn-2e-===Zn2+。
| A.①②③ | B.③④⑤ | C.④⑤⑥ | D.②③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】锌铜原电池(如图)工作时,下列叙述正确的是


| A.正极反应为Zn-2e-=Zn2+ | B.电池反应为Zn2++Cu=Zn+Cu2+ |
| C.盐桥中的K+移向CuSO4溶液 | D.在外电路中,电流从负极流向正极 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】微生物电池可用来处理废水中的对氯苯酚,其工作原理示意图如图。关于该电池的说法不正确 的是
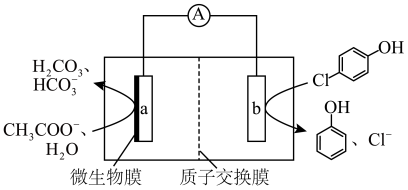

| A.a极是负极 |
| B.H+向b极迁移 |
C.b电极上发生的反应是 +H++2e-= +H++2e-=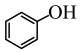 +Cl- +Cl- |
| D.生成0.1molH2CO3,电池反应电子转移数目为0.4mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
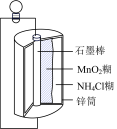
【推荐2】下列四个常用电化学装置的叙述错误的是
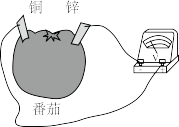 | 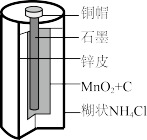 | 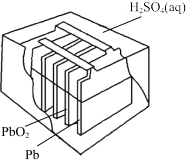 | 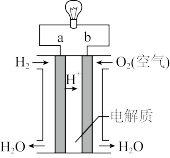 |
| 图I水果电池 | 图II干电池 | 图III铅蓄电池 | 图IV氢氧燃料电池 |
A.图  所示电池中,电子从锌片流出 所示电池中,电子从锌片流出 |
B.图  所示干电池中石墨作负极 所示干电池中石墨作负极 |
C.图  所示电池为二次电池 所示电池为二次电池 |
D.图  所示电池中正极反应为: 所示电池中正极反应为: |
您最近一年使用:0次
【推荐3】2019年诺贝尔化学奖授予在锂离子电池研究方面做出了贡献的三位科学家。高能LiFePO4电池的反应原理:xLiFePO4+nC FePO4+LixCn
FePO4+LixCn
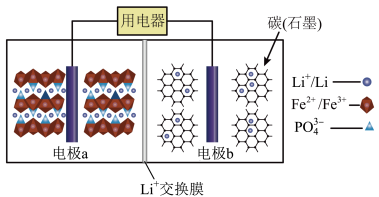
下列说法错误的是
 FePO4+LixCn
FePO4+LixCn
下列说法错误的是
| A.放电时,电子由电极b经导线、用电器、导线到电极a |
| B.充电时,Li+向右移动,电极b的电势大于电极a的电势 |
| C.充电时,电极b的电极反应式:LixCn-xe-===nC+xLi+ |
| D.放电时,电极a的电极反应式:xFePO4+xLi++xe-===xLiFePO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】一种钾离子电池的工作原理如图所示,下列说法正确的是
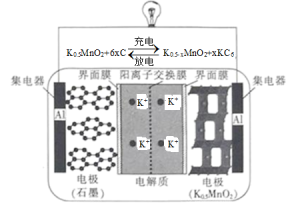

| A.放电时,K+通过阳离子交换膜向石墨电极移动 |
| B.放电时,负极的电极反应式:KC6-e-=K++6C |
| C.充电时,阳极的电极反应式:K0.5−xMnO2+xK++xe-=K0.5MnO2 |
| D.若仅把钾离子换成锂离子,当负极减少的质量相同时,钾离子电池转移的电子数比锂离子电池的多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】2021年6月17日,搭载神舟十二号载人飞船的长征二号F遥十二运载火箭成功发射,并顺利完成与天和核心舱对接。核心舱电源系统由锂离子蓄电池组及太阳电池翼组成。锂离子蓄电池放电时的反应为: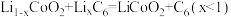 。下列说法正确的是
。下列说法正确的是
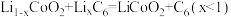 。下列说法正确的是
。下列说法正确的是| A.锂离子蓄电池比能量高,污染小,是理想的二次电池 |
B.锂离子蓄电池放电时, 在电解质中由正极向负极迁移 在电解质中由正极向负极迁移 |
C.充电时,阴极的电极反应式为: |
| D.锂离子蓄电池和太阳电池翼,均是将化学能转变为电能的装置 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】镁-锂双离子新型二次电池如图所示,下列关于该电池的说法正确的是
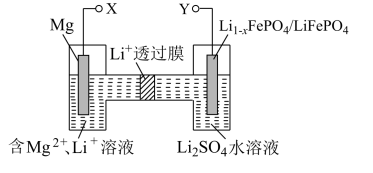

A.放电时,Mg作负极,溶液中 由右向左移动 由右向左移动 |
B.充电时,阳极的电极反应式为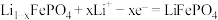 |
| C.充电时,Y应与外加电源的正极相连,此电极上的物质发生了还原反应 |
D.放电时,导线上每通过 ,左室溶液质量增重 ,左室溶液质量增重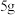 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】NA代表阿伏加德罗常数的值。下列说法正确的是
| A.1.7 g NH3完全溶于1 L H2O所得溶液中NH3·H2O微粒数目为0.1NA |
| B.14 g由乙烯和丙烯组成的混合气体中极性共价键数目为2NA |
| C.18 g D2O中含有的中子数为10NA |
| D.乙醇燃料电池负极消耗4.6 g乙醇时,电路中通过的电子数目为0.6NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是
| A.理论上锌的质量每减小13g,外电路中通过0.4mol电子 |
| B.电池工作时,锌作负极,失去电子,发生氧化反应,Zn被还原 |
| C.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
| D.电池工作时,氢氧化钾电解质溶液中OH-移向负极 |
您最近一年使用:0次