短周期元素X、Y、Z、W的原子序数依次增大,Z的一种常见氧化物是形成酸雨的罪魁祸首。X、Y、W可组成化合物I,I和Ca(OH)2共热的关系图如图:
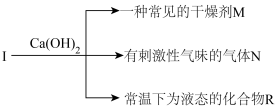
(1)W的元素符号为_______ ;Z原子的结构示意图为_______ 。
(2)I、N的电子式分别为_______ 、_______ 。
(3)I和Ca(OH)2共热的化学方程式为_______ 。
(4)I、M、N、R中离子化合物有_______ ;共价化合物有_______ 。

(1)W的元素符号为
(2)I、N的电子式分别为
(3)I和Ca(OH)2共热的化学方程式为
(4)I、M、N、R中离子化合物有
更新时间:2022-08-21 07:32:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,甲、乙、丙为常见化合物。它们之间有如下转化关系:

(1)乙与B的反应在工业上俗称__________ 反应,C电子式为____________ 。
(2)D与水蒸气反应的化学方程式为_________________________ 。
(3)甲的水溶液显_______ 性(填“酸”或“碱”),原因是(用离子方程式表示)_______________________ 。

(1)乙与B的反应在工业上俗称
(2)D与水蒸气反应的化学方程式为
(3)甲的水溶液显
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F、G、L、I九种主族元素分别位于三个不同的短周期,它们的原子序数依次增大,其中B、C、D位于同一周期,A与E、B与G、D与L分别位于同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,C和D的最外层电子数之和为11.请回答下列问题:
(1)元素B在周期表中的位置___________ ,,以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)___________ ,D、E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)___________ 。
(2)L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的结构式为___________ 。
(3)CI3常温下呈液态,可与水反应生成一种酸和一种碱,反应方程式为___________ 。
(4)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的化学方程式___________ 。
(1)元素B在周期表中的位置
(2)L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的结构式为
(3)CI3常温下呈液态,可与水反应生成一种酸和一种碱,反应方程式为
(4)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、M、R、W均为周期表中前四周期的元素。X的基态原子外围电子排布式为3s2;Y原子的L电子层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍。回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为___________ 。其基态原子有___________ 种能量不同的电子;
(2)X位于周期表中___________ 区;R的氢化物的稳定性比其上一周期同族元素氢化物的稳定性___________ 。(填“强”或“弱”)
(3)Y、Z、M、R的最高价氧化物对应的水化物中酸性最强的是___________ (填化学式)
(4)元素Z的氢化物的电子式为___________ ,该氢化物与元素Z的最高价氧化物对应的水化物反应的化学方程式为___________ 。
(1)W的基态原子的外围电子排布图为
(2)X位于周期表中
(3)Y、Z、M、R的最高价氧化物对应的水化物中酸性最强的是
(4)元素Z的氢化物的电子式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
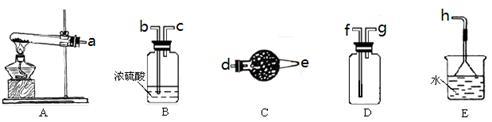
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选 填字母):a接______ ,______ 接______ ,______ 接h;
用A装置制取NH3的化学反应方程式为______
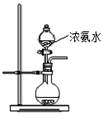
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用______ (选填字母编号);
A.碱石灰 B.生石灰 C.无水氯化钙 D.无水硫酸铜 E、烧碱
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是______ ,试写出制纳米级碳酸钙的化学方程式 ______ ;
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级______

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选 填字母):a接
用A装置制取NH3的化学反应方程式为
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用

A.碱石灰 B.生石灰 C.无水氯化钙 D.无水硫酸铜 E、烧碱
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】下图为从反面看到的某套实验装置示意图,无法看到实验说明,加热装置已经省略。

甲同学认为此套装置用于合成物质X,E处冰水冷却的U形管中有固体X(X溶于水得到中学化学常见强酸)出现;乙同学认为此套装置用于合成物质Y,E处冰水冷却的U形管中才有红棕色气体Y生成,并且越接近U形管底部颜色越浅。对于A处,甲认为有加热装置,乙认为没有。
(1)事实上此装置所附实验说明符合甲同学的推断,那么X的化学式是________ ,C装置中盛放的液体药品是___________ 。其作用是_______________________________ 。
(2)若要用上述装置完成乙同学所认为的实验,C处所起作用与合成X时所起作用相似,那么C处的广口瓶应改为_______________ ,所装药品为_______________ 。
(3)写出乙同学认为的D装置中发生反应的化学方程式_______________ 。为什么此时U形管中的红棕色气体越接近管底颜色越浅?__________________________________ 。

甲同学认为此套装置用于合成物质X,E处冰水冷却的U形管中有固体X(X溶于水得到中学化学常见强酸)出现;乙同学认为此套装置用于合成物质Y,E处冰水冷却的U形管中才有红棕色气体Y生成,并且越接近U形管底部颜色越浅。对于A处,甲认为有加热装置,乙认为没有。
(1)事实上此装置所附实验说明符合甲同学的推断,那么X的化学式是
(2)若要用上述装置完成乙同学所认为的实验,C处所起作用与合成X时所起作用相似,那么C处的广口瓶应改为
(3)写出乙同学认为的D装置中发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】归纳与演绎是重要的科学方法,也是常用的化学学习方法,请用该方法解决下列问题。
(1)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法。请你归纳出选择实验室制取气体反应发生装置,主要考虑因素有________ (填序号)。
①反应物的状态 ②生成气体的溶解性 ③反应条件 ④原料为纯净物 ⑤气体的密度
(2)研究课上,小明同学为了探究氨气的某些性质,做了以下实验(从左向右依次是他所做实验及现象)。

通过实验,小明同学可得出氨气的三点性质,分别是①______ ;②______ ;③________ 。
(3)在获得氨气的主要性质后,小明决定自己来制取氨气,他先查阅了有关资料,知道可通过多种反应得到NH3,他准备分别用以下两种化学反应来制备氨气,请结合所学帮助他完成氨气的实验制备方案。
①2NH4Cl(固体)+Ca(OH)2(固体) CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②CaO(固体)+NH3·H2O(浓)===NH3↑+Ca(OH)2
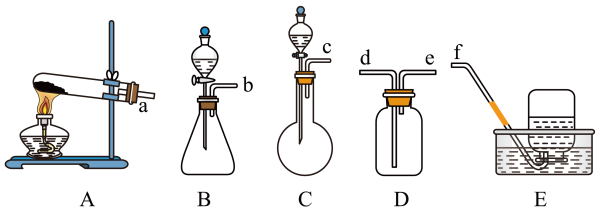
若选择反应①作为实验室制取NH3的反应原理,需要用上图装置中的________ 作NH3发生装置,若用E来收集氨气,实验过程中产生的后果是________________ ,若用D装置来收集,气体由________ 端导入。若选择反应②作为实验室制取NH3的反应原理,需要用上图装置中的________ 作NH3发生装置。
(1)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法。请你归纳出选择实验室制取气体反应发生装置,主要考虑因素有
①反应物的状态 ②生成气体的溶解性 ③反应条件 ④原料为纯净物 ⑤气体的密度
(2)研究课上,小明同学为了探究氨气的某些性质,做了以下实验(从左向右依次是他所做实验及现象)。

通过实验,小明同学可得出氨气的三点性质,分别是①
(3)在获得氨气的主要性质后,小明决定自己来制取氨气,他先查阅了有关资料,知道可通过多种反应得到NH3,他准备分别用以下两种化学反应来制备氨气,请结合所学帮助他完成氨气的实验制备方案。
①2NH4Cl(固体)+Ca(OH)2(固体)
 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O②CaO(固体)+NH3·H2O(浓)===NH3↑+Ca(OH)2

若选择反应①作为实验室制取NH3的反应原理,需要用上图装置中的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E五种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,C与A同主族;A与B、D、E所形成的常见化合物在常温下均呈气态,在周期表中D与E左右相邻,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数与E的最外层电子数相同。
请回答下列问题:
(1)B在元素周期表的位置为________________________ 。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序为_________ (用离子符号表示)。
(3)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物的水溶液与C的最高价氧化物的水化物反应的离子方程式为__________________________________________________ 。
(4)B的一种氢化物分子中含有18个电子,其化学式为_________________ 。
(5)BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种核外电子总数为10的气体,写出该反应的化学方程式_________________________________ 。
(6)下列事实能证明D与E非金属性强弱的是__________ (选填字母序号)。
A.比较这两种元素的气态氢化物的沸点 B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(7)已知D、E两种元素形成的化合物H,H结构与过氧化氢相似。5.4g的H中含有的电子数目为_______________ 。
请回答下列问题:
(1)B在元素周期表的位置为
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序为
(3)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物的水溶液与C的最高价氧化物的水化物反应的离子方程式为
(4)B的一种氢化物分子中含有18个电子,其化学式为
(5)BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种核外电子总数为10的气体,写出该反应的化学方程式
(6)下列事实能证明D与E非金属性强弱的是
A.比较这两种元素的气态氢化物的沸点 B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(7)已知D、E两种元素形成的化合物H,H结构与过氧化氢相似。5.4g的H中含有的电子数目为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是__________ :X与氢元素形成的化合物的电子式是__________ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,D与E能形成一种三核分子,该分子的结构式为__________ ;D所在族元素的氢化物中沸点最低的是__________ 。
(3)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为__________ 。
(1)该融雪剂的化学式是
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,D与E能形成一种三核分子,该分子的结构式为
(3)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E五种短周期主族元素,原子序数依次增大。A、B的族序数之和等于C的族序数,A、D同主族,且均可与C形成原子个数比为1∶1和2∶1的化合物,C元素形成的一种单质是地球的保护伞,E、C最外层电子数相同,根据以上信息回答下列问题:
(1)B的元素名称_______ 。
(2)写出D、C形成原子个数比1∶1化合物的电子式_______ 。
(3)由A、B、C三种元素中的两种元素可组成10电子的微粒:甲、乙、丙、丁,它们之间有如下关系:甲+乙 丙↑+丁,已知甲、丙所含元素相同,则甲是
丙↑+丁,已知甲、丙所含元素相同,则甲是_______ ,乙是_______ 。
(4)由A、C、D、E四种元素组成的两种酸式盐相互反应的离子方程式_______ 。
(1)B的元素名称
(2)写出D、C形成原子个数比1∶1化合物的电子式
(3)由A、B、C三种元素中的两种元素可组成10电子的微粒:甲、乙、丙、丁,它们之间有如下关系:甲+乙
 丙↑+丁,已知甲、丙所含元素相同,则甲是
丙↑+丁,已知甲、丙所含元素相同,则甲是(4)由A、C、D、E四种元素组成的两种酸式盐相互反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)请用下列10种物质的序号填空:①O2②H2③NH4NO3④K2O2⑤Ba(OH)2⑥CH4⑦CO2⑧NaF⑨NH3⑩I2。既有离子键又有非极性键的是________ ;既有离子键又有极性键的是________ ;只含离子键的是________ 。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为________ ;若XY2为共价化合物,其结构式为________ 。
(3)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为________ 。
(1)请用下列10种物质的序号填空:①O2②H2③NH4NO3④K2O2⑤Ba(OH)2⑥CH4⑦CO2⑧NaF⑨NH3⑩I2。既有离子键又有非极性键的是
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为
(3)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】过硫酸(H2S2O8)为无色晶体,易溶于水,在热水中易水解。
(1)依据硫酸和过硫酸的结构式,下列说法正确的是______ (填序号)。
a.硫酸和过硫酸均为共价化合物
b. 过硫酸分子中含有与过氧化氢分子中相同的化学键
c. 过硫酸分子可看作2个硫酸分子脱去1个水分子
(2)工业上利用过硫酸铵制备过氧化氢的一种方法如下图。
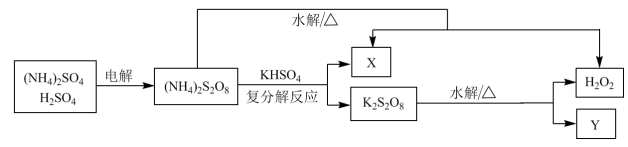
①电解法制(NH4)2S2O8过程中,得到S2 的电极反应式是
的电极反应式是______ 。
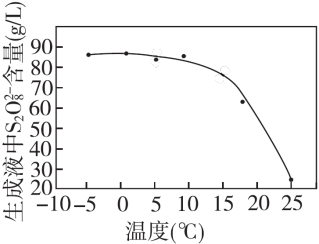
② 其他条件一定,电解相同时间后,测得生成液中S2 含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:
含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:______ 。
③X的化学式是______ 。
④过硫酸盐的水解反应______ (填“属于”或“不属于”)氧化还原反应。
⑤下图中a~e表示S2 中的部分化学键,则S2
中的部分化学键,则S2 发生水解反应时断裂的化学键是
发生水解反应时断裂的化学键是______ (选填字母)。

(3)过硫酸钾氧化法可用于分析锰钢中Mn元素的含量:取样品a g,加入过量浓硝酸,在加热条件下将Mn溶出,再用b L 过硫酸钾溶液将溶出的Mn2+全部转化为 ,检测
,检测 浓度,计算得出样品中Mn元素的质量分数为c。
浓度,计算得出样品中Mn元素的质量分数为c。
①该实验条件下氧化性:S2
______  (填“>”或“<”)。
(填“>”或“<”)。
②该过程中过硫酸钾溶液的浓度至少是______ mol/L(用含a、b、c的代数式表示)。
| 物质 | 硫酸 | 过硫酸 |
| 结构式 | 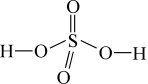 | 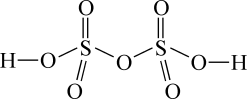 |
a.硫酸和过硫酸均为共价化合物
b. 过硫酸分子中含有与过氧化氢分子中相同的化学键
c. 过硫酸分子可看作2个硫酸分子脱去1个水分子
(2)工业上利用过硫酸铵制备过氧化氢的一种方法如下图。

①电解法制(NH4)2S2O8过程中,得到S2
 的电极反应式是
的电极反应式是② 其他条件一定,电解相同时间后,测得生成液中S2
 含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:
含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:
③X的化学式是
④过硫酸盐的水解反应
⑤下图中a~e表示S2
 中的部分化学键,则S2
中的部分化学键,则S2 发生水解反应时断裂的化学键是
发生水解反应时断裂的化学键是
(3)过硫酸钾氧化法可用于分析锰钢中Mn元素的含量:取样品a g,加入过量浓硝酸,在加热条件下将Mn溶出,再用b L 过硫酸钾溶液将溶出的Mn2+全部转化为
 ,检测
,检测 浓度,计算得出样品中Mn元素的质量分数为c。
浓度,计算得出样品中Mn元素的质量分数为c。①该实验条件下氧化性:S2

 (填“>”或“<”)。
(填“>”或“<”)。②该过程中过硫酸钾溶液的浓度至少是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】纳米材料二氧化钛(TiO2)可做优良的催化剂。
Ⅰ.工业上二氧化钛的制备方法:
①将干燥后的金红石(主要成分为TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4
②将SiCl4分离,得到纯净的TiCl4
③在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
④ TiO2·xH2O高温分解得到TiO2
(1)根据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是____ ,分离二者所采取的操作名称是______ 。
(2)③中反应的化学方程式是______ 。
Ⅱ.据报道:能“吃废气”的“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a. O2→2O b. O+H2O→2OH c. OH+OH→H2O2
(3)b中破坏的是_____ (填“极性共价键”或“非极性共价键”)。
(4)H2O2能清除路面空气中的CxHy、CO等,主要是利用了H2O2的_____ (填“氧化性”或“还原性”)。
Ⅲ.某研究性学习小组用下列装置模拟“生态马路”清除CO的原理。(夹持装置已略去)

(5)若缓慢通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重16.5g,则CO的转化率为______ 。
(6)当CO气体全部通入后,还要通一会儿空气,其目的是______ 。
| 资料卡片 | ||
| 物质 | 熔点/℃ | 沸点/℃ |
| SiCl4 | -70 | 57.6 |
| TiCl4 | -25 | 136.5 |
①将干燥后的金红石(主要成分为TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4
②将SiCl4分离,得到纯净的TiCl4
③在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
④ TiO2·xH2O高温分解得到TiO2
(1)根据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是
(2)③中反应的化学方程式是
Ⅱ.据报道:能“吃废气”的“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a. O2→2O b. O+H2O→2OH c. OH+OH→H2O2
(3)b中破坏的是
(4)H2O2能清除路面空气中的CxHy、CO等,主要是利用了H2O2的
Ⅲ.某研究性学习小组用下列装置模拟“生态马路”清除CO的原理。(夹持装置已略去)

(5)若缓慢通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重16.5g,则CO的转化率为
(6)当CO气体全部通入后,还要通一会儿空气,其目的是
您最近一年使用:0次



