下列说法中正确的是
| A.NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
| B.P4和CH4都是正四面体型分子且键角都为109.5° |
C.NH 的电子式为 的电子式为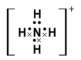 ,离子呈平面正方形结构 ,离子呈平面正方形结构 |
| D.NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 |
更新时间:2022-08-18 18:43:38
|
【知识点】 键能、键长、键角及应用解读
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】表中原子化热、晶格能、键能的单位都是kJ·mol-1
则下列说法正确的是
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
则下列说法正确的是
| A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ |
| B.Si(s)+2Cl2(g)=SiCl4(g) △H= -602kJ·mol-1 |
| C.从表中可以看出,氯化钠的熔点比晶体硅高 |
| D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.石墨晶体呈层状结构,每个碳原子只有3个价电子形成共价键 |
| B.白磷是正四面体分子,键角是109°28′,1摩尔白磷含共价键6NA个 |
| C.臭氧是直线型分子,等质量的臭氧和氧气所含的氧原子数相同 |
| D.S8是分子晶体,8个硫原子形成环状结构,摩尔质量为256g |
您最近一年使用:0次

 中两个氢氧键(H—O)的键角大于
中两个氢氧键(H—O)的键角大于 的键角
的键角 分子中的四个原子在同一平面上
分子中的四个原子在同一平面上 是非极性分子,C原子处于4个Cl原子所组成的正方形的中心
是非极性分子,C原子处于4个Cl原子所组成的正方形的中心

