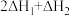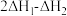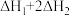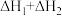题型:单选题
难度:0.65
引用次数:883
题号:16795644
 和
和 反应生成
反应生成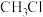 和HCl的部分反应进程如图所示。
和HCl的部分反应进程如图所示。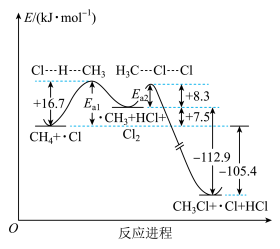
已知总反应分3步进行:
第1步
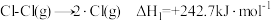 ;
;第2步
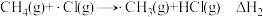 ;
;第3步
 。
。下列有关说法正确的是
A. |
| B.第2步的反应速率小于第3步的反应速率 |
| C.减小容器体积增大压强,活化分子百分数增加,反应速率加快 |
D.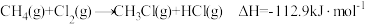 |
更新时间:2022-09-14 19:49:07
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列图示与对应的叙述相符的是
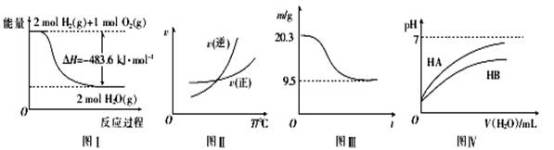

| A.图I表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H = -241.8 kJ.mol-1 |
| B.图Ⅱ表示某可逆反应正、逆反应速率随温度的变化,则该反应的正反应是放热反应 |
| C.图Ⅲ表示0.1 mol MgCl2.6H2O在空气中充分加热时固体质量随时间的变化 |
| D.图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用图1 和图2中的信息,按图3装置(连接的A、B瓶中已充有NO2气体)进行实验。下列说法正确的是
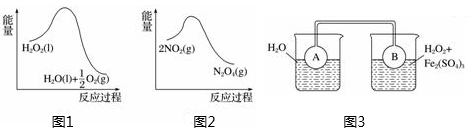

| A.H2O2中只含有极性共价键,不含离子键 |
B.2NO2 N2O4的平衡常数K随温度升高而减小 N2O4的平衡常数K随温度升高而减小 |
| C.向H2O2中加入Fe2(SO4)3后,B中颜色变浅 |
| D.H2O2分解反应中Fe2(SO4)3作催化剂,可以使反应的△H减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
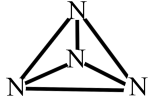
【推荐1】已知:①N4分子的结构式如图所示;②N—N键的键能为167kJ·mol-1,N≡N键的键能为942kJ·mol-1;③N2(g)+3H2(g) 2NH3(g) △H=-92.2kJ·mol-1。则反应N4(g)+6H2(g)=4NH3(g)的△H为
2NH3(g) △H=-92.2kJ·mol-1。则反应N4(g)+6H2(g)=4NH3(g)的△H为
 2NH3(g) △H=-92.2kJ·mol-1。则反应N4(g)+6H2(g)=4NH3(g)的△H为
2NH3(g) △H=-92.2kJ·mol-1。则反应N4(g)+6H2(g)=4NH3(g)的△H为
| A.-1066.4kJ·mol-1 | B.+1066.4kJ·mol-1 |
| C.+697.6kJ·mol-1 | D.-697.6kJ·mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组气体通常条件下不能相互发生化学反应的是
| A.SO2和H2S | B.Cl2和CO2 | C.H2和F2 | D.NH3和HCl |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学小组进行如下实验:在锥形瓶A中放入5.6 g铁粉,在锥形瓶B中放入相同质量的铁片,分别加入100 mL 1 mol/L盐酸。图中(x表示时间,y表示生成氢气的体积)能正确表示实验结果的是
A. | B.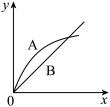 |
C.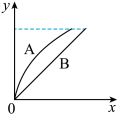 | D.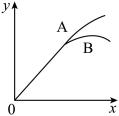 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述不正确的是
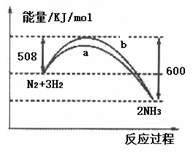

| A.在温度、体积一定的条件下,通入1mol N2和3mol H2 反应后放出的热量为92kJ |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,也不能提高N2的转化率 |
D.该反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=﹣92 kJ/mol 2NH3(g) △H=﹣92 kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组采用等质量的大理石和碳酸钻粉末、足量的 稀盐酸和
稀盐酸和 稀硫酸研究实验室制备
稀硫酸研究实验室制备 的化学反应速率。实验中
的化学反应速率。实验中 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。
已知:碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙会包裹在碳酸钙表面。
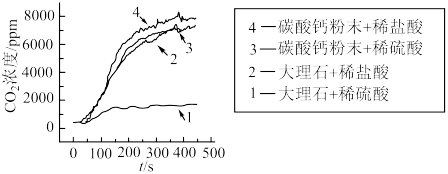
下列说法正确的是
 稀盐酸和
稀盐酸和 稀硫酸研究实验室制备
稀硫酸研究实验室制备 的化学反应速率。实验中
的化学反应速率。实验中 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。已知:碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙会包裹在碳酸钙表面。

下列说法正确的是
A.比较实验1和实验2,可以说明酸的 对生成 对生成 的速率有影响 的速率有影响 |
B.比较实验1和实验4,可以说明生成 的速率和酸中阴离子的种类有关 的速率和酸中阴离子的种类有关 |
C.实验结论:生成的 对碳酸钙粉末比对大理石的包裹作用更强 对碳酸钙粉末比对大理石的包裹作用更强 |
D.综合以上四个实验推断大理石粉末和稀硫酸反应能用于制备 |
您最近半年使用:0次

 (g)和
(g)和 (g)的相对能量为0,下列说法不正确的是
(g)的相对能量为0,下列说法不正确的是
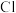 (g)在历程Ⅱ中作催化剂
(g)在历程Ⅱ中作催化剂 的平衡转化率:历程Ⅱ>历程I
的平衡转化率:历程Ⅱ>历程I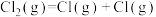 的
的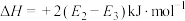





 的
的 为
为